查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





作者:复旦大学附属中山医院 刘玥隽 胡沁 刘亚岚 凌雁
1例43岁男性患者,因“发现甲状腺结节4月余”就诊。
患者4月余前在我院体检,彩超检查发现甲状腺双侧叶数个混合回声团块,左叶较大一枚10mm×7mm,内见点状彩色血流,内部回声均匀,建议短期随访。当时甲功正常,降钙素升高,为66.3pg/ml。患者无吞咽困难、呼吸不畅、声音嘶哑等不适。患者随后于我院连续3个月随访降钙素水平均升高,分别为90.0pg/ml、66.5pg/ml和99.5pg/ml,查癌胚抗原(CEA)正常。患者既往糖尿病病史,服用二甲双胍治疗,血糖控制可;高脂血症病史,服用非诺贝特、瑞舒伐他汀降脂治疗,血脂控制可。否认家族甲状腺疾患病史。
体格检查:血压、心率正常,心、肺、腹部查体阴性。甲状腺未及肿大,未触及明显结节。
患者为中年男性,体检发现甲状腺结节,多次查降钙素升高,需要完善甲状腺细针穿刺,以明确病变性质。患者于门诊行超声引导下甲状腺左叶结节细针穿刺,细胞病理示:甲状腺左叶送检涂片见大量小圆形细胞,倾向肿瘤性病变(髓样癌不能除外)(图1)。
患者于普外科行甲状腺癌扩大根治术。术中探查甲状腺左叶可扪及一肿块,范围约1.0cm,实质性,质地较硬。双侧气管旁、颈动脉旁未及肿大淋巴结。术中完整切除甲状腺左叶、峡部及甲状腺右叶,并清扫左侧颈部Ⅲ、Ⅳ区淋巴结,以及中央区淋巴结。术中冰冻病理报告提示:左甲状腺叶+峡部结合形态学及血清降钙素水平,考虑髓样癌。
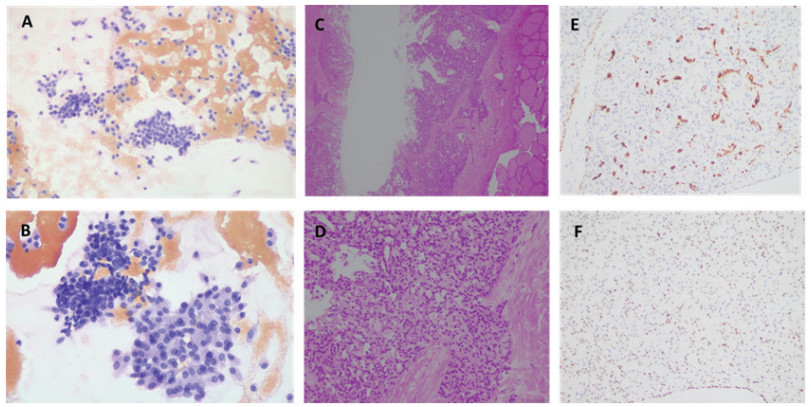
图1 细胞病理和组织病理。A:细胞散在失黏附排列,有浆细胞样、多角形、圆形及梭形等细胞形态。B:细胞内显示“椒盐样”染色质,部分细胞核浆比增大。C:肿瘤周围见纤维胶原包膜,同时可见肿瘤组织侵入包膜。D:肿瘤生长方式以类癌的器官样结构、腺泡状结构为主,细胞呈多角形,胞浆丰富,略呈颗粒状;肿瘤细胞巢被纤维胶原带分割。E:免疫组化染色显示降钙素。F:免疫组化染色显示TTF-1
三碘甲状腺原氨酸(TT3)1.3nmol/L;甲状腺素(TT4)99.1nmol/L;游离三碘甲状腺原氨酸(FT3)4.0pmol/L;游离甲状腺素(FT4)15.8pmol/L;超敏促甲状腺激素(TSH)2.750uIU/ml;甲状腺球蛋白(TG)12.50ng/ml;抗甲状腺球蛋白抗体(TGAb)10.8IU/ml;抗甲状腺过氧化物酶抗体(TPOAb)<9.0IU/ml;促甲状腺激素受体抗体(TRAb)<0.8IU/L。
降钙素72.6pg/ml;CEA3.4ng/ml;血钙2.42mmol/L,血磷1.25mmol/L,甲状旁腺激素29.3pg/ml;
空腹血糖5.9mmol/L,糖化血红蛋白6.5%;总胆固醇4.20mmol/L,甘油三酯1.26mmol/L,低密度脂蛋白胆固醇2.46mmol/L,高密度脂蛋白1.17mmol/L。促肾上腺皮质激素(8点)43.4pg/ml,皮质醇(8点)376.0nmol/L;促肾上腺皮质激素(16点)21.2pg/ml,皮质醇(16点)178.0nmol/L;
促肾上腺皮质激素(0点)7.3pg/ml,皮质醇(0点)48.8nmol/L;甲氧基肾上腺素38.4pg/ml,甲氧基去甲肾上腺素149.5pg/ml,3-甲氧酪胺<12.5pg/ml;醛固酮63.4pg/ml,肾素活性0.906ng/(ml·h)。
甲状腺超声:甲状腺右叶42mm×13mm×14mm,甲状腺左叶40mm×12mm×13mm,峡部3mm。右侧叶内见数个混合回声团块,最大8mm×6mm,左叶中下极见9mm×8mm低回声团块,边界尚清,隐约见点状强回声,彩色多普勒血流显像(CDFI)见短线状彩色血流。甲状腺内部回声均匀,甲状腺内血流分布正常。双侧颌下、双侧颈血管旁及双侧锁骨上未见明显肿块回声。CDFI未见异常血流。结论:甲状腺左叶结节,性质待定;甲状腺右叶增生结节。
甲状腺左叶+峡部巨检:腺叶大小5.8cm×3cm×1.1cm,峡部大小2cm×1.5cm×0.5cm,多切面切开,距峡切2.0cm、距被膜0.3cm,于腺叶中上极见一结节,最大径0.9cm,切面灰白灰红、质软、界尚清,似带包膜。免疫组化CK19(部分+),CEA(+++),Ki-67(1%阳性),CD56(+++),CgA(++),SYN(++),Calcitonin(少量+),TG(-),TTF-1(+),PAX-8(散在+),GATA3(-)。病理诊断:甲状腺左叶+峡部符合髓样癌(图1)。
甲状腺右叶巨检:腺叶组织大小4cm×3.5cm×2cm,书页状切开,于甲状腺叶中极见一胶样结节,大小1cm×0.8cm×0.5cm,周围甲状腺未见特殊。病理诊断:甲状腺右叶滤泡增生结节。
(左中央区淋巴结)送检淋巴结2枚,1枚见癌转移(1/2)。免疫组化:CK19(-);SYN(+)。(左颈3区淋巴结)检出淋巴结5枚,均未见癌转移(0/5)。
术后予以患者左甲状腺素钠片100μg每日1次口服。术后1月复查FT32.6pmol/L,FT416.3pmol/L,TSH42.2uIU/ml,TG0.04ng/ml,降钙素水平低于检测下限,增加左甲状腺素钠片用量为150μg每日1次口服。术后3月复查颈部彩超提示甲状腺及颈部未见占位。术后3月、6月随访降钙素均低于检测下限。
甲状腺髓样癌(MTC)是起源于甲状腺滤泡旁细胞(C细胞)的恶性肿瘤,其发病率较低,仅占甲状腺癌的3%~5%。甲状腺滤泡旁细胞特征性的表达和分泌降钙素(Ctn),故血清Ctn是MTC的肿瘤标志物,其对于诊断MTC的敏感性和特异性均较高,同时其检测费用较低。目前对于甲状腺结节患者是否常规测定Ctn的意见并不统一,指南也没有明确推荐。然而,现有的证据表明Ctn筛查有助于早期诊断MTC,并且手术后的完全缓解率也明显提高。
需要注意的是,慢性肾功能衰竭和其他疾病患者的血清Ctn水平可能会轻度升高,如甲状旁腺功能亢进、自身免疫性甲状腺炎、肺癌、前列腺癌、肥大细胞增多症以及各种肠道和肺神经内分泌肿瘤。本例患者血清Ctn水平多次接近100pg/ml,无上述相关疾病史,故考虑血清Ctn升高可能源于甲状腺。
血清Ctn水平越高,诊断为MTC的可能性越大。血清Ctn>100pg/ml的甲状腺结节患者,基本均为MTC。即使血清Ctn轻度增高,也不能除外MTC。小MTC(直径≤1.5cm)近年来诊断率越来越高,可能是因为甲状腺结节常规进行了Ctn测定。针对小MTC的研究发现,血清Ctn的水平与肿瘤大小密切相关,直径在0.1~0.5cm,0.6~0.8cm,0.9~1.0cm和1.1~1.5cm的小MTC的血清Ctn的中位数分别为33.3pg/ml,82.5pg/ml,140.5pg/ml和189pg/ml。本例患者的血清Ctn水平为66.3pg/ml~99.5pg/ml,与其肿瘤大小相当。C细胞也分泌CEA,但CEA的特异性不强,无法作为MTC理想的筛查指标。但一经诊断为MTC,仍建议同时检测血清CEA浓度。CEA升高程度与肿瘤外侵、淋巴结转移和远处转移呈正相关,可与Ctn一起用于风险评估。该患者进行了超声引导下的细针穿刺活检(FNA)。结合其血清Ctn增高及细胞病理表现,高度怀疑为MTC。MTC的FNA细胞学病理表现多变,细胞通常不互相黏附,可能是纺锤形的,浆细胞样的,或表皮样的,因此容易被误诊。ATA指南建议:如FNA结果不确定或提示MTC,应在FNA冲洗液中测量降钙素,并对FNA样本进行免疫化学染色,以检测是否存在Ctn、嗜铬粒蛋白和CEA等标志物以及甲状腺球蛋白的缺失。该患者最后接受了甲状腺全切及颈淋巴结清扫,术后病理确诊为MTC。该病例虽为散发性微小MTC,但由于MTC较高的多灶和双侧发病概率,主流意见仍推荐将全甲状腺切除作为初始的手术治疗方式。MTC的体积越小,包膜和淋巴结侵犯的概率越低,手术治愈的可能性越大,其预后越好。MTC术前的基线血清Ctn水平与有无淋巴结转移和远处转移,以及术后能否达到生化缓解等密切相关。MTC术后的血清Ctn水平则是预测肿瘤复发进展的重要标志物。针对小MTC的研究表明:术后Ctn水平>4.65pg/ml预测肿瘤有残留(敏感性93.8%,特异性90%)和>14.5pg/ml预测肿瘤进展(敏感性100%,特异性82%)。微小MTC较少有侵袭性的行为,预后较好。本例患者为偶然发现的微小MTC,术前Ctn水平轻度增高,CEA正常,术后Ctn水平无法测得,获得良好预后的可能性较大,但必须进行长期规范的随访。临床上1%~7%的散发性MTC患者实际具有遗传性MTC的基因背景,因此建议对散发性病例行RET基因突变筛查,可进一步明确疾病分型,也有助于发现复发高风险的患者。因此,该患者虽然没有MTC家族史,也建议对其进行RET基因突变筛查。
5月31日,特邀
复旦大学附属中山医院 凌雁教授
线上答疑
关于本病例,或临床中甲状腺疾病诊治相关问题,欢迎评论区留言~

查看更多