查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





8月24日下午,由中华医学会肝病学分会、感染病学分会共同制订的2019年版《丙型肝炎防治指南》(征求意见稿)(以下简称“新版指南”)于“第十九次全国病毒性肝炎及肝病学术会议暨2019年中华医学会肝病学分会年会、中华医学会感染病学分会年会”期间发布。大会共同主席、中华医学会肝病学分会前任主任委员、首都医科大学附属佑安医院段钟平教授对指南进行了详细解读。

目前,抗丙型肝炎病毒(HCV)治疗已进入直接抗病毒药物(DAA)的泛基因型时代。新版指南对中国的泛基因型DAA方案进行了重点推荐,并且在诊疗流程上也进行了适当的简化,在2015年版指南基础上进行了更新和修订,共提出39条推荐意见。


流行病学
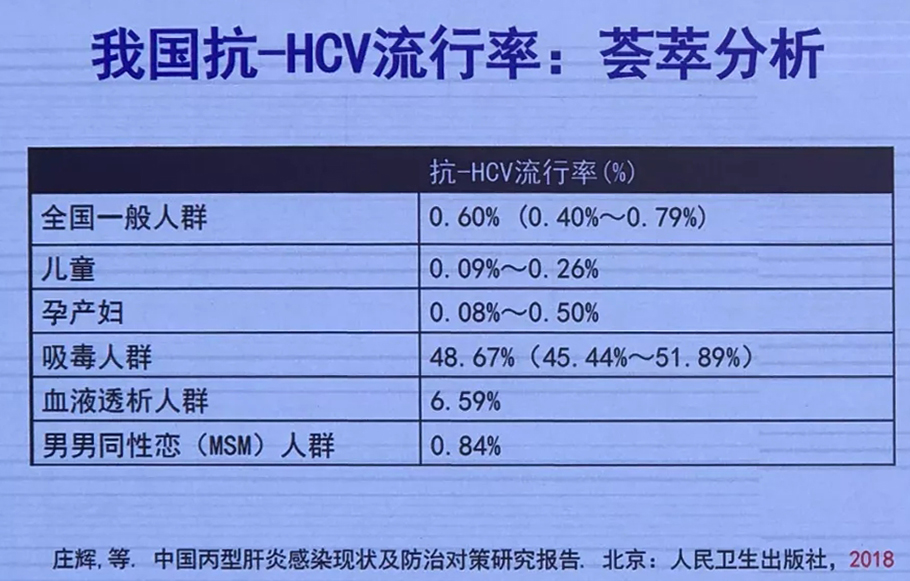
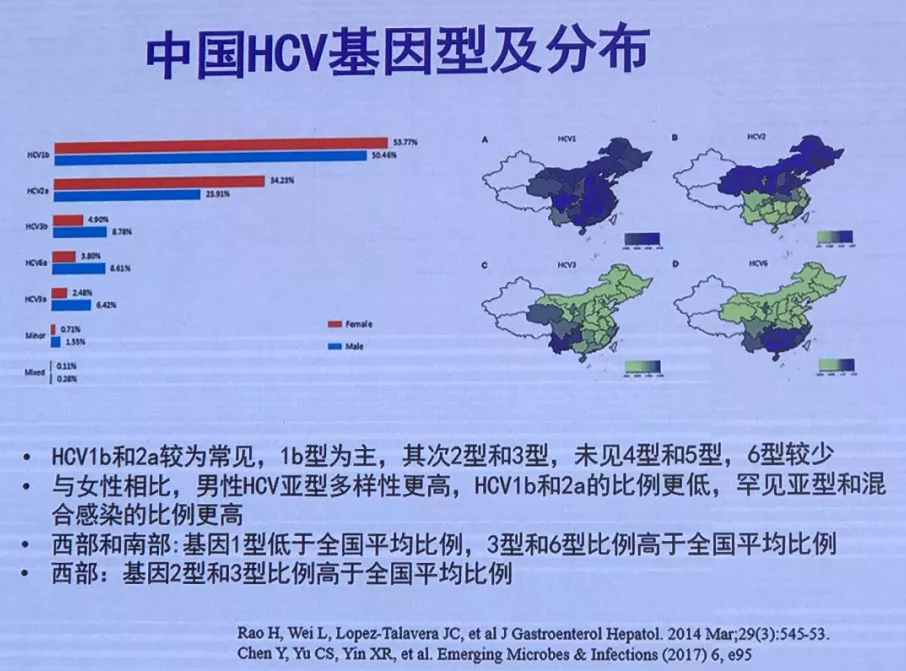
新版指南中加入了新的流行病学资料。2018年全国丙型肝炎感染现状及防治对策研究报告显示,我国一般人群抗HCV 流行率为0.6%。目前,全国大约有1000 万HCV感染者,以基因1b型和2a型为主。
预防
医疗卫生机构和体检机构可在体检人员知情同意前提下,将丙型肝炎检测纳入健康体检范畴;预防医源性传播,医疗机构要落实手术、住院、血液透析、侵入性诊疗等患者的丙型肝炎检查规定;积极治疗和管理感染者,新版指南强调,只要诊断为HCV感染,不论疾病分期如何,所有12岁或以上的感染者均应该接受治疗。
推荐意见-1
HCV感染筛查方案应根据当地HCV感染的流行病学情况制订,最好纳入国家防控计划中。可以根据中华人民共和国卫生行业标准《丙型肝炎筛查及管理》对丙型肝炎高危人群进行筛查及管理。(B1)
实验室检查
血清学检测
指南强调,采用基因型特异性DAAs方案治疗的感染者,需要先检测基因型。
推荐意见-2:
如果抗-HCV阳性,应进一步检测血清或血浆HCV RNA或HCV核心抗原(HCV RNA检测不可及时)检测,以明确患者是否有现症感染。(A1)
肝纤维化无创诊断
血清学和/或瞬时弹性成像(TE)等可帮助判断是否存在肝硬化或纤维化;对于肝硬化诊断效能优于显著肝纤维化(A1)。两者联合,可以提高显著肝纤维化的诊断准确率;两者结果不一致时,建议进行肝活检明确诊断(A1)
影像学和病理学诊断
新版指南对核磁共振(MRI)、CT、腹部超声(US)检查方法进行了比较。指南强调,MRI动态增强多期扫描及特殊增强剂显像对鉴别良性和恶性肝内占位性病变优于CT。此外,新版指南不再使用METAVIR评分系统用于病理诊断。

抗病毒治疗适应证
新版指南强调,以下人群应立即进行抗病毒治疗:① 进展期肝纤维化或肝硬化患者;② 显著肝外表现患者(如HCV相关混合冷球蛋白血症血管炎、HCV 免疫复合物相关肾炎、非霍奇金B细胞淋巴瘤等);③肝移植后HCV复发患者合并加速肝病进展的疾病;④ 传播HCV高风险的患者。
指南推荐,所有HCVRNA阳性患者,均应接受抗病毒治疗(A1);抗病毒治疗终点为治疗结束后12或24周,采用敏感检测方法(检测下限≤15 IU/ml)检测血清或血浆HCVRNA阴性[持续病毒学应答(SVR)12或24](A1);育龄期女性在DAAs治疗前先筛查是否已经妊娠,已经妊娠者,可在分娩后哺乳期结束后给予抗病毒治疗。如排除妊娠,则应告知,避免在服用DAAs 时妊娠(B1)。

治疗前评估
推荐意见-8:丙型肝炎患者进行抗病毒治疗前,需评估肝脏疾病的严重程度、肾脏功能、HCV RNA定量检测、HCV基因型、HBsAg、合并疾病以及合并用药情况。当基因型检测不可及并且当地HCV基因3b流行率低于5%,可不检测基因型。(B1)

治疗和管理
泛基因型方案
索磷布韦/维帕他韦治疗基因1-6型初治或者聚乙二醇干扰素联合利巴韦林(PR)经治患者,无肝硬化或代偿期肝硬化疗程12周,针对基因3型代偿期肝硬化或者3b型患者可以考虑增加利巴韦林,失代偿期肝硬化患者联合利巴韦林疗程12周(A1)。
格卡瑞韦/哌仑他治疗基因1-6型患者,初治无肝硬化患者疗程8周,初治代偿期肝硬化患者疗程12周;PR经治患者,非基因3型无肝硬化患者8周,代偿期肝硬化患者12周;基因3型PR经治患者疗程16周(A1)。
此外,考虑到DAAs方案的可负担性,部分DAAs联合聚乙二醇干扰素的方案可应用于临床。(A1)
表1 泛基因型DAA药物
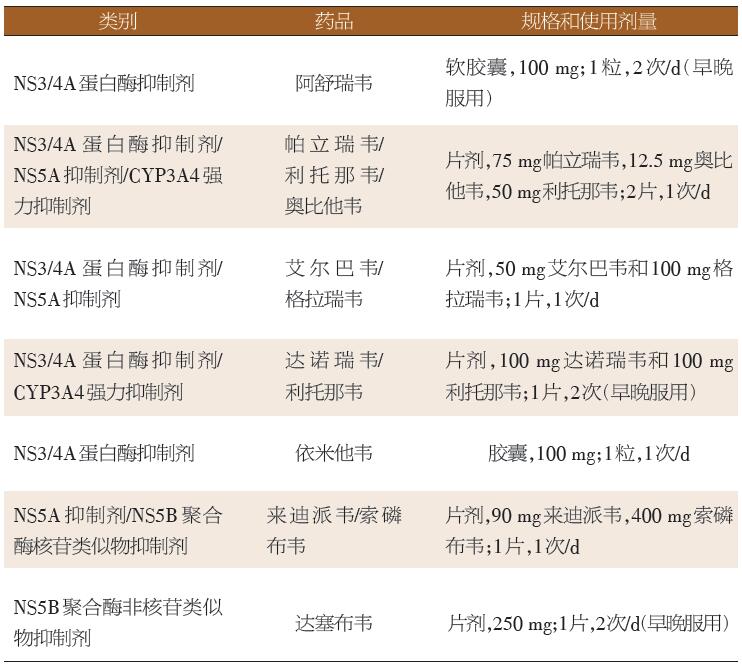
表2 基因特异性型DAA药物
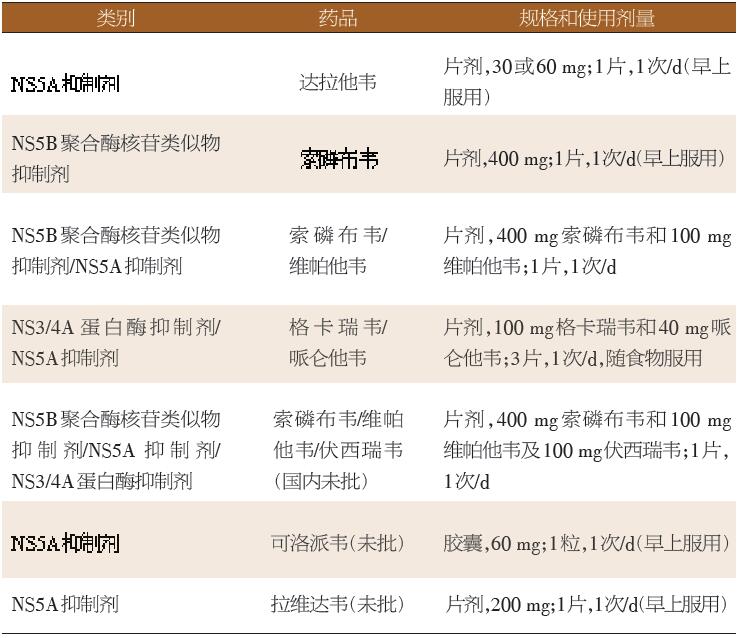
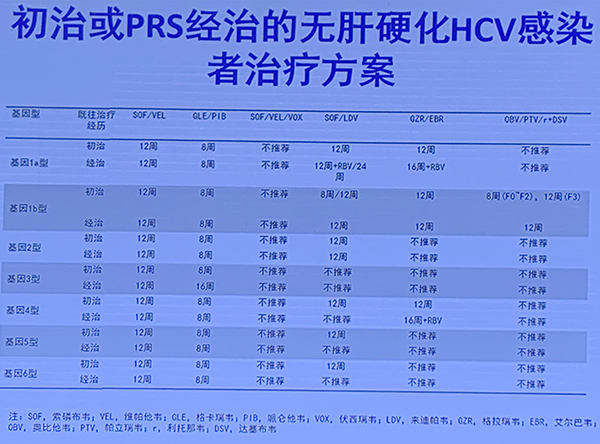
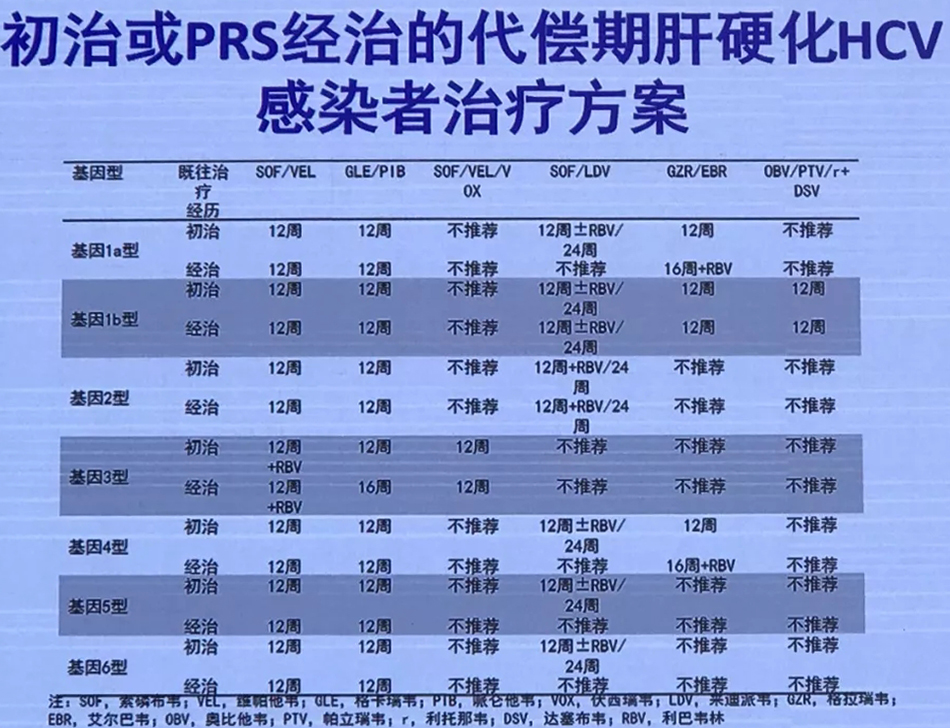
特殊人群
指南强调,要注意HCV特殊人群的治疗和管理;肝硬化患者获得SVR,仍然有肝细胞癌发生可能,需要定期检测。

推荐意见-17:
肝硬化失代偿期或曾有失代偿病史禁止使用NS3/4A蛋白酶抑制剂类DAAs以及干扰素;肝硬化失代偿期患者:可选择来迪派韦/索磷布韦(基因型1、4、5和6)或索磷布韦维帕他韦(泛基因型)或索磷布韦/达拉他韦(泛基因型),以及利巴韦林(<75 kg,1000 mg/d;≥75 kg,1200 mg/d)治疗12周;如果患者且有利巴韦林禁忌或无法耐受利巴韦林,则不联合利巴韦林,但疗程延长至24周(A1)
推荐意见18-19:
基因型特异性方案,12岁及以上或者体重超过35 kg的青少年
— HCV GT1,4,5,6:400mg索磷布韦/90mg来迪派韦治疗12周,经治代偿期肝硬化患者疗程延长至24周。
— HCV GT2,400 mg索磷布韦联合利巴韦林12周;HCV GT3,治疗24周。
泛基因型方案,12岁及以上或者体重超过45 kg青少年
—HCV GT1-6:格卡瑞韦100mg/哌仑他韦40mg,初治无肝硬化8周,初治代偿期肝硬化12周,经治无肝硬化或者代偿期肝硬化16周,无需调整剂量(B1)
12岁以下儿童,目前尚未有推荐的DAA治疗方案。(B1)
推荐意见20-23:
所有合并HCV感染CKD患者,均应积极立即抗病毒治疗(A1)
CKD 1-3b期(eGFR≥30 ml/min/1.73m2):DAA选择与无CKD一致(A1)。
CKD 4-5期(eGFR< 30 ml/min/1.73m2)和CKD 5D期(透析):① 格拉瑞韦艾尔巴韦,基因1、4型;② 格卡瑞韦哌仑他韦,泛基因型;③ 二线选择,奥比帕利/达塞布韦(基因1型),阿舒瑞韦/达拉他韦(基因1b型,阿舒用于未透析的CKD 4-5期患者时剂量减半)(A1)。
肾移植后CKD 1-3b期患(eGFR≥ 30ml/min/1.73m2):① 索磷布韦/来迪派韦,基因1、4、5、6型;② 索磷布韦维帕他韦,泛基因型;③不需要调整免疫抑制剂剂量。
肾移植后CKD 4-5期(eGFR≥ 30ml/min/1.73m2)和CKD 5D期(透析):格卡瑞韦哌仑他韦(泛基因型):监测免疫抑制剂血药浓度,必要时调整剂量。(A1)
推荐意见24-27:
等待肝移植且MELD评分<18-20分:移植前尽快治疗,可能从等待名单中移除。MELD评分≥18-20分:先肝移植 ,再抗HCV治疗;若等待时间超过6个月,根据具体情况移植前抗HCV治疗。(A1)
等待肝移植、无肝硬化或代偿期肝硬化:应移植前开始抗病毒;如立即肝移植,也可移植后抗病毒。(A1)
移植后HCV复发或者再感染:无肝硬化或代偿期肝硬化,来迪派韦/索磷布韦(基因型1、4、5和6)或索磷布韦/维帕他韦(泛基因型),治疗12周;失代偿期肝硬化,来迪派韦/索磷布韦(基因型1、4、5和6)或索磷布韦/维帕他韦(全基因型)以及利巴韦林12周,如果有利巴韦林禁忌或不耐受则24周。(A1)
移植后HCV复发、非失代偿期肝硬化eGFR<30ml/min/1.73m2:格卡瑞韦/哌仑他韦12周。(B1)
推荐意见28-29:
所有感染HCV的PWID都应立即接受抗病毒治疗,选择无IFN的全口服DAA。(B1)
SVR后随访中HCV再次感染者应再次予抗HCV治疗。(B1)
推荐意见30:
对于血友病、地中海贫血、镰刀细胞贫血等血液系统疾病患者合并HCV感染时,HCV抗病毒治疗的指征不变。
选择无IFN、无利巴韦林的全口服DAA,具体方案同普通患者。(B1)
推荐意见31:
有精神病史HCV患者:无IFN的DAAs抗HCV治疗(B1)
推荐意见32:
合并HBV感染,HCV治疗与单纯HCV感染治疗方案相同:同时符合HBV抗病毒治疗指征,予以IFN或核苷类似物抗HBV治疗;不符合HBV抗病毒指征,抗HCV治疗监测HBV DNA,HBV DNA活动时予以核苷类似物(B1)
推荐意见33:
合并HIV感染时,HCV治疗与单纯HCV感染DAA方案相同(B1)
推荐意见34:
急性丙型肝炎患者:治疗8周(B1)。
— 泛基因型方案:索磷布韦/维帕他韦;格卡瑞韦/哌仑他韦;
— 基因型特异性方案:格拉瑞韦/艾尔巴韦(基因型1b或4);来迪派韦/索磷布韦(基因型1,4,5,6);奥比帕利/达塞布韦(基因型1b)。
推荐意见35:PRS经治
选择的DAA治疗方案与初治患者类似;仅有一些基因型或者肝硬化的患者需要延长疗程(A1)。
推荐意见36:无肝硬化或代偿期肝硬化、DAA经治患者
索磷布韦/维帕他韦/伏西瑞韦,治疗12周;索磷布韦联合格卡瑞韦/哌仑他韦,治疗12周(B2)。
推荐意见37:DAA经治失败2次的患者
下列方案加用利巴韦林12周,①索磷布韦/维帕他韦/伏西瑞韦;② 索磷布韦联合格卡瑞韦/哌仑他韦(C2)。
推荐意见38:失代偿期肝硬化或失代偿病史、DAA经治患者
索磷布韦/维帕他韦,加用利巴韦林治疗24周(B2)。
推荐意见39:
未治疗或治疗失败的患者,以无创诊断方式每年复查、评价一次肝纤维化的进展情况对于有肝硬化基础的患者,无论是否获得SVR,每6个月复查一次腹部超声和AFP。

(中国医学论坛报 徐嘉惠 整理 段钟平教授 审阅)
查看更多