查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





讲者:复旦大学华山医院抗生素研究所 王明贵教授

王明贵教授
王明贵教授介绍,自20世纪80年代起,抗菌药物的研发在经历一段低潮之后,已逐渐走出低谷。21世纪以来,上市的新抗菌药物多为对耐药革兰阳性菌具抗菌活性的抗菌药物,但这类药物的临床需求较少。2014年以后,广谱新抗菌药的数量逐渐增多。近10年来,上市的新抗菌药物以抗革兰阳性球菌(GPC)的新抗菌药物、抗革兰阴性杆菌(GNB)的新抗菌药物和广谱抗菌新药为主。接下来,王明贵教授对以上新抗菌药物特点进行介绍。
替拉凡星、达巴凡星和奥他凡星是脂糖肽类的3个新抗菌药物。此类药物的半衰期较长,可每周给药1次,且在组织中消除速率慢,中重度肾功能损伤、中度肝损伤的时不需调整剂量。这类药物对大部分革兰阳性菌的疗效较好,但在国内临床需求不高,因此使用较少。
利法呋林(Lefamulin)是一种新型剪短侧耳素类衍生物,该药的抗菌谱类似大环内酯类,但较之作用更强,并且对耐甲氧西林金黄色葡萄球菌(MRSA)也更有效。Lefamulin具有静脉和口服制剂。在空腹情况下,口服生物利用度达25.8%。2019年8月,该药在美国同时批准静脉及口服制剂治疗社区获得性肺炎(CAP)。今后可能将急性细菌性皮肤和皮肤结构感染(ABSSSIs)、骨关节炎、性传播疾病(STD)、儿童感染列入其适应证中。
特地唑胺(Torezolid)为唑烷酮类抗生素,对葡萄球菌、肠球菌及链球菌属的抗菌活性较利奈唑胺强4~8倍,对携带基因的利奈唑胺耐药菌株具抗菌活性,最低抑菌浓度(MIC)<2mg/L,给药方案为200 mg ,qd ,口服。2014年6月,美国FDA批准该药用于治疗复杂性皮肤软组织感染,2019年2月,中国批准该药治疗皮肤软组织感染。与利奈唑胺相比,Torezolid胃肠道反应及骨髓移植发生率低,并且具有静脉及口服制剂。
头孢罗膦(ceftaroline)
ceftaroline在体内快速水解为ceftaroline而起抗菌作用,对包括MRSA在内的革兰阳性菌具良好抗菌活性,此外,对粪肠球菌也具一定抗菌作用。ceftaroline对非产对超广谱β-内酰胺酶(ESBL)的肠杆菌科细菌的抗菌活性与头孢他啶相仿,对不发酵糖细菌无抗菌活性。2010年10月,美国FDA批准该药用于治疗急性细菌性皮肤软组织感染和社区获得性细菌性肺炎;目前,中国已完成CAP, ABSSSI的Ⅲ期临床试验。Ceftaroline的推荐给药方案为600mg,q12h,静脉滴注。
头孢比罗(Ceftobiprole)
Ceftobiprole为广谱头孢菌素,与青霉素结合蛋白(PBP)2a的结合力强。对革兰阳性菌的抗菌活性强,对MRSA、万古霉素耐药及中等耐药金黄色葡萄球菌(VRSA/VISA)均具抗菌活性。该药对革兰阴性杆菌包括铜绿假单胞菌的抗菌活性和抗菌谱与头孢他啶和头胞吡肟相仿。2008年3月,美国FDA批准Ceftobiprole上市,用于治疗复杂性皮肤软组织感染(包括糖尿病足感染),后因故被撤;2014年欧洲批准该药上市;中国正在申请注册上市。Ceftobiprole的主要不良反应为恶心等胃肠道反应和静脉炎。
奈诺沙星(nemonoxacin)
nemonoxacin为无氟喹诺酮类,具有广谱抗菌活性,对MRSA、耐青霉素肺炎链球菌(PRSP)具抗菌活性,对流感嗜血杆菌、卡他莫拉菌的抗菌作用也有增强。该药是中国首次批准上市的1.1类新药。2016年5月,CFDA批准该药治疗CAP,2019年被列入国家医保国谈目录。
西他沙星(Sitafloxacin)
Sitafloxacin抗菌活性全线增强,对包括MRSA的革兰阳性菌,包括铜绿假单胞菌的革兰阴性菌,厌氧菌以及非结核分枝杆菌(NTM)均有抗菌作用。并且对DNA旋转酶及拓扑异构酶Ⅳ有较强的双重抑制作用,对部分环丙沙星大肠埃希菌(60%~709%)有抗菌活性。Sitafloxacin具有良好的药动学特性,每日只需1次给药。该药批准用于呼吸道感染、尿路感染的治疗。推荐剂量为100mg,qd;对于中重度复杂患者的推荐剂量为100mg,bid。
德拉沙星 (delafloxacin)
delafloxacin对MRSA具抗菌活性,对其敏感率为87.6%。该药口服生物利用度58.8%,蛋白结合率84%,口服半衰期为3.7h,静脉半衰期为4.2-5.8h。美国批准皮肤软组织感染和社区获得性细菌性肺炎(CABP)为其适应证。
阿维巴坦具有广谱的抑作用,是新型β-内酰胺酶抑制剂复方制剂,与传统酶抑制剂相比,阿维巴坦可显著抑制肺炎克雷伯菌(KPC)酶活性。
头孢他啶阿维巴坦
头孢他啶/阿维巴坦对革兰阴性菌有较好的抗菌活性,对产ESBL和产KPC酶碳青霉烯类耐药肠杆菌科细菌有效。对多重耐药的其他革兰阴性菌如铜绿假单胞菌、鲍曼不动杆菌有效,对头孢他啶耐药铜绿假单胞菌有一定作用,但碳青霉烯类耐药鲍曼不动杆菌多对其耐药。该药对革兰阳性菌的抗菌活性较差。病原菌对头孢他啶/阿维巴坦的耐药主要由KPC-3的突变引起,KPC-2是中国耐碳青霉烯肺炎克雷伯菌中最常见的碳青霉烯酶,发生耐药的风险可能性低。王明贵教授团队对2019年在中国11家医院收集的605株铜绿假单胞菌进行研究发现,61%对头孢他啶非敏感的菌株,对头孢他啶/阿维巴坦敏感。
头孢他啶/阿维巴坦在中国批准了复杂性腹腔感染、HAP包括呼吸机相关性肺炎(VAP),及有限碳青霉烯耐药的肠杆菌科细菌(CRE)感染,例如在血流感染、尿路感染、皮肤感染、中枢感染的成人患者中治疗革兰阴性菌引起的感染。
Plazomicin为西索米星的衍生物,该药对所有氨基糖苷类钝化酶稳定,但产甲基化酶细菌对其耐药。每日15mg/kg,5天后的Cmax为113mg/L,半衰期为 3 h。2018年6月,美国FDA批准其上市,适应证为复杂性尿路感染。
依拉环素(Eravacvcline)
Eravacvcline为含氟四环素类,结构与替加环素类似,抗菌活性优于替加环素,有口服和静脉制剂。2018年8月,美国FDA批准上市,适应证为复杂性腹腔感染。
奥马环素(Omadacvcline)
Omadacvcline为氨基甲环素( aminomethylcvcline),四环素的衍生物。抗菌谱与替加环素相仿。具有口服及静脉制剂。2018年10月,美国FDA批准其上市,适应证为CAP、皮肤软组织感染。
有无能覆盖所有耐药GNB的新抗菌药?
铁螯合儿茶酚胺侧链头孢菌素可以覆盖所有耐药GNB,但缺陷是容易出现诱导耐药。头孢地尔(Cefiderocol)属于铁螯合儿茶酚头孢菌素,对绝大多数革兰阴性杆菌,包括碳青霉烯类不敏感(MIC>2)肠杆菌科细菌、铜绿假单胞菌、鲍曼不动杆菌、以及麦芽窄食单胞菌均具有抗菌活性(各种菌MIC90均≤1μg/ml)。目前,该药已在日本上市,用于治疗革兰阴性杆菌引起的院内获得性肺炎、血流感染、复杂性尿路感染;2019年11月,美国批准该药用于复杂性尿路感染。
王明贵教授谈到,目前新抗菌药研发利好的一面是国家政策上的扶持,例如美国颁布的抗生素研发激励法案(GAIN)和中国重大新药创制专项支持,都在很大程度上鼓励了新抗菌药的研发;但是同时困境也是存在的,抗菌药上市后的临床应用问题以及目前的国家“集采”政策可能对创新药研发产生一定影响。
目前,与欧美抗耐药菌新药研发现状相比,中国的细菌耐药性更严重,新抗菌药的审批无特殊优先,由于政策扶持相对较差,药企对抗耐药菌新药的研发兴趣较低(表1)。
表1 中国和欧美抗耐药菌新药研发现状比较
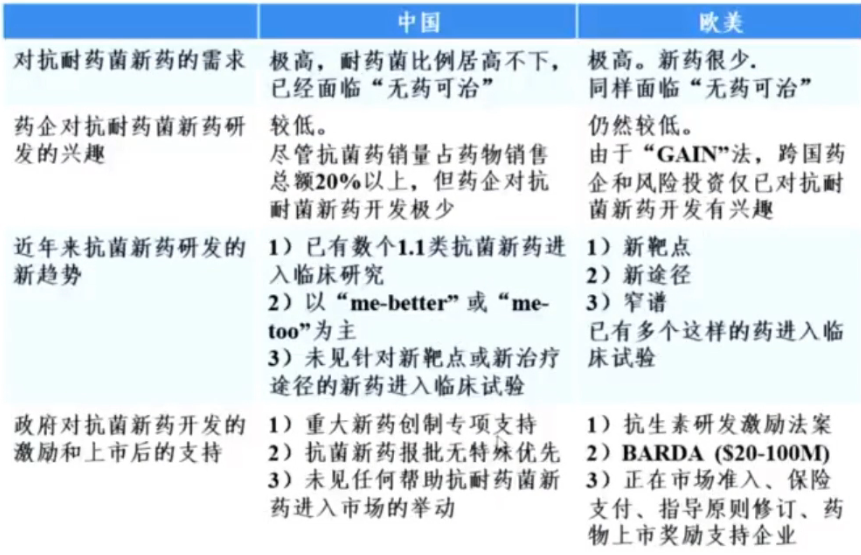
当前,抗菌药研发公司普遍存在新药获批后销售缓慢的困境。2019年,一篇发表于《临床感染病》(Clin Infect Dis)杂志的评论写道,“感染病专家在医学界是很特别的:我们大声呼吁我们实在需要新药,但是当新药真的批准上市,我们总是尽一切努力减少其临床使用。我们恳求每一位内科及外科同行不要使用新抗生素”,说出了当下抗菌药研发的问题所在。
此外,王明贵教授还表示,“集采”是国策,应该坚决拥护,坚定执行,但具体应如何操作,是大刀阔斧还是“摸着石子过河”,这是需要认真思考的。
在报告最后,王明贵教授指出,基于耐药菌治疗的临床需求,在多种政策的引导下,近十年新抗菌药的研发又有趋暖之势,多个对耐药菌有效的新抗菌药物获批上市。但同时也感受到了一丝丝“倒春寒”,王明贵教授呼吁,“新抗菌药的研发,需要大家呵护”,希望刚破土的禾苗,能应对严峻的、但愿是短时的环境变化。
(中国医学论坛报为IDSC官方合作媒体,转载需授权)
查看更多