查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





2026年2月2日,我国自主研发的TROP2 ADC芦康沙妥珠单抗正式获得中国国家药品监督管理局(NMPA)批准上市,用于治疗既往接受过内分泌治疗且在晚期疾病阶段接受过至少一线化疗的不可切除或转移性的激素受体(HR)阳性、人表皮生长因子受体2(HER2)阴性(IHC0、IHC1+或IHC2+/ISH-)乳腺癌成人患者。
芦康沙妥珠单抗的获批,标志着我国在HR+/HER2-乳腺癌后线治疗领域取得了重要突破,为经CDK4/6抑制剂治疗后进展、治疗选择局限的患者,提供了一个兼具创新机制与显著疗效的新选择。值此里程碑时刻,我们特别邀请到OptiTROP-Breast02研究的Leading PI、中国医学科学院肿瘤医院徐兵河教授,系统梳理相关研究的核心数据,深入解读其临床价值与行业影响,展望中国创新药物研发的未来路径。


临床困局
后CDK4/6抑制剂时代亟待破解的治疗瓶颈

HR+/HER2-乳腺癌是乳腺癌中最常见的分子亚型,约占全部病例的70%,其治疗策略的演变直接影响着整体乳腺癌的疾病管理格局。目前,CDK4/6抑制剂联合内分泌治疗已成为该亚型晚期患者的一线标准治疗。然而,肿瘤固有的异质性及后续产生的适应性耐药机制,导致大多数患者最终难免出现疾病进展。进入后线治疗后,有效治疗方案的选择空间显著收窄,临床决策面临严峻挑战。
尽管近年来治疗手段不断丰富,HR+/HER2-晚期乳腺癌患者的生存预后得到一定改善,但CDK4/6抑制剂耐药后的治疗路径仍缺乏标准化共识。对于经CDK4/6抑制剂及内分泌治疗失败的患者,传统化疗虽广泛应用,但客观缓解率普遍偏低,无进展生存期较短,且常伴随明显的骨髓抑制及消化道反应等毒性,总体临床获益有限。
随着精准治疗理念的深入,HR+晚期乳腺癌的后线治疗策略正逐步拓展,涵盖AKT抑制剂、PI3K抑制剂、mTOR抑制剂及新型雌激素受体靶向药物等多种机制。在这一演进过程中,ADC已成为乳腺癌领域最具变革性的治疗突破之一。其中,靶向TROP2的ADC因其在HR+/HER2-亚型中展现出的治疗潜力而备受关注,为破解后CDK4/6抑制剂时代的治疗瓶颈提供了新的重要方向。

中国证据
OptiTROP-Breast02研究的突破性成果

芦康沙妥珠单抗的获批,核心依据源于其关键III期临床研究OptiTROP-Breast02所提供的高级别循证证据。该研究是一项在中国开展的多中心、随机、开放标签III期临床试验,旨在比较芦康沙妥珠单抗与研究者选择的化疗方案在经治的不可切除局部晚期或转移性HR+/HER2-乳腺癌患者中的疗效与安全性。研究聚焦中国人群,纳入高比例内脏转移和多线化疗患者,旨在为中国患者群体提供直接、可靠的疗效与安全性数据。
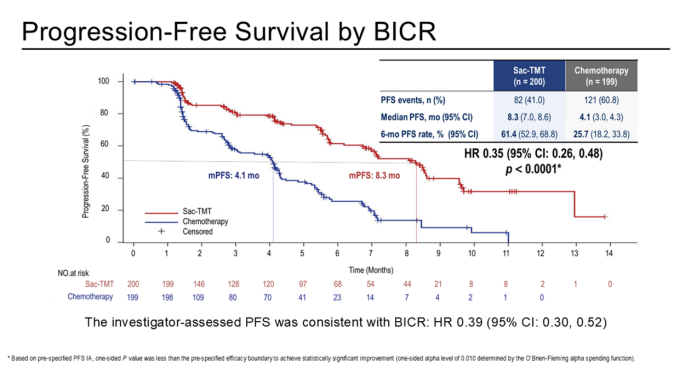
研究结果证实了芦康沙妥珠单抗显著的临床获益。在主要终点方面,芦康沙妥珠单抗显著延长了无进展生存期,中位PFS达到8.3个月,较化疗组的4.1个月实现倍增(HR=0.35),患者的疾病进展或死亡风险降低了65%。亚组分析显示,无论患者HER2表达状态如何,芦康沙妥珠单抗组均观察到一致的PFS获益,提示其疗效在不同HER2表达水平患者中均具有可靠性,降低了由该生物标志物异质性带来的疗效不确定性。在客观缓解率方面,芦康沙妥珠单抗组达到41.5%,显著高于化疗组的24.1%,提示其可诱导更深度的肿瘤退缩。尽管OS数据尚未成熟,但早期分析已显示出令人鼓舞的生存优势(HR=0.33),提示其潜在的长期生存获益。
在安全性方面,芦康沙妥珠单抗整体耐受性良好,安全性特征可控。最常见的治疗相关不良事件为血液学毒性,此类毒性在临床已有成熟的监测与管理流程。此外,芦康沙妥珠单抗中≥3级腹泻发生率仅为1.0%,任何级别的肺炎发生率为1.5%,且均为低级别事件。芦康沙妥珠单抗优化的链接子与载药设计更加稳定,在保证肿瘤细胞杀伤的同时降低了毒性,提升了患者的治疗依从性。

多维价值
从临床实践到研发生态的深远影响

芦康沙妥珠单抗此次适应证的获批,其价值不仅在于为临床增添一种新的治疗选择,更在于从多个维度为HR+/HER2-晚期乳腺癌的诊疗格局与产业创新注入了新的动力,产生深远影响。
在临床实践层面,该药物的获批为CDK4/6抑制剂治疗失败后的关键决策点,提供了一个疗效明确优于传统化疗、且作用机制创新的ADC靶向治疗选择。这有力推动了后线治疗策略从既往“以化疗为主”的被动模式,向“以精准靶向为导向”的主动管理范式演进。对临床医生而言,它提供了强有力的循证武器,使治疗决策更具依据与信心;对患者而言,这意味着在耐药困境中获得了能够显著延长高质量生存时间的新希望,切实体现了“以患者为中心”的诊疗宗旨。
在创新研发与转化领域,芦康沙妥珠单抗的成功标志着从源头创新到临床验证的全链条突破。其基于差异化分子结构的设计理念,为卓越的治疗潜力奠定了科学基础,并迅速转化为高质量的临床证据。其关键III期研究OptiTROP-Breast02的数据在2025年欧洲肿瘤内科学会(ESMO)大会上公布,获得国际学界的高度关注,这亦印证了中国临床研究在方案设计与执行质量上已达到国际先进水准。国家药品监督管理局基于该项高质量本土研究予以批准,充分体现了中国监管机构以临床价值为导向、科学高效回应紧迫医疗需求的审评智慧。
在更宏观的产业与国家战略层面,芦康沙妥珠单抗的成功是“中国创新”深度参与全球医药研发并贡献关键价值的集中展现。从靶点验证、分子优化到关键临床试验的设计与实施,全程彰显了中国本土创新药企在前沿科学探索和复杂临床开发领域的深厚积淀与强大执行力。其所产生的“中国证据”,不仅支持了国内决策,也为全球医学界理解TROP2 ADC在经治人群(尤其是亚洲人群)中的疗效与安全性提供了重要参考。这是落实“健康中国2030”战略,推动高水平科技自立自强,确保重大疾病患者能够同步、甚至更早享受到全球最新科技成果的生动实践,彰显了中国为全球抗癌事业贡献解决方案的能力与担当。

未来展望
拓展疆界的无限可能

立足于此项获批所带来的坚实基础,芦康沙妥珠单抗的治疗疆界与探索维度正持续拓展,展现出更为广阔的应用前景。
目前,其临床研究触角正积极向更前线治疗阶段延伸。在HR+/HER2-乳腺癌领域,研究重点已聚焦于探索该药物在一线治疗中的潜力,旨在为患者提供获益更早、疗效更优的治疗选择。与此同时,该药物与免疫检查点抑制剂的联合策略,也成为前沿探索的重要方向,旨在通过多通路协同,克服耐药瓶颈,进一步提升治疗效果。此外,在新辅助治疗等早期场景中的探索也已展开,致力于将这一高效治疗模式前移,以实现更深度的病理学缓解,从而改善患者的长期生存预后。
芦康沙妥珠单抗在三阴性乳腺癌领域已确立的治疗地位,与其在HR+/HER2-乳腺癌中取得的突破相互呼应,共同印证了TROP2作为乳腺癌关键治疗靶点的广泛价值与平台潜力。这些系统性探索,不仅为该药物在乳腺癌不同亚型及治疗阶段中的应用奠定了坚实基础,也持续推动着精准治疗理念在临床实践中的深化与拓展。
芦康沙妥珠单抗新适应证的获批,是我国乳腺癌精准治疗领域的一项重要突破。这一成果根植于针对中国患者的高级别循证证据,完整体现了从明确临床需求到以严谨科学予以回应的研发逻辑。它不仅为CDK4/6抑制剂治疗失败的患者提供了切实有效的解决方案,也充分展现了中国在新药临床研究领域已达到国际水准。展望未来,随着创新疗法的不断涌现与临床研究的持续深化,中国乳腺癌诊疗水平必将迈向新的高度,最终为更多患者带来长久的生存获益与生活质量的改善!
审核丨中国医学科学院肿瘤医院徐兵河教授
查看更多