查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





非小细胞肺癌(NSCLC)约占所有肺癌的85%[1],对于驱动基因阳性NSCLC,靶向治疗已成为患者治疗的重要选择并显示出临床获益。HER2是NSCLC新兴的驱动基因分子靶点,也是受体酪氨酸激酶的重要成员之一。然而,由于单抗类药物和酪氨酸激酶抑制剂(TKI)对其临床疗效有限,HER2基因异常晚期NSCLC患者目前的治疗药物与驱动基因阴性患者没有显著差异。同时,靶向治疗始终面临获得性耐药的问题,EGFR突变耐药在我国NSCLC患者中并不少见[2]。因此,改善多线治疗后HER2基因异常晚期NSCLC患者的治疗策略已成为亟待解决的问题,ADC药物就是其中一项探索热点。
本期我们将分享一例HER2过表达的T3N2M1 Ⅳ期左肺上叶腺癌伴右肺、纵隔、肝脏、脾脏转移患者的治疗案例。在一系列病情反复和治疗方案调整后,以维迪西妥单抗为基础的后线综合治疗方案有效地遏制了病情的进一步恶化,在EGFR突变耐药后为患者取得了18.5个月的PFS。让我们在重庆医科大学附属第三医院蓝美玲医师的分享及重庆医科大学附属第三医院谢启超副教授的专业点评之中,深入分析和解读患者治疗历程,为HER2过表达NSCLC的治疗带来新的视角和策略。
病例分享
蓝美玲 医师
重庆医科大学附属第三医院 主治医师
研究生毕业于第三军医大学肿瘤学专业
2017-2018年参加“第二届中法放疗医师学习班”学习法语1年
2018-2019前往法国圣埃蒂安Lucien Neuwirth癌症研究中心学习放疗
以第一作者/通讯作者发表SCI论著3篇,中文核心2篇
基本情况
女性,58岁,2021-09-08因“确诊肺腺癌5+年,末次化疗1+月,活动后喘累加重1周”入院。
现病史
患者因“喘累、气促2月余”于2016年1月至外院就诊。2016-01-18外院胸部CT提示:左肺上叶软组织肿块影,大小约3.5 cm×5 cm。双肺散在多发结节影。纵隔多发淋巴结肿大。左侧少量胸腔积液。2016-01-18外院肿瘤标志物检测提示:CEA>30 ng/ml,CA125 134.42 kU/L。2016-01-28行穿刺活检,2016-02-04行基因检测,外院初步诊断:1、左肺上叶腺癌(T3N2M1 IV期 EGFR 21L858R突变);2、右肺继发性恶性肿瘤;3、纵隔淋巴结继发性恶性肿瘤;4、左侧胸腔积液(少量)。遂于外院治疗。
2016年2月至2019年4月期间行1线治疗,用药方案为培美曲塞(800 mg)+顺铂(100 mg),3周期(2016-02-03、2016-02-24、2016-03-17),联用吉非替尼。
治疗期间定期复查影像学显示肿瘤缩小(PR)。2019-04-11影像学复查提示:与2019-02-20影像学检查比较,左肺上叶前段病灶范围稍增大,双肺野结节稍增大;脾脏内结节影(PD)。2019-04-22第2次基因检测(血液)未检测到相关驱动基因突变。1线治疗PFS为39个月。
2019年4月起行2线治疗,用药方案为奥希替尼。
2020-03-24影像学复查提示:与2019-12-12影像学检查比较,左肺上叶前段病灶较前稍增大,双肺结节体积部分增大(SD)。2020-04-02第3次基因检测(血液)提示:EGFR 21L858R突变,突变丰度0.29%。故继续奥希替尼治疗。2020-12-16头颅MRI提示:左侧顶叶异常信号,结合病史,考虑转移性肿瘤;与2019-02-18头颅MRI比较,左侧顶叶病灶为新增,其余病灶变化不大。考虑肿瘤进展(PD)。2线治疗PFS为19个月。
2020年12月起行3线治疗,用药方案为培美曲塞(745 mg)+奈达铂(110 mg),4周期(2020-12-16、2021-01-07、2021-01-30、2021-02-23),联用奥希替尼。
2021-03-16头颅MRI疗效评估为PR。2021年5月胸部CT及头颅MRI复查提示PD:肺内进展、颅内进展。3线治疗PFS为5个月。
2021年6月起行4线治疗,用药方案为贝伐珠单抗(400 mg,q3w),2周期(2021-06-04、2021-06-24)。
2021-09-07胸部CT复查提示:与2021-07-19影像学检查相比,左肺上叶肿块增大,双肺结节部分稍增大。新增肝左外叶及右前叶类圆形低密度影,脾脏病灶较前稍增大(PD)。4线治疗PFS为4个月。
外院治疗总体经过如图1所示,现患者因活动后喘累加重至我院治疗。
图1 外院治疗经过
辅助检查
2021-09-10肝脏增强MRI(图2)提示:肝内及脾脏异常信号,结合病史考虑转移性肿瘤(肝脏最大病灶:2.8 cm×3.0 cm:脾脏:2.4 cm×3.6 cm)
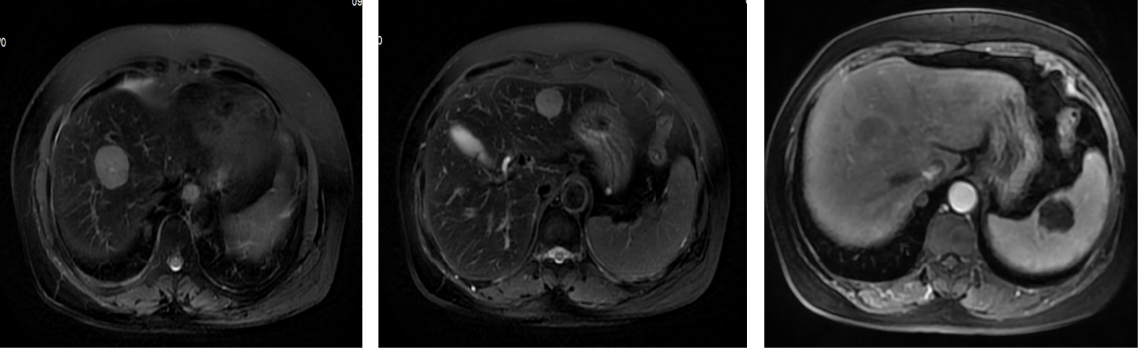
图2 2021-09-10肝脏增强MRI
2021-09-10头颅增强MRI(图3)提示:左顶叶小结节(大小约1.4 cm×1.1 cm×0.9 cm),结合病史考虑转移瘤。
图3 2021-09-10头颅增强MRI
2021-09-14行经皮肺穿刺活检术。病理提示:(左肺)腺癌;免疫组化:CD56(-),Syn局部(+),CgA(-),Ki-67局部热区约20%(+),CK7(+),TTF-1(+),NapsinA局部弱(+),CK5/6(-),P40(-),P63局灶(+)。第四次基因检测(血液+组织)提示(图4):EGFR p.L858R突变,突变频率为56.43%,ERBB2基因扩增,拷贝数变化26.07。

图4 2021-09-09基因检测报告
临床诊断
1、左肺上叶腺癌(T3N2M1 Ⅳ期 EGFR 21L858R突变 ERBB2扩增);2、右肺继发性恶性肿瘤;3、纵隔淋巴结继发性恶性肿瘤;4、肝脏继发性恶性肿瘤;5、脾脏继发性恶性肿瘤。
治疗经过
2021年9月起行5线治疗,用药方案为紫杉醇脂质体(180 mg)+顺铂(90 mg),3周期(2021-09-28、2021-10-23、2021-11-20),联用阿法替尼(30 mg)。
2021-11-24复查头颅增强MRI,疗效评价为SD。分别于2021-12-02至2022-01-12行肝脏局部放疗(PGTV:69Gy/30F),2022-02-11至2022-03-11行全脑放疗(PGTV:50Gy/20F,PTV:40Gy/20F),以对症治疗。2022-04-06复查胸部CT(图5)评估为PD,5线治疗PFS为7个月。
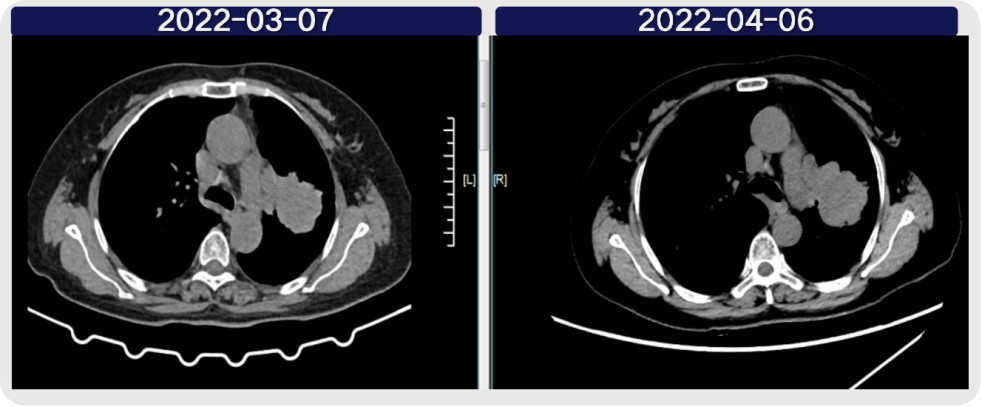
图5 2022-03-07、2022-04-06影像学对比
2022年4月起行6线治疗,用药方案为吡咯替尼。
2022-05-04复查胸部CT,疗效评价为PR,CEA由664.5 ng/ml下降至328.6 ng/ml。2022-07-11复查腹部增强CT(图6)提示肝脏进展,评估为PD,CEA升高至1215 ng/ml。6线治疗PFS为3个月。
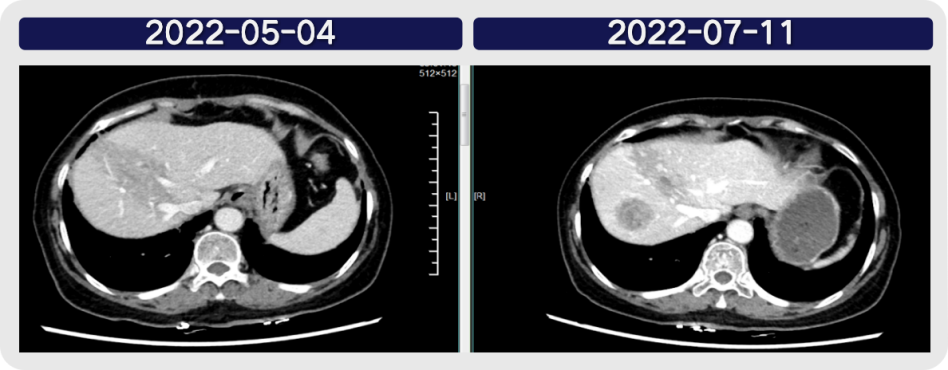
图6 2022-05-04、2022-07-11影像学对比
2022年7月起行7线治疗,用药方案为安罗替尼+特瑞普利单抗。
2022-12-05复查胸部增强CT(图7)提示肺部进展(PD)。2022-12-07行经皮肺穿刺活检术,病理提示(左肺穿刺组织)恶性肿瘤符合腺癌,免疫组化提示HER2(3+)。7线治疗PFS为5个月。
图7 2022-10-17、2022-12-05影像学对比
9线治疗用药方案为维迪西妥单抗(120 mg)+伏美替尼,5周期。8线+9线治疗应用维迪西妥单抗,PFS达18.5个月。
治疗期间定期复查,并多次行局部处理。2024-07-02复查影像学(图8)提示PD。
图8 2024-07-02头颅MRI
2024年7月起行10线综合治疗方案(免疫治疗+化疗+靶向治疗),患者目前接受治疗中。
治疗全流程如图9所示。
图9 治疗全流程
病例点评
谢启超 副教授
肿瘤学博士、主任医师、硕士研究生导师
重庆医科大学附属第三医院肿瘤科主任
中国抗癌协会第二届家族遗传性肿瘤专业委员会委员
中国抗癌协会肿瘤热疗专委会委员
重庆市医药生物技术协会肿瘤精准诊疗专业委员会主任委员
重庆市渝北区医学会副会长
重庆市医学会肿瘤放射治疗专委会副主任委员
重庆市医药生物技术协会肿瘤罕见病疑难病专业委员会副主任委员
重庆市免疫学会代谢免疫专业委员会常务委员
重庆市中西医结合学会肿瘤介入与微创专委会常务委员
重庆抗癌协会肝癌专业委员会委员
主持参与国家自然科学基金、重庆市科委基金、吴阶平基金等项目十余项
以第一或通讯作者在国外发表SCI论文10余篇,最高影响因子12.8分,国内发表学术论文40余篇,获重庆市渝北区“临空人才”称号
HER2作为肿瘤治疗的关键靶点之一,其基因异常形式包括HER2突变、HER2扩增及HER2过表达,在NSCLC患者中的发生率分别为1.6%~3%、2%~4%和7.7%~15.49[3]。虽然HER2基因异常在NSCLC中较为少见,但基于庞大的肺癌患者基数,其临床意义和治疗潜力不容忽视。有研究报道,HER2突变肺癌患者容易出现脑转移,且与不良预后有关[4],但目前尚缺乏针对HER2基因异常NSCLC患者的有效靶向药物。在《中国临床肿瘤学会(CSCO)非小细胞肺癌诊疗指南2024版》中[5],对于Ⅳ期HER2突变NSCLC患者的一线及后线治疗,Ⅰ级推荐均参考Ⅳ期无驱动基因NSCLC患者的治疗方案,即主要为免疫治疗、化疗或两者联合。
然而,由于其本身具有驱动基因改变,传统治疗的疗效不够理想,往往要差于驱动基因阴性的患者。尽管单抗类药物和酪氨酸激酶抑制剂(TKI)等靶向药物在HER2阳性乳腺癌或胃癌患者中表现优异,但HER2阳性NSCLC患者并未从这些传统的抗HER2治疗中显著获益[6]。直到ADC药物的出现,为HER2阳性的NSCLC患者带来了新的希望。维迪西妥单抗作为我国首个提交新药上市申请的自主研发的ADC新药,其连接子可裂解,且拥有具有旁杀伤效应的小分子毒素MMAE,同时偶联的抗体对HER2抗原的亲和力较高,能够有效杀伤靶细胞。在一项真实世界研究中,维迪西妥单抗在治疗HER2基因异常的NSCLC患者上,展现了良好的疗效和安全性[7]。
在这例病例报告中,患者由于肿瘤负荷较大,1线接受了吉非替尼靶向治疗联合化疗的治疗方案。治疗结果显示,患者达到了PR,且PFS达到了39个月,显示出较好的疗效和耐受性。在病情出现进展后,血液标本基因检测未检测到相关驱动基因突变。因患者不愿化疗,查阅文献得知奥希替尼对部分T790M阴性患者亦有抗肿瘤活性[8],转而使用奥希替尼作为2线治疗方案。患者在使用奥希替尼后,病情一度稳定,尽管期间血液样本基因检测未发现耐药突变,但最终PFS停留在19个月。
在此之后,患者经历了一系列化疗、免疫治疗和靶向治疗,由于EGFR突变耐药,后续治疗的PFS并不如1、2线治疗理想。通常,治疗线数越多,找到有效治疗方案的难度也越大。幸运的是,在后续检查时发现患者存在HER2过表达,随后凭借以维迪西妥单抗为基础的治疗方案,在超后线治疗的严峻情况下依旧为患者带来了长达18.5个月的PFS。这提示维迪西妥单抗在NSCLC多线治疗后也可展现出潜在的疗效,为处理相似病例提供了宝贵的治疗参考,有助于指导医生为患者选择更为合适的治疗路径。回顾患者的治疗历程,可以深刻意识到动态基因检测在治疗中的重要作用。尤其在EGFR突变耐药后,患者有必要再做一次基因检测,这有助于患者获得更精准的治疗选择。并且血液检测要结合组织检测,才能得到更准确的结果。有研究报道,HER2基因异常可能在10%的EGFR突变NSCLC中作为耐药机制[9]。因此,在发现HER2基因异常后第一时间使用维迪西妥单抗,或许能为患者带来更长的生存获益。展望未来,期待以维迪西妥单抗为基础的联合治疗方案在HER2基因异常NSCLC中积累更多的临床实践经验和科学数据,为EGFR突变耐药人群提供新的治疗希望,为肺癌治疗领域开拓新的视野。
参考文献:
[1]. Arbour C K ,Riely J G .Systemic Therapy for Locally Advanced and Metastatic Non–Small Cell Lung Cancer: A Review[J].JAMA,2019,322(8):764-774.
[2]. 陈薪如,周彩存.肺癌内科治疗临床研究十年回顾和现状[J].实用肿瘤杂志,2024,39(03):209-218.DOI:10.13267/j.cnki.syzlzz.2024.033.
[3]. 中国抗癌协会肿瘤精准治疗专业委员会,中华医学会杂志社肺癌研究协作组. 驱动基因阳性晚期非小细胞肺癌免疫治疗专家共识(2023版)[J]. 中华肿瘤杂志,2023,45(9):717-740.
[4]. M R ,I S ,P A , et al.Targeting HER2 in non-small-cell lung cancer (NSCLC): a glimpse of hope? An updated review on therapeutic strategies in NSCLC harbouring HER2 alterations.[J].ESMO open,2021,6(5):100260-100260.
[5]. 中国临床肿瘤学会指南工作委员会组织.中国临床肿瘤学会(CSCO)非小细胞肺癌诊疗指南2024[M].北京:人民卫生出版社, 2024.
[6]. J A C ,F J G .Human Epidermal Growth Factor Receptor 2-Mutant Non-Small-Cell Lung Cancer: Continued Progress But Challenges Remain.[J].Journal of clinical oncology : official journal of the American Society of Clinical Oncology,2022,40(7):JCO2102550-JCO2102550.
[7]. M. Z ,L. W ,Q. W , et al.588P First real-world study with HER2 ADC in treating HER2-altered non-small cell lung cancer[J].Annals of Oncology,2023,34(S4):S1700-S1700.
[8]. Eide Z J I ,Helland Å ,Ekman S , et al.Osimertinib in T790M-positive and -negative patients with EGFR -mutated advanced non-small cell lung cancer (the TREM-study)[J].Lung Cancer,2020,143(prepublish):27-35.
[9]. F. N U ,M. C M ,S. C B .HER2 in Non-Small Cell Lung Cancer: A Review of Emerging Therapies[J].Cancers,2022,14(17):4155-4155.
查看更多