查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





作者:徐启桓教授 中山大学附属第三医院
我国是慢性乙型病毒性肝炎发病大国,慢乙肝患者易于进展为肝硬化、肝癌,严重影响着人民的身心健康。但慢乙肝的发病机制迄今为止尚未完全明确。目前的研究认为HBV感染诱导机体免疫应答引起的病理损伤是引起慢性HBV感染肝损伤的主要原因。Interleukin-32(IL-32,白细胞介素32)是一种促炎症细胞因子,研究发现IL-32可以诱导IL-6、TNF-α、IL-8、MIP-2等细胞因子的表达。最新的研究发现HBV及HBV编码的蛋白可诱导肝细胞IL-32表达增高,慢性乙型病毒性肝炎患者外周血中IL-32表达增高,证实HBV感染导致机体外周血中IL-32表达水平发生变化,认为IL-32可能参与了慢性HBV感染者肝组织损伤及病情发展。
针对慢乙肝可能的发病机制,目前公认抗病毒治疗在控制慢乙肝的病情进展中起重要作用。用于抗病毒的药物主要是两类:核苷(酸)类似物(Nucleoside analogues,NA),干扰素(IFN)。因此,本研究通过检测接受不同治疗方案的慢乙肝患者血清中IL-32的水平,探讨药物对IL-32表达的影响,以期为治疗慢性HBV感染提供新的依据和思路。
1 材料与方法
1.1 一般资料 我院接受抗病毒治疗的HBeAg阳性的慢乙肝患者180例,随机分为两组:一组为核苷类似物治疗组(NA),共92例,其中男性70例,女性22例,平均年龄(32±3.8)岁,给予拉米夫定0.1 g+阿德福韦酯10 mg口服,1次/d,疗程48周;另一组为干扰素治疗组(IFN),共88例,其中男性68例,女性12例,平均年龄(30±5.6)岁,给予IFN-α2a皮下注射,180 U/次,1次/周,疗程48周。两组人员在性别、年龄上比较,差异无统计学意义(P>0.05)。慢乙肝诊断标准参照2000年全国病毒性肝炎学术会议修订标准。
1.2 标本收集 于晨起采空腹肘静脉血10 ml于非抗凝干燥无菌真空管中,室温静止60 min自行凝固,再以1500 r/min离心10 min,取上清液装于EP管内,置-80度冰箱保存。分别收集抗病毒治疗前及治疗后12周、24周、48周的外周血标本。
1.3 检测方法 人IL-32 ELISA试剂盒购自美国GBD公司,按照说明书进行操作。
1.4 肝功能的检测 试剂购自美国Beckman公司。用13本Olympus AU2700全自动生化分析仪进行检测。检测指标包括ALT、AST、TBIL等。
1.5 统计学方法 数据分析采用用SPSS 17.0软件。两组间均数比较采用t检验。IL-32水平与ALT、AST、TBIL及HBV DNA间的相关性分析采用Pearson相关性分析。P<0.05认为差异有统计学意义。
2 结果
2.1 两组患者血清生化指标、病毒载量比较 两组患者抗病毒治疗前ALT、AST、TBIL等指标差异无统计学意义,P>0.05)。见表1。

2.2 抗病毒治疗期间ALT复常率、HBeAg转阴率、HBV DNA转阴率 核苷类药物抗病毒治疗24周、48周时的ALT复常率分别是50%、95%,IFN抗病毒治疗24周、48周时的ALT复常率分别是22%、77%,两组之间的差异有统计学意义,核苷类药物组高于干扰素组(P<0.05)。抗病毒治疗48周时两组之间的HBeAg转阴率有差异(IFN组32%,核苷类药物组28%),但差异无统计学意义(P>0.05)。抗病毒治疗48周时两组之问的HBV DNA转阴率有差异,核苷类药物治疗组(67%)高于干扰素治疗组(54%),且两组之问的差异有统计学意义(P<0.05)。
2.3 两组患者血清中IL-32表达水平的比较 两组人员抗病毒治疗前血清中IL-32表达水平差异无统计学意义(P>0.05)。抗病毒治疗后两组患者的血清IL-32均有下降,直到48周时两组间IL-32的下降水平仍差异无统计学意义(P>0.05),但与抗病毒治疗前血清IL-32相比有明显差异(P<0.05)(图1)。
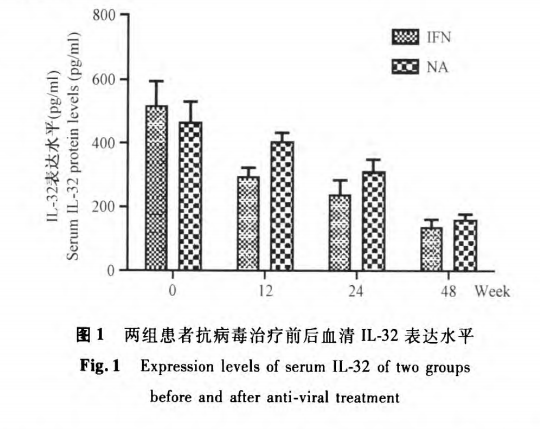
2.4 慢乙肝患者血清中IL-32表达水平与外周血中ALT、AST、TBIL、HBV DNA定量的相关性分析 对所有患者标本的检测结果进行双变量相关性分析,结果显示:血清中IL-32水平与ALT(r=0.48,P=0.033)、AST(r=0.56,P=0.015)、HBV DNA(r=0.45,P=0.045)呈正相关,与TBIL(r=0.078,P=0.372)无显著相关性。
3 讨论
核苷类药物与干扰素属于目前用于抗HBV的两类主要药物,此两类药物的作用机制不同。核苷类药物以HBV DNA聚合酶为靶点,抑制HBV复制。干扰素是通过调节免疫发挥作用,可诱导IL-2、TNF-α等多种细胞因子表达水平的变化而达到抗病毒的目的。Xu等研究证实慢乙肝患者肝组织中IL-32表达增高,且证实干扰素抗病毒治疗48周后肝组织中IL-32水平较抗病毒治疗前明显下降,肝组织炎症减轻。庄桂龙等研究发现乙肝相关性肝衰竭患者血清中IL-32表达增高,与炎症程度相关,认为IL-32可能参与乙肝相关性肝衰竭的发病。本课题研究证实慢乙肝患者外周血中IL-32表达增高,这与许春梅等研究结果一致,进一步证实了IL-32在HBV引起的肝疾病中的作用。
本研究亦发现慢乙肝患者抗病毒治疗后血清IL-32表达逐渐降低,且IL-32表达水平与ALT、AST水平呈正相关。据此我们推测促炎症细胞因子IL-32可能在慢乙肝的发病中起重要的作用。Pan等最近报道HBV及其编码蛋白HBx诱导肝细胞表达IL-32,本研究发现慢乙肝患者抗病毒治疗前IL-32明显增高,抗病毒治疗后IL-32表达水平逐渐下降,可能是HBV复制减少,HBV及其编码的HBx蛋白逐渐降低,诱导IL-32表达的水平下降。此研究结果进一步证实HBV感染后诱导IL-32表达增高,IL-32与慢乙肝发病密切相关。
两组患者抗病毒治疗后血清IL-32表达均有下降,但两组之间的IL-32下降水平并无显著性差异,这可能与HBV可诱导IL-32表达,而抑制病毒复制后,IL-32表达下降有关。邹敏等研究发现使用干扰素的慢乙肝患者血清IL-21表达增高,而使用核苷类药物的慢乙肝患者血清IL-21表达下降,推测可能与干扰素的免疫调节机制有关。接下来,我们将扩大样本,进一步分析使用不同抗病毒药物后IL-32 mRNA的表达变化,以进一步探讨IL-32对机体的调节作用。本研究亦发现核苷类药物组患者ALT复常率、HBV DNA转阴率均高于干扰素组患者,这可能与干扰素使用后可引起部分患者ALT升高及样本量较小、观察疗程有限等因素有关,我们将扩大样本量、延长随访时间等继续观察两类药物在慢乙肝治疗中的利弊。
查看更多