查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





作为肺癌领域的盛会,每年世界肺癌大会(WCLC)都会为全球肺癌医生带来最新、最前沿的肺癌诊疗手段。在万众期待下,第21届世界肺癌大会(WCLC 2020)在2021年1月28—31日拉开帷幕。本报特将精彩口头报告内容分享如下,以飨读者。
本文为Mini oral01中09摘要内容:Glembatumumab Vedotin治疗晚期或转移性肺鳞癌的疗效和安全性。
摘要号:MA01.09
标题:Glembatumumab Vedotin治疗晚期或转移性肺鳞癌的疗效和安全性(PRECG 0504)
背景:
糖蛋白nmb (gp-NMB)是一种在多种癌症中表达的跨膜蛋白,与预后不良有关。大多数鳞状细胞肺癌患者的细胞高表达gp-NMB。Glembatumumab Vedotin是一种靶向gp-NMB的抗体-药物偶联物。
方法:
这项Ⅰ期研究旨在确定表达gp-NMB的肺鳞癌患者对Glembatumumab Vedotin的最大耐受剂量。入选患者的ECOG表现状态为0-1,并且在先前治疗中进展。经脑转移患者符合条件。主要目的是确定格列本单抗韦多汀在该人群中的安全性和耐受性。每个剂量群组计划由3-6例患者组成。
结果:
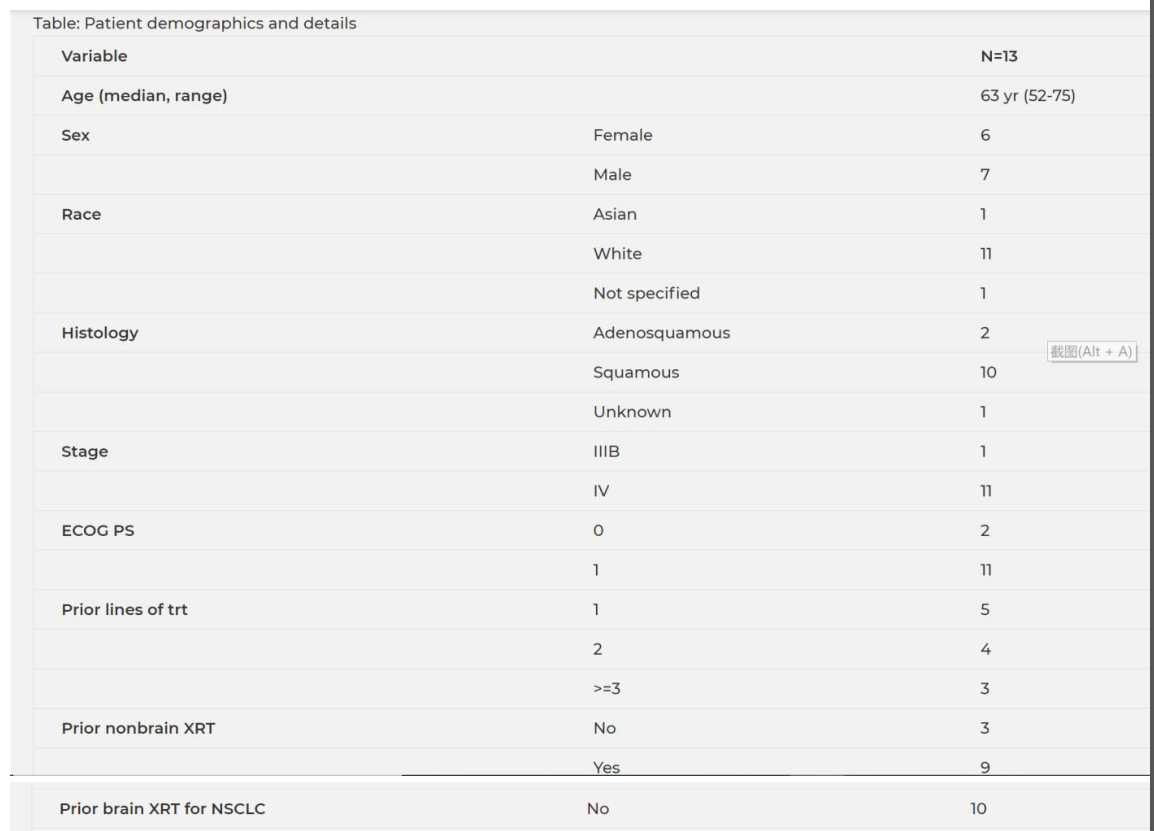
13例患者被纳入(患者详情见表): 9例剂量水平为1,3例剂量水平为-1,然后1例患者再次升级至剂量水平1。接受的治疗周期数的中位数为2(范围1-18)。中位总生存期为5.7个月(95%可信区间:2.2-16.8),中位无进展生存期为3.6个月(95%可信区间:1.6-12.4)。使用RECIST 1.1,在剂量水平为1时,一例患者获得部分缓解,并在17个月后进展。10例患者达到最佳缓解——疾病稳定,8例进展,2例无法评估。在最初的6例患者中,1例因呼吸衰竭(并发癌症进展)DLT导致另外3例患者被纳入剂量水平1。额外的DLT为治疗相关的3级瘙痒导致3例患者在恢复剂量水平1之前被纳入剂量水平-1。15%的患者出现任何级别的不良事件,包括呼吸困难、中性粒细胞减少、呼吸衰竭、贫血、>谷草转氨酶/谷丙转氨酶、腹泻、低磷血症。没有不良事件发生率超过23%,包括食欲下降,疲劳,皮疹,体重减轻。仅有的5级事件是2例呼吸衰竭(一例部分、一例完全归因于癌症进展)。另一例5级事件仅为“疾病进展”。
结论:
Ⅱ期研究的推荐剂量为1.9 mg/kg。在这一经治患者群体中观察到适度的抗癌活性。靶向gp-NMB是可行的,然而这种联合Glembatumumab Vedotin的方案在鳞状细胞肺癌患者中的活性有限。由于公司决定停止该药物的进一步开发,因此未进行研究的第二阶段。
查看更多