查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





人表皮生长因子受体2(HER2)是肿瘤治疗的关键靶点之一,其基因组改变形式包括HER2突变、HER2扩增及HER2过表达。HER2阳性通常与肿瘤的侵袭性、复发转移和预后较差有关,针对HER2的靶向治疗已成为改善患者预后的关键策略之一。维迪西妥单抗作为中国首款自主研发的新型抗体偶联药物(ADC),是HER2阳性肿瘤患者的优选治疗方案之一。
本期,中国医学科学院肿瘤医院山西医院李元教授为我们分享1例HER2(3+)的晚期直肠癌伴肝脏和肺部转移患者,其在一线治疗中采用以维迪西妥单抗为基础的靶向联合治疗后,较好地控制了疾病进展,无进展生存期(PFS)长达5+X个月。让我们跟随山西省肿瘤医院白威教授的点评,深入了解这一病例,以期为类似患者提供更多的治疗启示。
病例分享

李元 教授
中国医学科学院肿瘤医院山西医院消化内科 主治医师
医学博士
山西省抗癌协会大肠癌专业委员会委员
山西省营养学会委员
基本情况
64岁男性患者。2023年6月26日因“排便习惯改变,伴里急后重,大便不成形”就诊。
既往史:2020年行食管癌切除术+右肺上叶楔形切除术;1993年因外伤导致颈椎错位行牵引术。
个人史:有吸烟史,日吸8支,30年;有饮酒史,3两/日,偶尔。
无家族遗传病史
辅助检查
2023-6-26肿瘤标志物:CEA 5.97 ug/L,CA19-9 265.46 U/ml,CA242 104.42 U/ml。
2023-6-26胸腹盆增强CT:食管癌术后改变,右肺上叶及下叶支气管扩张;双肺散在肺大疱;右肺少许炎性改变;直肠壁环形不均匀增厚,恶性可能,结合肠镜;直肠周围系膜内淋巴结增大,考虑转移;肝左外叶轻度强化结节,MT不除外,建议MR检查;肝S2段血管瘤;肝左叶点状不强化影,囊肿可能。
2023-6-26(直肠)活检:中分化腺癌;免疫组化:MLH1(+),PMS2(+),MSH2(+),MSH6(+),Ki-67(约80%+),HER2(3+),Claudin18.2(-)。
2023-6-29肝脏增强MRI:肝左外叶环形强化结节,转移可能;肝S2段血管瘤;肝左外叶散在小囊肿。
临床诊断
1. 直肠癌
cTxN+M1 Ⅳ期,中分化腺癌,肝转移,pMMR,HER2(3+)
2. 食管癌根治术后
诊疗经过
2023-7-6和2023-07-28分别予以XELOX方案治疗2周期。
2023-8-6患者出现腹部胀痛不适,停止排便排气,2023-8-8就诊于我院急诊科,经肛门置管引流协助排气排便后,胀痛缓解。
2023-8-17行盆腔MRI检查:直肠中上段肠壁增厚,符合直肠癌征象,MR分期T4aN2MX,EMVI(+),请结合临床;前列腺增生。
2023-8-18行肝脏MR检查:肝左外叶结节,考虑转移可能,请结合其他检查;肝S2段血管瘤;肝囊肿;双肾囊肿。
2023年8月21日全麻下行“腹腔镜直肠癌根治术+预防性回肠双腔造口术+肝转移灶微波消融术”。
直肠癌切除标本病理提示,中分化腺癌,少许肿瘤退变,间质较多炎性细胞浸润,符合治疗后改变,TRG 3级;溃疡型,肿物大小3*3*2 cm,浸润固有肌层外纤维脂肪组织,未见明确脉管及神经累犯。肿瘤出芽:低级别;肠系膜淋巴结17枚呈反应性增生:另见2枚癌结节。ypTNM 分期:pT3N1cMx。送检上、下切缘:未见癌;环周切缘:未见癌。
直肠癌切除标本基因检测提示,KRAS基因Exon2/3/4未检测出突变、NRAS基因Exon 2/3/4未检出突变、BRAF基因Exon 15未检出突变。UGT1A1*28基因多态性 TA 6/6型。MSI D2S123稳定 MSS。
2023-9-25至2024-01-18予以术后辅助化疗XELOX*5,期间间断复查胸腹部CT及肝脏MRI未发现复发征象。
2024-2-28行“回肠造瘘还纳术”。
2024-03-28复查胸腹部CT检查:原肝左外叶病变旁稍低密度灶增多,考虑转移,必要时集合MRI检查,腹盆腔少量积液,余未见明显变化。
2024-4-2复查肝脏MRI检查:肝转移术后改变,肝左外叶病变较前增大,其周围多发异常信号影,考虑转移;腹盆腔少量积液;门静脉旁淋巴结稍大,余未见明显变化。
2024-4-23于我院行左肝外叶切除术,术后病理示:(肝左外叶)转移性腺癌,结合病史,符合来源于直肠,肿物呈多灶,大者大小7*7*4 cm,小者直径0.3 cm。肝脏断端:未见癌。12a组淋巴结转移性癌1/1。免疫组化:MLH1(+),PMS2(+),MSH2(+),MSH6(+),HER2(3+)。
2024-6-26行PET-CT检查:肝脏S8段结节,考虑转移;双肺上叶及左肺下叶近膈肌多发转移结节。
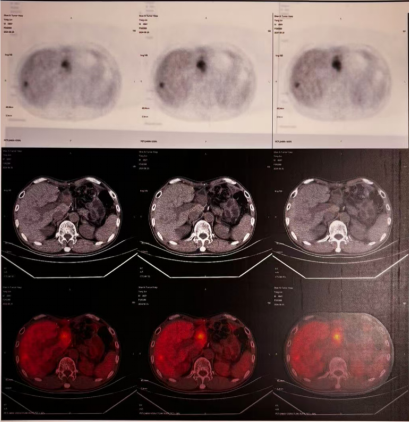
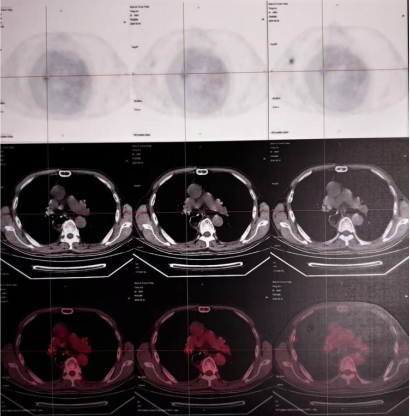
2024-6-28至2024-11-10予以维迪西妥单抗联合呋喹替尼治疗8周期,具体剂量:维迪西妥单抗(120 mg,静滴,每两周重复1次);呋喹替尼(5 mg,口服三周,休息一周)。
2024-8-27疗效评价:复查胸腹部CT提示,食管癌术后改变,直肠癌术后改变,双肺多发结节,较大者位于右肺上叶前段胸膜下,直径约0.5 cm,部分缩小,右肺上叶前段胸膜下结节增大。肝脏形态不规则,左叶部分缺如,术区可见线样致密影,局部见斑片状低密度影,边界不清,未见强化,考虑术后改变,局部包裹性积液,范围较前缩小。肝门部可见环形强化结节影,考虑增大淋巴结影,结合临床。肝S8段血管畸形可能,同前相仿。余未见明显变化。评效SD。
2024-11-28疗效评价:复查胸腹部CT提示,肺部结节大致同前,肝门部稍大淋巴结,短径约0.4 cm,较前缩小,其余同前相仿。评效SD。
靶向药物治疗期间肿瘤标志物变化趋势
诊疗经过一览

白威 教授
山西省肿瘤医院
中国医学科学院肿瘤医院山西医院特聘专家
消化内科主任医师
中国抗癌协会肿瘤营养与支持专业委员会肿瘤营养 化疗学组委员
中国医师协会外科医师分会MDT专业委员会委员
中国抗癌协会肿瘤靶向治疗专业委员会委员
CSCO结直肠癌专家委员会委员
CSCO胃癌专家委员会委员
山西省抗癌协会康复与姑息治疗专委会主任委员
山西省抗癌协会肿瘤营养与支持专业委员会常委
山西省抗癌协会大肠癌专业委员会常委
山西省抗癌协会肝癌专业委员会常委
山西医科大学肿瘤学副教授
本病例为64岁男性,确诊为直肠癌(中分化腺癌,cTxN+M1 Ⅳ期)伴肝转移,免疫组化提示HER2(3+)。历经新辅助治疗、直肠癌扩大根治术、肝转移灶微波消融术、术后辅助化疗后,患者获得了10个月生存期。然而,患者随后出现了肝脏新发转移灶。行左肝外叶切除术,术后病理提示肝转移灶来源于直肠,免疫组化仍提示HER2(3+)。此后不久,PET-CT检查发现双肺多发结节,考虑新发双肺转移,治疗难度进一步加大,迫切需要调整治疗方案。
HER2变异在结直肠癌的发生率较低,总体约5%,但与预后不良有关,可以作为预后评价的潜在生物标志物[1]。研究表明,对于标准治疗失败的HER2阳性结直肠癌患者,抗HER2治疗可使患者显著获益,改善预后[2]。尽早启动抗HER2治疗,包括新辅助/辅助以及一线治疗的应用,或可进一步改善患者的生存获益。
维迪西妥单抗是我国首个原创ADC类药物,可通过特异性结合HER2蛋白,将细胞毒性药物直接递送到肿瘤细胞内,从而提高治疗效果,并减少对正常细胞的损害。维迪西妥单抗于2021年6月9日由NMPA宣布上市,适应证为至少接受过 2 个系统化疗的HER2过表达局部晚期或转移性胃癌(包括胃食管结合部腺癌)的患者和既往接受过含铂化疗且HER2过表达局部晚期或转移性尿路上皮癌的患者。维迪西妥单抗在广泛瘤种中也展现出了较强的抗肿瘤作用,包括肠癌、泌尿、乳腺、阴茎癌、乳房外paget等,相关成果接连在美国临床肿瘤学会(ASCO)、欧洲肿瘤内科学会(ESMO)、欧洲肿瘤内科学会亚洲会议(ESMO-ASIA)重磅会议及《European Urology Oncology》、《European Journal of Cancer》、《Cancer Medicine》等重磅期刊上亮相。
本例患者在一线治疗选择了维迪西妥单抗联合抗血管生成治疗的方案,随访数据显示,患者的肝脏和双肺转移灶稳定,肿瘤标志物(CEA、CA242、CA19-9)快速下降后持续维持在较低水平,整体疗效评价为SD。截至最近的随访期(2024-11-28),患者已获得了5个月PFS,且无严重不良反应发生,安全性好。鉴于当前取得的良好疗效,患者将继续接受后续的治疗疗程,并处于严密的随访监测中。
总的来说,维迪西妥单抗联合治疗显著控制了患者的疾病进展,为难治的合并肝、肺转移的晚期直肠癌患者争取了更长的生存获益。未来,期待随着研究的不断深入和临床实践经验的积累,维迪西妥单抗可为类似患者带来更多获益。
参考文献:
1. Siena S, Sartore-Bianchi A, Marsoni S, et al. Targeting the human epidermal growth factor receptor 2 (HER2) oncogene in colorectal cancer[J]. Ann Oncol, 2018, 29(5): 1108-1119.
2. Laurent-Puig P, Balogoun R, Cayre A, et al. ERBB2 alterations a new prognostic biomarker in stage III colon cancer from a FOLFOX based adjuvant trial (PETACC8)[J]. Ann Oncol, 2016, 27(Suppl. 6): vi151.
查看更多