查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





罗玲, 廖献花, 钟碧慧
中山大学附属第一医院消化内科
代谢相关脂肪性肝病(metabolic associated fatty liver disease, MAFLD),于2020年由非酒精性脂肪性肝病(NAFLD)更名而来[1],这一更名强调了代谢因素在慢性肝病发病机制及诊治过程中的重要性。MAFLD是最常见的慢性肝脏疾病,全球及我国患病率分别高达25%和29%;MAFLD不仅可最终进展为肝硬化、肝癌和肝衰竭,还是心脑血管疾病、肝外恶性肿瘤的危险因素;因此,逐年上升的MAFLD患病率给医疗保健系统带来沉重的负担,但暂无批准上市的有效药物[2-4]。维生素D是一种在人体生理过程中发挥重要作用的多功能维生素,除调节矿物质、骨代谢平衡外,在免疫调节、代谢性疾病、心血管疾病、肿瘤发生和肌肉功能等方面均有重要作用[5-6]。MAFLD患者普遍存在维生素D缺乏(vitamin D deficiency, VDD),提示维生素D水平下降可能与MAFLD的发生发展密切相关[7]。本文将维生素D与MAFLD的最新研究进展进行综述,以期为今后进一步探索奠定理论基础。
1 VDD与MAFLD的关系
随着人们户外活动日趋减少、外出防护增加,全球维生素D不足及缺乏发生率高达50%~80%[8];我国对北京、上海、广州、武汉及重庆五大城市的1436例健康人群的调查结果显示,维生素D缺乏、不足及充足比率依次为57.0%、31.3%和11.7%[9]。维生素D是人体必需的营养素,日渐严重的VDD已成为世界范围内倍受关注的公共健康问题。
目前大部分研究认同VDD与MAFLD密切相关。一方面,维生素D被报道与MAFLD的患病率相关。一项基于美国人口的流行病学调查[10]表明,维生素D水平越低,MAFLD的患病风险越高。另一方面,MAFLD患者维生素D水平也被证实与MAFLD的严重程度相关。来自美国[11]和日本[12]的两个团队分别对病理诊断的190例和229例MAFLD患者进行分析并得出一致结论:维生素D水平越低,肝脏炎症及纤维化程度越严重,非酒精性脂肪性肝炎(NASH)的患病率也越高。另有我国学者[13]在根据超声诊断的MAFLD患者中发现维生素D水平与NAFLD纤维化评分也呈负相关。
然而,部分学者认为MAFLD与维生素D并不完全相关。中国东部的一项研究[14]表示,成年男性维生素不足率低于女性,但在维生素D水平处于最低四分位时,反而男性MAFLD患病率明显增加,女性患病率无明显变化,分析可能维生素D水平下降仅为男性发生MAFLD的独立危险因素,推测与男性睾酮水平等因素有关。而巴西学者[15]对肝活检诊断的139例MAFLD患者进行分析后,认为维生素D水平与MAFLD的严重程度及其合并症均无关,但此研究中女性患者比例高达83%,不排除为性别比例失衡造成的结论偏倚。另外,MAFLD与维生素D的关系可能在中西方人群间也有差异,多数基于西方人群的研究表明MAFLD患者普遍存在VDD,而我国的一项调查[16]结果提示,MAFLD与血清维生素D浓度及状态均无关。维生素D可能只对某些特定基因型或临床表现的MAFLD有影响,而不同种族间维生素D受体(vitamin D receptor, VDR)基因多态性存在差异;亦或是维生素D状态受BMI影响,西方人群超重率明显高于中国人群,可能在调整肥胖等影响因素后VDD与MAFLD无关。
上述关于维生素D和MAFLD之间关系的矛盾观点值得深思,需要进一步分析、讨论两者关系的潜在混杂因素。首先,肝脏本身是合成维生素D的重要器官,慢性肝脏疾病可能因肝功能受损而导致维生素D水平下降。其次,维生素D主要来源于紫外线照射,各项研究可能因来自纬度、气候不同的地区导致结论不一。此外,研究结果也可能受不同遗传因素、生活环境以及个人生活习惯的影响[7]。然而,这些因素在既往研究中并未全面考虑到,今后在开展相关研究时需要在研究设计中尽可能排除更多的混杂因素,以期为临床实践提供更有力的证据。
2 VDD参与MAFLD发生发展的可能机制
MAFLD发病机制仍未完全阐明,目前较为认可的是“多次打击”学说[17],包括胰岛素抵抗(IR)、氧化应激、肠道微生态和环境遗传因素等。近年研究提示VDD或许也是MAFLD发生的“打击”之一,可能通过影响肝脏糖脂代谢、炎症反应、免疫调节以及肠道微生态等环节促进MAFLD形成(图1),但具体机制值得引起研究者关注和深入探讨。
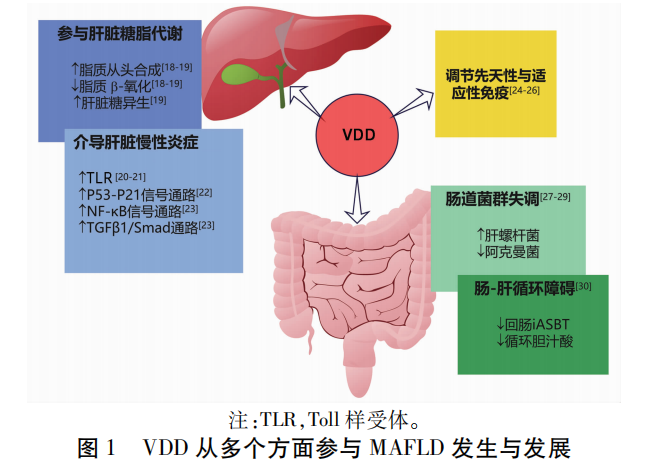
2.1 维生素D影响肝脏糖脂代谢
肝脏脂肪生成增加、分解减少和IR是肝内脂质异常蓄积的直接原因。我国学者[18]以高脂饮食(high fat diet,HFD)建立小鼠脂肪肝模型,并连续8周注射不同浓度的维生素D3,发现维生素D3呈剂量依赖性改善肝脏脂肪变性,同时发现脂肪酸合成酶和乙酰辅酶A羧化酶等促脂肪合成的相关基因表达下调,而与脂质β-氧化相关的肉碱棕榈酰转移酶-1表达增加。另一项用VDD饮食诱导大鼠形成边缘性NASH的研究[19]发现,VDD可以改变胰岛素信号传导和促进游离胆固醇蓄积,从而促使肝脏脂肪变性,但在补充维生素D后,胰岛素信号传导异常出现较大程度逆转,并出现肝脏脂肪合成和糖异生减少。以上研究提示维生素D与肝脏糖脂代谢密切相关,可能通过抑制肝脏脂肪生成和促进脂质β-氧化、调节糖代谢稳态发挥抗MAFLD作用,并且作用强弱与剂量有关。
2.2 维生素D调控肝脏慢性炎症
肝脏持续慢性炎症是MAFLD进展至脂肪性肝炎、肝纤维化的关键因素。有美国学者[20]以低脂饮食(low fat diet,LFD)、低脂伴VDD饮食(LFD+VDD)、高脂高糖的西式饮食(westernized diet,WD)或西式饮食加VDD饮食(WD+VDD)喂养年轻大鼠(鼠龄25 d),10周后发现WD+VDD组小鼠肝脏小叶炎症与NAFLD活动评分(NAS)明显高于WD组小鼠,并伴有肝组织TLR2、TLR4和TLR9以及下游的炎症因子mRNA表达增加。分析表明NAS评分与TLR2、4及9的mRNA水平呈正相关,由此推断当西方饮食的超重儿童出现VDD时,可能会经TLR通路引起MAFLD。糖尿病患者为MAFLD的高发人群,一项中国的研究[21]发现糖尿病大鼠模型补充维生素D后TLR4、核因子κB(NF-κB)和炎症因子的表达下调,肝脏炎症与纤维化程度改善。但在MAFLD形成早期,TLR4通路常处于激活状态,该研究提示维生素D对糖尿病患者的肝脏保护作用。Ma等[22]对MAFLD大鼠的研究发现1,25-(OH)2D3可能通过阻断p53-p21信号通路促进肝细胞衰老,从而减轻肝脏炎症与氧化应激,延缓MAFLD的进展。此外,我国学者[23]发现维生素D3可能作用于NF-κB和TGFβ1/Smad通路,MAFLD小鼠模型补充维生素D3后肝损伤减轻,IKK-β、NF-κB、TGFβ1和Smad3等促进炎症与纤维化的基因下调,而纤维化抑制基因Smad7表达增加。总之,维生素D可能与多个炎症信号通路相关,未来的药物研发可以通过干扰通路的一个或多个环节,为防治或逆转MAFLD进展带来新突破。
2.3 维生素D可能参与免疫调节
MAFLD常伴肝脏免疫紊乱,如巨噬细胞在肝脏大量聚集和细胞因子分泌不平衡,免疫紊乱可促进NASH和肝纤维化的发生,加速病情恶化。有文献[24-25]报道,维生素D可以作为先天性和适应性免疫系统的调节剂。有以色列学者[26]用HFD建立小鼠NASH模型,并连续补充富含维生素D的蘑菇提取物25周,观察发现小鼠体内总脂肪与肝脏脂肪含量下降,转氨酶降低,并伴淋巴细胞CD4+/CD8+比值增加,血浆炎症因子浓度改变,如血浆TNFα、IL-1α和IL-1β浓度下降,TGFβ1水平增加。由此可见,富含维生素D的蘑菇提取物有效成分可能通过调节免疫系统,改善代谢紊乱及肝损伤,但该研究中维生素D可能单独起护肝作用,亦或和蘑菇其他成分起协同作用。因此,未来有待高质量的研究进一步阐明维生素D是否通过免疫调节发挥肝保护作用。
2.4 其他可能机制
MAFLD患者常伴有肠道菌群失调,而胃肠道是VDR主要表达部位,提示维生素D可能对肠道微生态具有调节作用[27-28]。研究[29]表明HFD+VDD饮食较单纯HFD饮食饲养小鼠会促发更严重肠道菌群失调和代谢紊乱:肠道内有害菌肝螺杆菌(Helicobacter hepaticus)增加、益生菌阿克曼菌(Akkermansia muciniphila)减少;补充维生素D可以逆转HFD引起的菌群稳态失衡,并减轻IR与脂肪变程度。VDD也可经肠-肝循环障碍参与MAFLD发生,有中国学者[30]发现在VDD时胆汁酸在肝脏及胆道系统的滞留能力下降,回肠顶端钠依赖性胆汁酸共转运蛋白的表达减少,从而因胆汁酸减少间接促进肝脏脂肪堆积和炎症反应,诱导小鼠单纯性肝脏脂肪变进展为NASH。
3 肝脏VDR在MAFLD形成中的作用
维生素D/VDR轴已被证实与多个靶器官组织(肝脏、胰腺、骨骼肌、脂肪组织等)的代谢相关。维生素D随血流与全身VDR相结合,发挥全身或组织特异性的胰岛素敏化、抗炎、抗纤维化等作用[31]。值得强调的是,在MAFLD患者肝脏不同种类细胞VDR介导的维生素D功能不相同。
通常情况下,肝细胞表面VDR非常少,而肝脏巨噬细胞、肝星状细胞等非实质细胞VDR呈高表达。近年研究表明维生素D3抗炎保肝作用主要通过巨噬细胞VDR介导,有美国的团队[32]对饮食诱导的肥胖小鼠补充卡泊三醇后发现IR和肝脏脂肪变性程度明显改善;但在氯膦酸盐脂质体特异性消融肝脏巨噬细胞后,卡泊三醇的抗MAFLD作用却很大程度上被抵消。然而,肝细胞VDR与MAFLD关系复杂,欧洲学者[33]在小鼠MAFLD模型和脂肪肝患者中观察到MAFLD早期阶段肝细胞VDR表达增加,促进肝脏脂肪累积,但剔除或抑制肝细胞VDR可以防止饮食诱导的肝脏脂肪变。然而,另有研究[34]表明疾病进展至NASH阶段时,细胞和胆管细胞的VDR反而减少,并且在调整BMI、IR、脂联素等混杂因素后VDR数量与肝脏脂肪变性及炎症程度呈负相关。以上结果表明,在不同疾病阶段,肝脏不同部位的VDR介导的作用不同,提示VDR可能成为MAFLD新型药物的靶点。可见,研究清楚肝脏VDR参与MAFLD的发病机制具有重要的临床意义。
4 维生素D治疗MAFLD的临床研究
基于现有流行病学调查、基础实验的证据,维生素D已被提议作为MAFLD的潜在治疗选择[35]。近年陆续有维生素D治疗MAFLD的临床试验报道,但观点不一。最新的一项随机对照试验(RCT)的荟萃分析[36]表明,补充维生素D对MAFLD的血糖、IR具有有益影响,并可以略微降低ALT水平。另有学者[37]利用瞬时弹性成像技术对MAFLD患者进行随访,发现补充低中剂量(1000 IU/d)维生素D可以改善肝脏脂肪变性程度。一项对20例经肝活检证实的NASH患者进行的双盲RCT[38]结果表明,维生素D也可以显著改善肝酶指标。美国学者[39]对42例合并VDD的MAFLD患者(其中26例NASH)补充维生素D3 2000 IU/d,6个月后仅有38.1%患者维生素D水平复常,复常者伴有ALT和IR指数改善,并且大部分复常者为非NASH患者。相反的是,部分研究提示补充维生素D对MAFLD无效。2017年一项包含7项RCT的荟萃分析[40]表明,补充维生素D不能改善MAFLD患者的肝酶、血脂、血糖及BMI。伊朗学者[41]对MAFLD患者补充维生素D 50 000 IU/周,12周后发现与安慰剂组相比,肝酶、血脂方面均无明显改善。总之,目前关于维生素D治疗效果的RCT结论不统一。有学者提出维生素D是一种营养素,它的剂量-效应关系并不会和药物一样是线性,而是S型的,推测治疗效果可能受到基线维生素D水平的影响。此外,随访期时长、维生素D测定方法、个体吸收能力以及试验期间维生素D额外来源,也会影响试验结果[42]。因此,未来需要更严谨的、更长周期的RCT去验证维生素D是否有抗MAFLD作用。
研究者另一个关注的重点是维生素D的补充方式,目前常用剂型维生素D水溶性差、易化学降解、生物利用度具有异质性,对疗效有直接影响,维生素D纳米乳剂、光疗等方式可能成为未来新趋势[43-44]。研究[43]表明,与常规口服维生素D相比较,维生素D纳米乳剂对改善肝功能、减轻肝脏炎症及纤维化的效果更好。另有研究[45]提示早期超负荷补充维生素D 或将取代常规维持剂量补充方式,前者血清维生素D增加幅度更高,并且无药物相关不良事件。
5 总结与展望
受现代亚健康生活方式与高热量饮食结构的影响,VDD和MAFLD的发生率均逐年上升。目前研究表明VDD普遍存在于MAFLD患者,可能通过影响肝脏糖脂代谢、炎症反应、免疫调节以及肠道微生态等多种途径参与MAFLD的发生发展。临床需关注MAFLD患者维生素D水平的管理,应保证足够的日照、均衡的饮食以减少VDD发生,必要时在医生指导下补充维生素D。维生素D亦有望成为MAFLD的治疗药物,但其内在机制、具体补充剂量及疗程仍有待高质量基础实验和大样本、长周期临床试验来进一步验证。
点击链接,免费下载全文
罗玲, 廖献花, 钟碧慧. 维生素D缺乏与代谢相关脂肪性肝病的关系[J]. 临床肝胆病杂志, 2022, 38(7): 1641-1645.
查看更多