查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过






2021年11月12日—14日,第72届美国肝病研究学会年会(AASLD 2021)在线上举行。会议吸引了世界各地的肝病学家和医生参加,一起分享肝病学领域的最新研究进展和先进的治疗方案,并有公共卫生专家就 COVID-19 的焦点话题进行学术交流。《中国医学论坛报》将为大家分享年会的热点内容,敬请关注。
壁报展示15

目前,尚缺乏关于新型冠状病毒(SARS-CoV-2)疫苗在慢性肝病(CLD)患者中的安全性和免疫原性的足够证据。兰州大学第一医院祁小龙教授团队和复旦大学附属华山医院张文宏教授团队牵头,联合中国门脉高压联盟(CHESS)评估了SARS-COV-2疫苗在CLD人群中的安全性和免疫原性,并在本届年会中以壁报形式进行报告。结果显示,SARS-CoV-2疫苗对CLD患者是安全的。CLD患者对SARS-CoV-2疫苗的免疫应答低于健康人群。非肝硬化CLD和代偿期肝硬化患者的免疫原性相似,但失代偿期肝硬化的免疫原性较低。
该前瞻性、多中心、开放标签临床研究的参与者为年龄超过18岁的确诊CLD患者和健康志愿者。所有参与者都接受了SARS-CoV-2疫苗的全程接种。记录每次接种SARS-CoV-2疫苗后14天内的不良反应,全程接种疫苗后收集实验室检测结果,并在最后一次接种后14天内收集受试者的血清样本并检测SARS-CoV-2中和抗体。
这项研究共纳入中国的15个地区登记的640名参与者(496例CLD患者和144名健康志愿者)。最常见的不良反应是轻微短暂的注射部位疼痛[39(7.9%)]。3名受试者在整个SARS-CoV-2疫苗接种计划后出现3级氨基转移酶升高(定义为丙氨酸氨基转移酶>5 ULN),其中一人被判定为可能是SARS-CoV-2疫苗接种相关的严重不良反应。
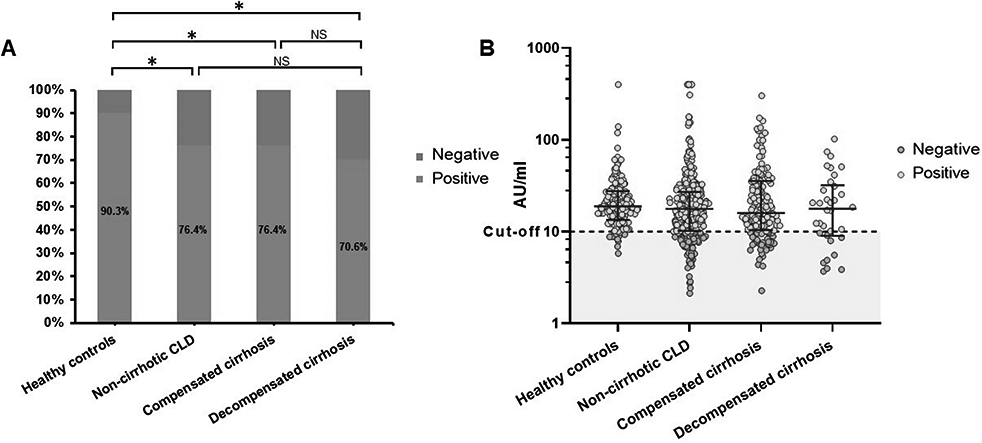
非肝硬化CLD组的SARS-CoV-2中和抗体阳性率为76.4%,代偿性肝硬化组的中和抗体阳性率为76.4%,失代偿性肝硬化组的中和抗体阳性率为70.6%(P=0.745),健康对照组的中和抗体阳性率为90.3%(P=0.002)(图1A)。经年龄和性别调整后,差异仍无统计学意义(P=0.603)。非肝硬化CLD组中和抗体浓度为17.68 AU/ml(10.17 AU/ml~27.01 AU/ml),代偿期肝硬化组中和抗体浓度为15.94 AU/ml(10.37 AU/ml~35.63 AU/ml),失代偿期肝硬化组中和抗体浓度为17.79 AU/ml(8.98 AU/ml~32.07 AU/ml),对照组中和抗体浓度为18.83 AU/ml(13.42 AU/ml~27.66 AU/ml)(P=0.151)(图1B)。
中国医学论坛报 佟艳华 编译
查看更多