查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





3月31日,国家药品监督管理局药品评审中心(CDE)正式受理永泰生物-B(06978.HK)核心产品扩增活化的淋巴细胞(EAL®,拟定通用名:爱可仑赛注射液)的附条件上市许可申请,受理号为CXSS2500039。
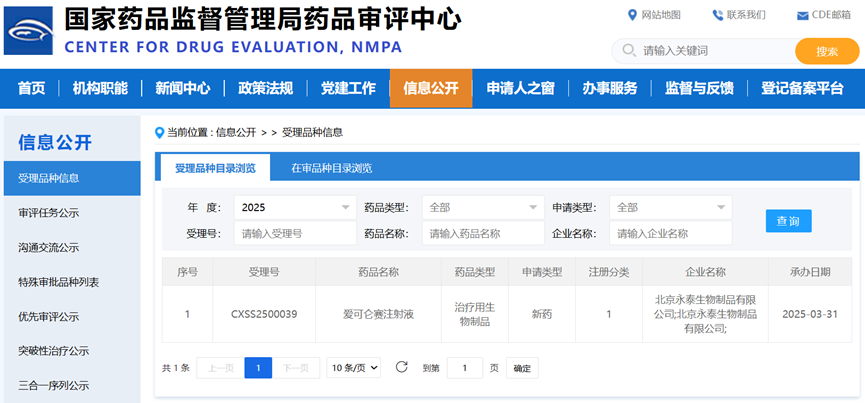
图:受理品种目录(CDE网站截图)
这意味着中国首款针对实体瘤的细胞因子诱导杀伤细胞(CIK)疗法进入上市审批阶段,更标志着实体瘤自体免疫细胞治疗药品从实验室走向临床应用的重大跨越。
目前,全球范围内已上市的细胞治疗产品(如CAR-T类等)主要针对血液瘤领域,在实体肿瘤治疗的战场上,我们仍然面临挑战。据网络数据显示,截至2025年3月,全球已获批上市的针对实体瘤治疗的免疫细胞药品只有9款,而中国在此领域尚未有获批上市药品。
爱可仑赛注射液未来如获批上市,将在中国实体瘤治疗的免疫细胞药品领域实现零的突破,不仅填补了国内实体瘤细胞药物空白,延长肿瘤患者无复发生存期,更为肝癌等高风险复发癌种术后防止复发提供了全新的思路和临床解决方案。
爱可仑赛注射液适应证为高复发风险原发性肝细胞癌外科根治术后预防复发。该产品拥有诸多核心优势,主要包括以下几点:
一、来源于自体的非基因修饰产品,安全性高
爱可仑赛注射液属于个性化自体细胞治疗产品,系由供者自体外周血为原材料,经分离、活化、扩增培养制备而成。主要活性成分为CD3+CD8+杀伤性T细胞,同时包含NK细胞、辅助T细胞等免疫细胞亚群,形成广谱抗肿瘤效应。
与CAR-T类等基因改造疗法不同,爱可仑赛注射液为非基因修饰技术,无需病毒载体转导,避免了基因插入突变风险,长期安全性更受到临床认可。
二、具有广谱抗肿瘤特性,显著降低肿瘤复发风险
直接杀伤:通过释放穿孔素、颗粒酶等物质穿透肿瘤细胞膜,诱导细胞凋亡;
细胞因子:分泌IFN-γ、TNF-α等促炎因子改变肿瘤微环境,抑制免疫逃逸;
免疫记忆长期监控:回输后有可能形成记忆性T细胞,可长期控制肿瘤复发。
三、创新性强、临床需求迫切,市场潜力大
目前,在原发性肝细胞癌术后动脉化疗栓塞术治疗的基础上,CIK细胞已纳入原发性肝癌临床治疗指南。然而,由于尚未有上市产品,临床上缺少可使用产品。爱可仑赛注射液产品创新性强、临床需求急迫,于2023年9月纳入CDE突破性治疗品种名单,并在2025年3月13日,纳入CDE优先审评品种名单。

图:优先审评品种名单(CDE网站截图)
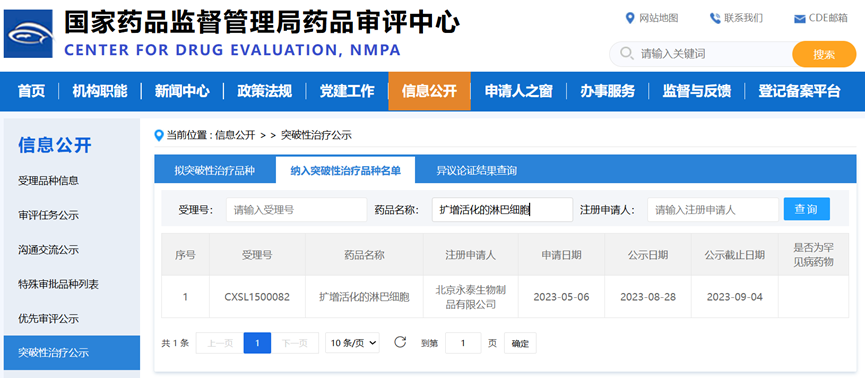
图:突破性治疗品种名单(CDE网站截图)
我国每年新发肝癌占全球约50%,新发病例近40万,五年生存率仅14%,全国肝癌患者约100万人。爱可仑赛注射液II期临床试验显示其显著降低复发风险,爱可仑赛注射液上市后,将打破肝癌术后无药可用的现状,填补我国实体瘤领域免疫细胞治疗空白。同时,依托永泰生物已在京落成的数字化免疫细胞药品生产中心,将快速实现商业化。
此前,爱可仑赛注射液已经作为三类医疗技术在临床上治疗了4000多例癌症患者,累计回输超过20000次,适应证涵盖肝癌、肺癌、胃癌、白血病等多种实体瘤和血液瘤,潜在市场潜力巨大。
四、临床研究团队专业实力领先
爱可仑赛注射液的II期临床研究由国内顶尖的医学临床专家团队负责试验设计和实施。由中国人民解放军总医院作为牵头单位,中国医学科学院肿瘤医院、北京协和医院、北京大学人民医院、首都医科大学佑安医院、郑州大学第一医院等全国多家临床中心参与,为本试验科学严谨高效开展提供了有力保障。
五、创新开拓个性化自体免疫细胞产品规模化生产实践范例
永泰生物拥有涵盖细胞药物临床前研究、临床试验研究、数字化CMC的全流程体系。近20年来,永泰生物打造了免疫细胞药物研发的关键技术平台,包括新靶点新结构的发现平台、无血清细胞培养及扩增技术平台、基因修饰技术平台、抗原特异性T细胞体外扩增技术平台、基因载体生产技术平台、个体化细胞产品自动化生产平台;打造了药品全周期研发管理体系,包括药品注册申报流程平台;细胞药品临床试验组织及管理平台;细胞药品的物流运输管理平台;细胞药品的GMP生产质量管理平台;个体化细胞药品生产和质量管理的数字化管理平台。
通过上述自主可控的技术力量和管理平台的建立及完善,永泰生物实现了免疫细胞药品从靶点和结构发现、临床前研究、临床研究、药品上市到最终GMP标准化生产和商业化的全链条、多环节精准高效衔接,并形成从研发到生产快速转换可复制的标准路径,保证公司可持续发展。同时,这些平台的应用将逐步解决CGT领域产学研转化困难、进口依赖性大、自动化程度低、标准化不足、产业规模小、生产成本高等制约行业发展的难题,加快提高行业发展水平。
本次爱可仑赛注射液上市申请的正式受理,标志着我国在针对实体瘤治疗的免疫细胞药品领域有望尽快实现产品获批零的突破,产品上市后可惠及更多肝癌患者,为他们带来更多治愈的可能与希望。展望未来,永泰生物始终秉承“让生命在我们手中延续”的企业使命,继续深耕免疫细胞药品领域,为推动健康中国行动贡献力量!
查看更多
暂无留言