查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





特发性低促性腺激素性性腺功能减退症(idiopathic hypogonadotropic hypogonadism,IHH),是由GnRH合成、分泌和作用障碍引起的疾病,表现为不孕不育,青春期不发育或部分发育。该疾病具有显著的遗传、临床异质性。根据有无嗅觉异常分为卡尔曼综合征(Kallmann syndrome,KS)和嗅觉正常的低促性腺激素性性腺功能减退症(normosmic idiopathic hypogonadotropic hypogonadism,nIHH)。
国外数据显示,IHH总体发病率为1/100000~10/100000;女性较男性低。
目前已明确20余种基因突变可导致IHH,如KAL1、FGFR1、FGF8、GnRH、GNRHR、PROK2、PROKR2、TAC3、TACR3、DAX1、NELF、CHD7、SEMA3A、SOX2、FEZF1等。对有家族史的患者,详细分析其遗传方式,可提示某些基因突变。例如,KAL1突变以X染色体隐性遗传为主,而FGFR1和PROKR2突变以常染色体显性遗传为主。若对患者进行以上基因筛查,约1/3患者可找到突变基因。近年来,每年发现1~2种IHH新致病基因。虽有研究提示FGFR1突变患者可合并骨骼畸形和牙齿发育异常,PROKR2突变患者常伴随超重或肥胖,KAL1和FGFR1突变患者易出现隐睾,但基因突变和临床特点之间并非简单的对应关系。
1.第二性征不发育和配子生成障碍 男性表现为童声、小阴茎、无阴毛生长、小睾丸或隐睾、无精子生成;女性表现为乳腺不发育、幼稚外阴和原发闭经。
2.骨骺闭合延迟 上部量/下部量<1,指尖距>身高,易患骨质疏松症。
3.嗅觉障碍 因嗅球和嗅束发育异常,40%~60%IHH患者合并嗅觉丧失,不能识别气味。
4.其他表现 面中线缺陷,如唇腭裂;孤立肾;短指(趾)、并指(趾);骨骼畸形或牙齿发育不良;超重和肥胖;镜像运动等。
1.一般检查 肝肾功能、血尿常规,以除外慢性系统性疾病或营养不良导致青春发育延迟。
2.性激素 FSH,LH,睾酮,雌二醇,孕酮(女性);重视基础状态LH水平:LH在0~0.7 IU/L,提示IHH;LH≥0.7 IU/L,提示青春发育延迟或部分性IHH。
3.其他相关激素 GH/IGF-1,PRL,ACTH/皮质醇(早上8点)/24h尿游离皮质醇,FT4/TSH,AMH、inhibin B。
4.影像学检查 脑部MR,以除外各种垂体和下丘脑病变,评估嗅球、嗅束、视神经、内耳发育情况;骨密度、双肾超声和骨龄。
骨龄是衡量生长发育的重要标尺,对疾病鉴别诊断有重要价值。骨龄测定有多种方法,目前常用G-P图谱法:根据手掌和腕关节的骨骼形态来评定年龄,必要时加拍肘、踝、足跟和髂骨翼的X线片,用来帮助判断骨龄。正常男性骨龄达到12岁时,青春发育自然启动。IHH患者或暂时性青春发育延迟者,骨龄一般落后生物学年龄2~3年。暂时性青春发育延迟者,骨龄达到12岁时就会开始青春发育;如骨龄>12岁甚至骨骺闭合时仍无青春发育迹象,且LH、FSH和睾酮水平低下,可确诊IHH而非暂时性青春发育延迟。
5.戈那瑞林兴奋试验 静脉注射戈那瑞林100 μg,测定0和60分钟LH水平:在男性,LH60分钟≥8 IU/L,提示下丘脑-垂体-性腺轴启动或青春发育延迟;或曲普瑞林兴奋试验:肌内注射曲普瑞林100 μg,测定0和60分钟LH水平。对男性,LH60分钟≥12IU/L提示下丘脑-垂体-性腺轴完全启动或青春发育延迟;LH60分钟≤4 IU/L提示性腺轴未启动,可诊断IHH。LH60分钟在4~12 IU/L,提示性腺轴功能部分受损,需随访其变化;对女性,LH60分钟≥18 IU/L,提示性腺轴功能完全启动;LH60分钟≤6 IU/L提示性腺轴未启动,可诊断IHH;LH60分钟在6~18 IU/L,提示性腺轴功能部分受损。
6.HCG兴奋试验(可选) 用来评价睾丸间质细胞(Leydig细胞)功能,主要有两种方法。单次肌内注射HCG 2000~5000 IU,测定0、24、48和72小时血睾酮水平。或肌内注射HCG 2000 IU,每周2次,连续2周,测定第0天,第4天,第7天,第10天和第14天睾酮水平。睾酮≥100 ng/dl提示存在睾丸间质细胞,睾酮≥300 ng/dl提示间质细胞功能良好。该试验可能存在假阴性,应慎重评估试验结果,必要时重复试验或试验性促性腺激素治疗3个月,观察睾酮水平变化。
7.嗅觉测试 若不能鉴别酒精、白醋、水和香波的气味,可拟诊卡尔曼综合征。
8.基因诊断 染色体核型分析、微阵列分析评估是否有染色体数量及大片段异常,检测是否存在微缺失及微重复以排除连续基因综合征。
男性骨龄>12岁或生物年龄>14岁尚无第二性征出现和睾丸体积增大,睾酮水平低(≤100 ng/dl)且促性腺激素(FSH和LH)水平低或“正常”。女性到14岁尚无第二性征发育和月经来潮,雌二醇水平低且促性腺激素水平(FSH和LH)低或“正常”。且找不到明确病因者,拟诊断本病。
因青春发育是一个连续变化的动态过程,因此IHH的诊断需综合考虑年龄、第二性征、性腺体积、激素水平和骨龄等诸多因素。14岁尚无青春发育的男性,应进行青春发育相关检查,对暂时难以确诊者,应随访观察,以明确最终诊断。
1.多种垂体前叶激素分泌障碍 除下丘脑-垂体-性腺轴功能受损外,同时存在一种或多种其他垂体前叶激素分泌缺陷。因此需筛查PRL、GH-IGF-1轴、TSH-FT4轴、ACTH-F轴功能。垂体前叶发育不良、垂体柄中断综合征、垂体和下丘脑肿瘤以及其他鞍区病变,均可致垂体前叶多种激素分泌不足。
2.体质性青春发育延迟 又称为“暂时性青春发育延迟”。绝大多数男孩在14岁之前出现青春发育表现。有少数男孩,青春发育时间会延迟到14~18岁,甚至更晚。虽然青春发育较晚,但他们成年后身高、性腺轴功能和骨密度均正常。体质性青春发育延迟可能和体型偏瘦或青春发育延迟家族史有关。如患者在骨龄达到12岁时,戈那瑞林兴奋试验中LH 60分钟≥8 IU/L,或曲普瑞林兴奋试验中LH60min≥12 IU/L,提示体质性青春发育延迟的诊断。随访观察或小剂量睾酮补充,均为可选治疗方案。女性体质性青春发育延迟少见。
3.营养状态对青春发育的影响 过度节食、长期腹泻等病因造成营养不良,会引起两性青春发育延迟或低促性腺激素性性腺功能减退症。神经性厌食是女性闭经常见原因。肥胖可致男性隐匿性阴茎和睾酮水平降低,易被误诊为IHH。在肥胖患者,睾酮水平随着体重增加而降低,他们的促性腺激素水平和睾丸体积一般接近正常。饮食控制或胃肠道手术减轻体重后,睾酮水平可明显提高。
4.慢性系统性疾病对青春发育影响 哮喘、肾病综合征、严重甲状腺功能减退症、肝硬化、炎症性肠病、地中海贫血、组织细胞增多症等,可致青春发育延迟。
5.合并有性腺轴功能减退的各种遗传性疾病或综合征 常见的有普拉德-威利综合征,表现为极度肥胖和IHH;DAX-1基因突变,表现为先天性肾上腺发育不全和IHH;劳-穆-比综合征(Laurence-Moon-Biedl综合征),表现为极度肥胖、糖尿病和IHH;
1.对于男性患者,治疗方案主要有3种,包括睾酮替代、促性腺激素生精治疗和脉冲式GnRH生精治疗。雄激素替代治疗可促进男性化,使患者能够完成正常性生活和射精,但不能产生精子;促性腺激素治疗可促进睾丸产生睾酮和精子;脉冲式GnRH治疗通过促进垂体分泌促性腺激素而促进睾丸发育。
(1)睾酮替代治疗:睾酮替代治疗可促进男性化表现。初始口服十一酸睾酮胶丸40 mg,一日1~3次,或十一酸睾酮注射剂125mg,肌内注射,每个月1次。6个月后增加到成人剂量:十一酸睾酮胶丸,80 mg,一日2~3次或十一酸睾酮注射剂,250 mg,肌内注射,每个月1次。
(2)HCG/HMG联合生精治疗:肌内注射HCG 2000~3000 IU,每周2次,共3个月,期间调整HCG剂量,尽量使血睾酮维持在300~500 ng/dl;然后添加肌内注射HMG 75~150 IU,每周2~3次,联合HCG进行生精治疗。为提高依从性,可把HCG和HMG混溶于生理盐水(或注射用水)中肌内注射,每周2次。间隔2~3个月随访1次,需监测血睾酮和β-HCG水平、睾丸体积和精液常规;70%~85%患者在联合用药0.5~2年内产生精子。
(3)脉冲式GnRH生精治疗:戈那瑞林10 μg/90 min。带泵3天后,如血LH≥1 IU/L,提示初步治疗有效。如LH无升高,提示垂体前叶促性腺激素细胞缺乏或功能严重受损,治疗预后不佳。此后,每个月随访1次,监测FSH、LH、睾酮和精液常规,调整戈那瑞林的剂量和频率,尽可能将睾酮维持在正常中值水平,稳定后可3个月随访1次,依据患者的具体情况调整药物剂量。治疗3个月后就可能有精子生成。
(4)对女性IHH患者的治疗:无生育需求时,予周期性雌孕激素联合替代治疗,促进第二性征发育。有生育需求时,可行促性腺激素促排卵治疗或脉冲式GnRH治疗。
1)雌孕激素替代治疗:尽量模拟正常青春发育过程补充性激素。参考方案:起始小剂量雌激素(戊酸雌二醇0.5~1 mg,qd)6~12个月;然后增加雌二醇剂量(戊酸雌二醇2 mg,qd)6~12个月;如乳腺发育和子宫大小(B超)接近或达到成年女性水平,随后可行周期性雌孕激素联合治疗(戊酸雌二醇2 mg,qd×11天,戊酸雌二醇2 mg+醋酸环丙孕酮1 mg×10天,停药期间可有撤退性阴道出血);治疗的前2年,间隔2~3个月随访1次,观察乳腺和子宫大小变化。此后,应6~12个月随访1次。
2)促排卵治疗:脉冲式GnRH治疗,可诱导规律月经和排卵,获得妊娠机会。戈那瑞林10 μg/90 min;间隔2~3个月随访1次,监测促性腺激素、雌二醇、孕酮、子宫体积、卵巢体积和卵泡数目;警惕卵巢过度刺激和卵泡破裂风险。另外,可以在辅助生育专科医生指导下,行促性腺激素促排卵治疗,获卵子率近100%。
诊疗流程(图 53-1)
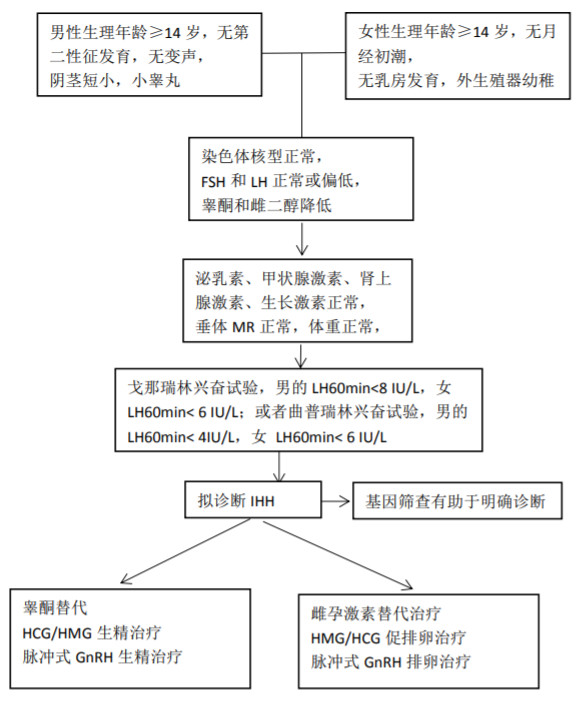
图 53-1 特发性低促性腺激素性性腺功能减退症诊疗流程
参考文献(略)
来源:国家卫健委《罕见病诊疗指南(2019年版)》
查看更多