查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





2月2日, CheckMate 743研究最新随访数据公布于《肿瘤学年鉴》(Annals of Oncology)杂志,其结果支持纳武利尤单抗联合伊匹木单抗作为不可切除恶性胸膜间皮瘤(MPM)的标准治疗方案。现将研究整理如下。
在Ⅲ期CheckMate 743研究(NCT02899299)结果显示,与化疗相比,一线纳武利尤单抗联合伊匹木单抗治疗显著提高了不可切除的恶性胸膜间皮瘤患者的总生存(OS)期。本次报告的是至少3年随访的最新数据。
研究纳入既往未经治疗、经组织学证实、不可切除且东部肿瘤合作组的表现状态为≤1的恶性胸膜间皮瘤成年患者,以1∶1的比例随机分配接受纳武利尤单抗(3 mg/kg,每2周一次)联合伊匹木单抗(1 mg/kg,每6周一次)治疗2年,或6个周期的铂类联合培美曲塞化疗。
该报告包括最新的疗效和安全性结果、探索性生物标志物分析(包括4-基因炎症表达特征评分)以及对因治疗相关不良事件(TRAEs)而停止治疗的患者进行的事后疗效分析。
研究共纳入605例患者,截至2021年5月7日,中位随访时间为43.1个月。与化疗相比,纳武利尤单抗联合伊匹木单抗继续延长OS期(图1)。中位OS期分别为纳武利尤单抗联合伊匹木单抗组18.1个月和铂类联合培美曲塞组14.1个月[HR (95%CI)为0.73(0.61~0.87)],3年OS率分别为23%和15%。
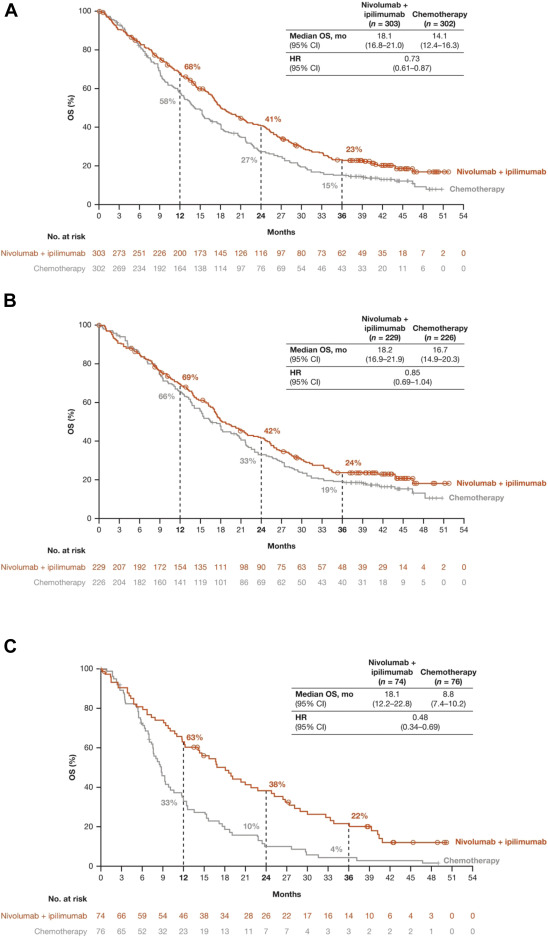
图1 所有患者(A)、组织学为上皮样的患者(B)和非上皮样的患者(C)的OS期结果
3年无进展生存(PFS)率分别为14%和1%;客观缓解率(ORR)分别为40%和44%;在缓解者中,3年缓解持续时间(DOR)率为28%和0%(图2)。在亚组(包括组织学)中观察到,与化疗相比,纳武利尤单抗联合伊匹木单抗提高了生存获益。4-基因炎症标志物的高分似乎与纳武利尤单抗联合伊匹木单抗改善生存获益相关。
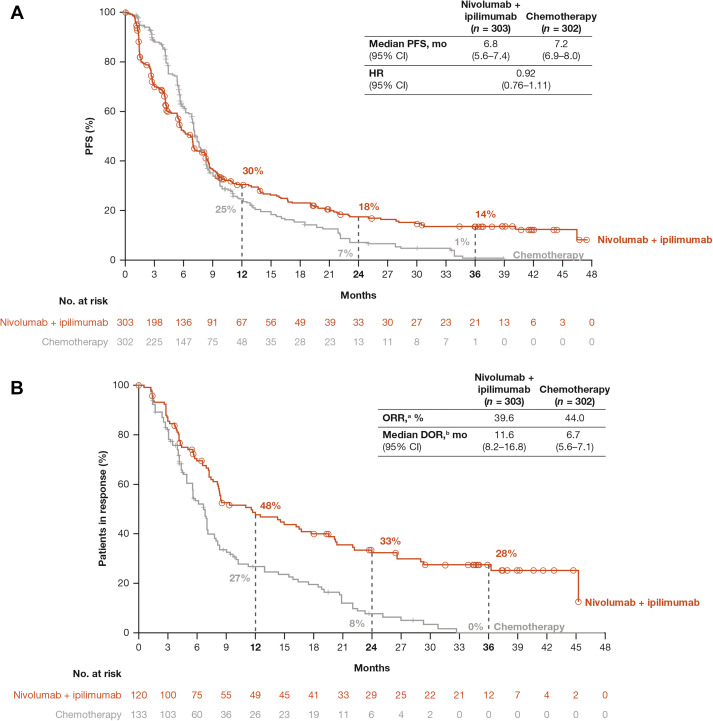
图2 所有患者的PFS期、ORR和DOR结果
尽管患者已停止治疗一年,但纳武利尤单抗联合伊匹木单抗组未观察到新的安全信号。在因TRAEs而停用纳武利尤单抗联合伊匹木单抗的患者中,中位OS期为25.4个月,34%的缓解者在停药后缓解持续时间≥3年。
在至少3年的随访时间内,纳武利尤单抗联合伊匹木单抗继续提供比化疗更长期的生存获益和可控的安全性,研究结果支持该方案作为不可切除恶性胸膜间皮瘤的标准治疗方案,无论其组织学分类如何。
中国医学论坛报 刘佳玲编译
往期回顾
● 前沿快讯丨CheckMate 9ER试验的患者报告结局结果公布,纳武利尤单抗联合卡博替尼更有优势
● 前沿快讯丨ATTRACTION-4研究数据公布于Lancet Oncology,为胃或胃食管结合部癌患者带来治疗新希望

查看更多