查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





2019年6月18日~22日,第15届国际淋巴瘤大会(ICML)在风光旖旎的瑞士·卢加诺(Lugano)隆重举行。目前ICML已成为全球淋巴瘤领域最具影响力的盛会,数千名来自世界各地的淋巴瘤领域专家参加了这次学术盛会。泽布替尼(zanubrutinib)是一种具有高选择性的不可逆BTK抑制剂,既往研究已证实可有效抑制BTK,对其他激酶的脱靶抑制作用很小。本次ICML期间,来自北京大学肿瘤医院的宋玉琴教授报告了泽布替尼治疗复发/难治套细胞淋巴瘤(R/R MCL)研究的更新结果(Oral:015)。
【肿瘤资讯】特邀北京大学肿瘤医院的朱军教授对该研究进行了点评,详情如下。

朱军主任医师,教授,博士生导师
北京大学肿瘤医院党委书记、大内科主任、淋巴瘤科主任
中国临床肿瘤学会(CSCO)常务理事
中国抗淋巴瘤联盟主任委员
CSCO抗淋巴瘤联盟主任委员
中国抗癌协会肿瘤靶向治疗专业委员会副主任委员
中国老年学学会老年肿瘤专业委员会常委
朱军教授现场点评
BTK抑制剂泽布替尼治疗MCL中疗效安全性均优
朱军教授:我特别高兴再次来到Lugano参加第15届ICML大会,从开始参会到现在,我能感受到中国的声音越来越多。今天的开幕式很受鼓舞,大会主席指出中国无论是投稿数量还是参会人数都很多,并且有很多中国的研究入选了大会口头报告。其中包括我们医院宋玉琴教授报道的泽布替尼治疗R/R MCL最新研究结果。
与伊布替尼不同,新型BTK抑制剂泽布替尼具有更强的选择性。在临床研究中,泽布替尼也表现出较好的疗效和安全性。本次ICML会议上宋玉琴教授汇报了国内开展的泽布替尼治疗R/R MCL的多中心、单臂临床研究的最新研究数据。截止目前,随访已接近18.4个月,有效率高达84.7%,且安全性较好。目前此部分数据已上报中国国家药品监督管理局,期待泽布替尼的临床上市批准。
优秀的团队合作促进泽布替尼走向临床
朱军教授:百济神州作为一家新药研发,特别在生物免疫抗肿瘤治疗领域具有优势的新型创新性公司,在泽布替尼的研发过程中,我们能感受到其理念、意愿和能力。期待今后进一步加强合作,通过长期观察泽布替尼的毒副反应和进一步积累疗效方面的数据,进一步扩大泽布替尼的适应证,为全中国乃至全世界的患者服务。
泽布替尼在血液肿瘤中前景广阔
朱军教授:我们对BTK抑制剂充满了期待,目前国际上也有领先的新药。百济神州在中国领先研发了新型BTK抑制剂泽布替尼,并且泽布替尼获得较好数据进入临床试验。未来通过临床试验进一步扩展其临床适应证,通过深入的临床研究和更长时间的积累,我们相信会获得更多的临床数据和更好的结果。我们也期待百济神州能够在其它肿瘤领域开发更多的创新性新药。作为临床科研团队,我们也愿意且期待与其进一步合作。泽布替尼未来在其他B细胞淋巴瘤包括慢性淋巴细胞白血病/小淋巴细胞淋巴瘤、华氏巨球蛋白血症都有临床扩展空间。通过临床实践进一步探索泽布替尼的剂量、疗程、使用方法,包括联合应用的方式,都是未来临床研究的方向。
宋玉琴教授口头报告泽布替尼治疗R/R MCL的最新研究结果

宋玉琴主任医师,副教授,硕士生导师
北京大学肿瘤医院院长助理,淋巴瘤科主任医师、副主任
中国临床肿瘤学会(CSCO)抗淋巴瘤联盟秘书长
中国老年肿瘤学会淋巴血液肿瘤专业委员会副主任委员
中国血液免疫专业委员会委员
研究背景
泽布替尼是具有高选择性的不可逆BTK抑制剂,既往研究已证实可有效抑制BTK,对其他激酶的脱靶抑制作用很小。此次会议上报告了2期研究中泽布替尼治疗R/R MCL的安全性和疗效的更新结果。

研究方法
在该单臂多中心2期研究中,R/R MCL患者口服泽布替尼(160 mg BID),直至疾病进展(PD)或出现不可接受的毒性。主要研究终点是总治疗反应率(ORR),由独立审查委员会(IRC)根据2014Lugano分类进行评估。次要研究终点包括无进展生存(PFS)、出现治疗反应时间(TTR)、反应持续时间(DOR)、研究者评估的ORR和安全性。

研究结果
中位随访时间18.4个月,60.5%的患者仍在继续接受治疗。
疗效分析:86例疗效可评估患者中,研究者评估的最佳ORR为83.7%,67例(77.9%)达到完全缓解(CR)。

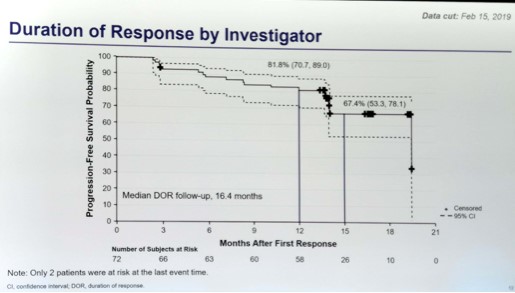
15个月中位持续缓解(DOR)为67.4%,15个月无进展生存(PFS)为72.1%,所有亚组的ORR通常一致。
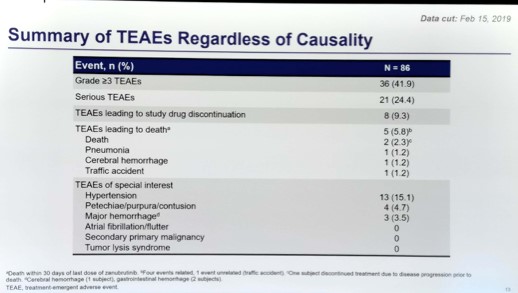
安全性分析:86例患者中,≥3级不良事件发生率为41.9%,其中房颤、第二肿瘤、肿瘤溶解综合征的发生率均为0,高血压发生率为15.1%,瘀点/紫癜/挫伤发生率4.7%,主要出血事件发生率3.5%。
研究结论
泽布替尼在R/R MCL患者中表现出较高且持久的治疗活性,基于PET的ORR和CR率均很高(分别为84%和78%)。同时,泽布替尼在该研究中的安全性与既往报道一致。
查看更多