查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





血管性水肿
变态反应科诊治的常见病中,有一大类起病急骤、严重时可能危及生命的疾病——血管性水肿。它多表现为皮肤和黏膜的水肿,可见于颜面部、外阴、胃肠道、呼吸道等部位,当水肿发生于气道时,可能出现喉头水肿、呼吸困难,严重时导致窒息死亡。因此,针对血管性水肿的及时识别及治疗十分重要。
遗传性血管性水肿(HAE)
临床上比较常见的大部分的血管性水肿发生机制与荨麻疹类似,系接触药物、食物、花粉或动物皮屑等过敏原后,肥大细胞介导的急性过敏反应。但有少部分特殊类型的血管性水肿是由缓激肽介导的、因缓激肽及补体通路功能障碍,而导致的皮下组织血管通透性增加,血管内液体外渗产生的肿胀。这一系列特殊类型的血管性水肿被发现与遗传有关,又称为遗传性血管性水肿(Hereditary angioedema, HAE)。
发病机制
不同类型的HAE中一般存在C1-酯酶抑制物(C1 Inhibitor, C1-INH)的缺乏或功能障碍,C1-INH是凝血因子 XII/激肽释放酶蛋白水解级联反应的关键调节因子。它的缺失除导致补体通路激活受限外,还可使机体失去对激肽释放酶的抑制作用,导致缓激肽释放增加。增加的缓激肽与内皮细胞上的缓激肽B2受体结合,使得液体向局部组织内主动转移,产生血管性水肿。
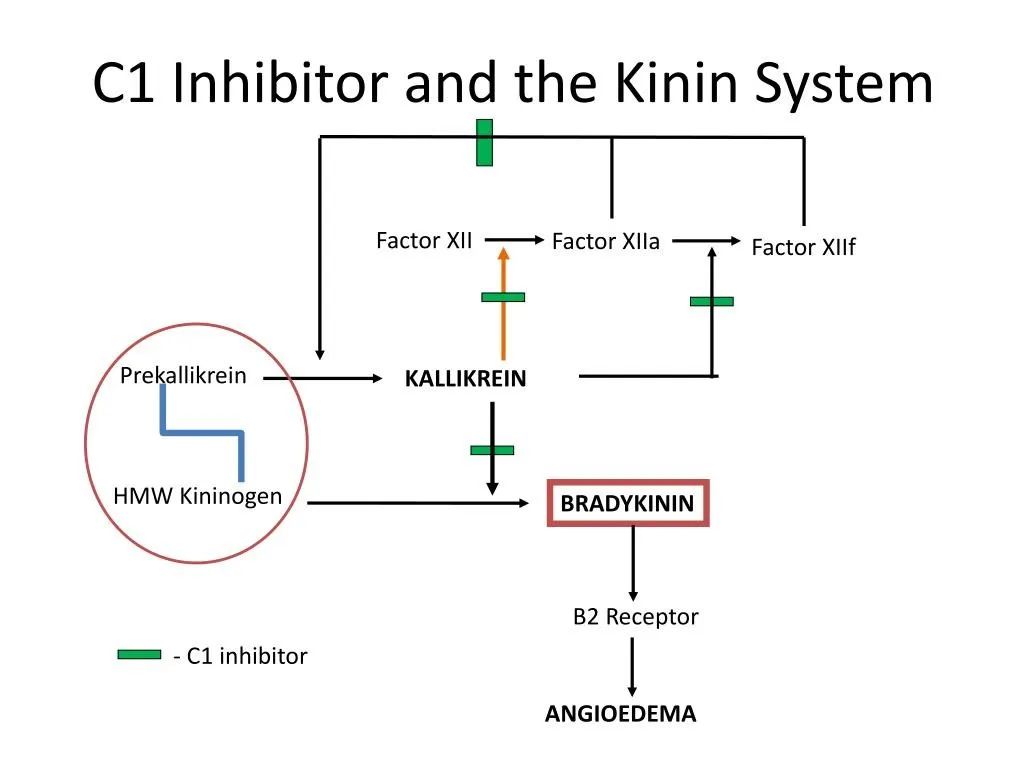
HAE简要发病机制图
基于上述发病机制,可通过补充C1-INH、抑制缓激肽、抑制缓激肽受体等方式治疗HAE。
艾替班特(Icatibant)
艾替班特(Icatibant)是一种缓激肽B2受体拮抗剂,通过竞争性拮抗缓激肽B2受体,抑制过多的缓激肽导致的皮肤、胃肠道、呼吸道黏膜水肿。早在2008年,艾替班特就被欧盟批准用于治疗成人HAE的急性发作。2011年获美国FDA批准上市,用于18岁及以上成年人的HAE急性发作治疗。2017年,它在欧盟的适应证人群扩大,被批准用于2岁及以上儿童和青少年HAE患者。2021年,艾替班特正式在国内获批上市,用于治疗成人、青少年和≥2岁儿童的遗传性血管性水肿(HAE)急性发作,也是国内第一个获批的HAE急性发作期治疗药物。
用法用量
针对成人HAE患者,急性发作时建议腹部皮下注射30mg艾替班特,如症状未控制或复发,可6小时后注射第2剂,如仍未缓解或复发,可再于6小时后注射第3剂,但24小时给药不可超过3次,临床试验针对成人患者中每月给药次数未超过8次。针对2岁以上儿童HAE患者,需根据患者体重确定给药剂量(如下表),临床试验中发作时给药次数未超过1次。
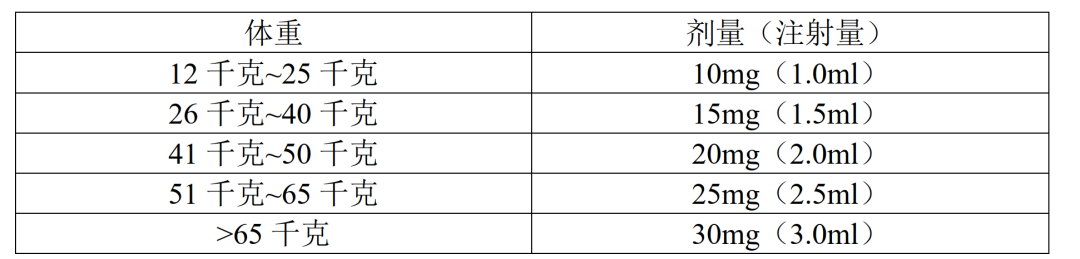
不良反应和禁忌证
一般来说,艾替班特安全性良好,常见不良反应为注射部位的红斑、肿胀、灼痛、皮肤疼痛和瘙痒,部分患者还可能出现头痛、头晕、恶心、发热及转氨酶升高等其他系统不适,但多数不良反应为轻度至中度、表现为一过性,无需进一步治疗,可自行缓解。此外,尽管临床试验中观察到罕有患者出现抗艾替班特抗体阳性,但即使在这部分患者中,艾替班特仍保持疗效。
艾替班特的禁忌证为对活性成分艾替班特或对该品种用到的任何辅料过敏患者。此外,由于拮抗缓激肽B2受体可能使心功能恶化、冠脉血流减少,也可能减弱缓激肽的正性晚期神经保护作用。因此,对有急性缺血性心脏病或不稳定型心绞痛的患者,在艾替班特治疗过程中应注意观察心脏情况;对卒中后数周内的患者,在给药过程应注意观察其神经系统受累情况。
作者:王兰庭
来源:华山变态反应科
查看更多