查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





前言

2020年2月13日-15日,美国临床肿瘤学会-泌尿生殖系统肿瘤研讨会(ASCO-GU) 在美国旧金山召开,本次会议的主题是:“追求以患者为中心的治疗(IN PURSUIT OF PATIENT-CENTERED CARE)”。本文特邀请北京大学第一医院虞巍教授对于本次大会发布的尿路上皮癌(UC)免疫治疗相关的重要研究及进展做以评述,供各位泌尿肿瘤领域专家参阅。
免疫治疗是近年来尿路上皮肿瘤系统治疗的重要进展,已经被美国国立综合癌症网络(NCCN)指南推荐用于转移性尿路上皮癌(mUC)二线治疗,或者顺铂不耐受mUC患者的一线治疗。随着免疫治疗临床研究的开展,其在UC整个诊疗流程当中的作用特点得到了进一步认识,且由于免疫治疗整体上副反应发生率相对较低,因此免疫治疗研究在UC领域进入联合治疗阶段。
一、转移性尿路上皮癌(mUC)
01 免疫治疗联合化疗
对于mUC二线患者,帕博利珠单抗、纳武利尤单抗、德瓦鲁单抗、阿特珠单抗和阿维单抗(avelumab)都已获批mUC二线治疗的适应证。依据KEYNOTE-045研究,单药帕博利珠单抗相对于化疗能够显著改善患者的总体生存(OS)时间,并且副反应发生率较低。但该研究也显示了免疫治疗的一些临床特性,起效较慢、肿瘤无进展生存(PFS)时间较短、免疫治疗早期的生存率低于二线化疗。客观缓解率(ORR)约为20%,PFS为2个月,并且无论是PD-L1高表达还是低表达患者,都存在以上问题,而其他能够预测免疫治疗快速起效的标志物尚在研究中。临床工作中,这些特点使得免疫治疗的临床疗效令人担忧,早期患者尤甚。如果将免疫治疗使用在二线化疗后,患者肿瘤负荷较高、一般状况不佳,免疫治疗疗效可能更不尽如人意。这些都是临床选择免疫治疗时需要实际考虑的因素。
针对这一问题,国际上研究者结合二线化疗早期效果较好,免疫治疗长期疗效较好的特性,提出了化疗联合免疫治疗的策略,让化疗起到免疫治疗搭档和领跑员的作用,并且希望通过化疗的肿瘤杀伤,释放肿瘤抗原,在理论上增强免疫治疗的作用。针对二线患者,在化疗药物的选择上,需要选择副反应较小,早期ORR相对较高的化疗药物。紫杉类药物是目前研究较多的药物。在本次ASCO GU大会上,带来了紫杉类化疗联合免疫治疗的研究报告。
PEANUT研究: 转移性尿路上皮癌的挽救性治疗新选择——帕博利珠单抗联合纳米白蛋白紫杉醇 (nab-paclitaxel) (abstract494)
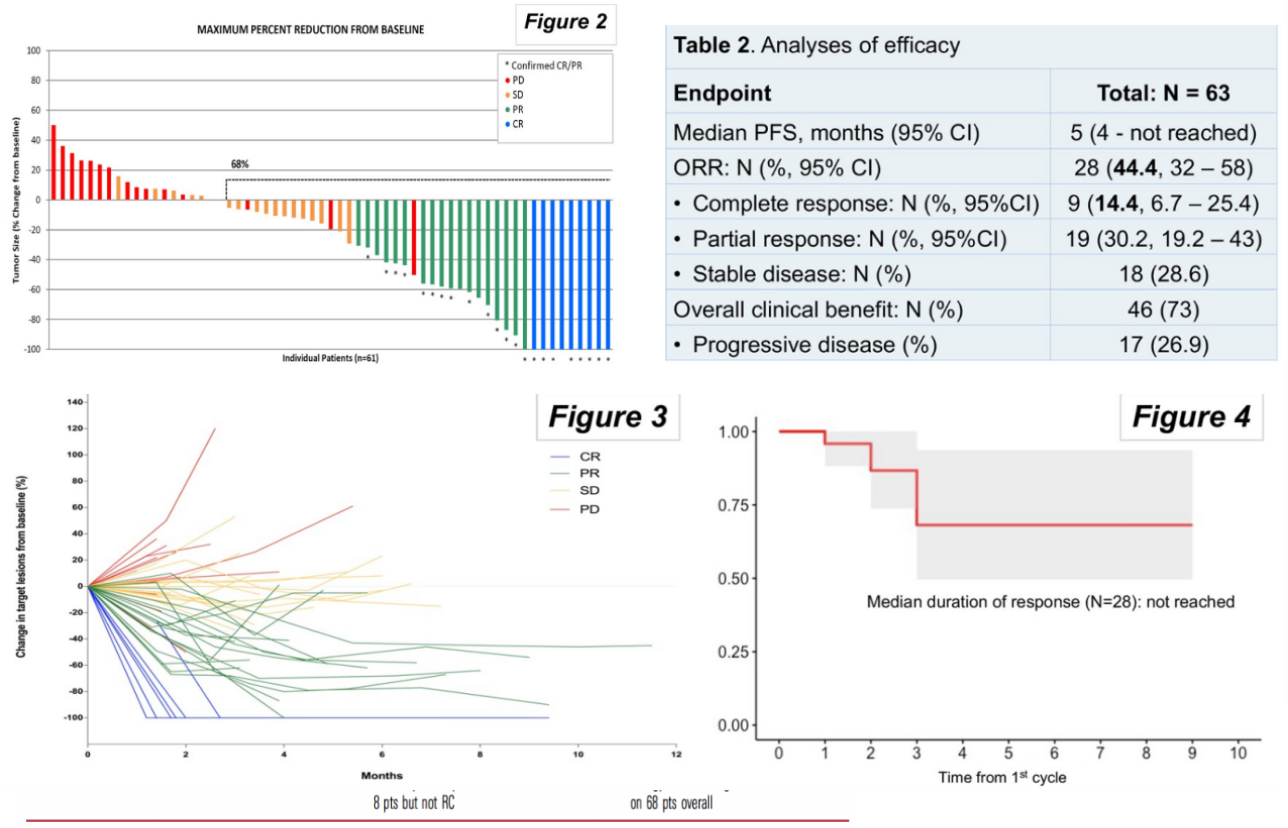
PEANUT研究是一项开放标签、单臂II期研究,评估帕博利珠单抗联合nab-paclitaxel用于含铂化疗失败患者的安全性及疗效。患者接受帕博利珠单抗(200 mg,iv,D1)+ nab-paclitaxel(125 mg/m2 ,iv,D1,D8) Q3w治疗。研究共入组63例患者,中位随访时间5个月,中位年龄69岁;美国东部肿瘤协作组(ECOG)体力状态(PS)评分 1占35%;33%患者有肝转移。疗效方面,中位PFS为5个月,肿瘤控制起效比较迅速,ORR为44.4%,其中完全缓解(CR) 9例(14.4%),部分缓解(PR)19例(30.2%),缓解持续时间(DOR)未达到,疾病稳定(SD)18例(28.6%)。安全性方面,3-4级治疗相关不良反应 (TRAE) 14 例(22%),最常见的TRAE是脱发(76%),乏力和中性粒细胞减少。9例因白蛋白紫杉醇毒性而永久停药。
AVETAX研究:Avelumab联合紫杉烷类化疗在铂难治或不适合铂类化疗的晚期尿路上皮癌患者中的Ⅰb期研究结果(abstract487)
该研究是一项Ⅰb期、单臂、非随机、开放标签的前瞻性临床试验,主要分为两个阶段:第1b阶段采用标准剂量Avelumab(10 mg/kg)联合减量多西他赛(0:75 mg/m2,1:60 mg/m2,2:45 mg/m2)的剂量,以确定标准3+3设计中的第2阶段剂量。在剂量扩展阶段,将评估Avelumab联合多西紫杉醇的第2阶段疗效。联合治疗每3周一次,持续6个周期,然后每2周单独使用Avelumab。共10名患者纳入该研究,Avelumab联合75 mg/m2的多西他赛被认为是安全的剂量扩大队列。初步疗效情况,1名患者达到CR,2名患者出现PR,2名患者出现SD,1名患者出现疾病进展(PD),4名患者尚未评估。最常见的3级或4级AE为发热性中性粒细胞减少、尿路感染和精神异常。未发现与治疗相关的死亡。
小结:对于这两个小样本量的研究,紫杉类化疗联合免疫治疗疗效基本实现了研究者对于两者联合的期待,改善了肿瘤控制情况。但由于是二线治疗患者,联合治疗副反应依然需要重视,副反应还是以化疗相关的副反应为主。整体上,对于二线患者而言,3~4级副反应没有显著增加。因此,联合治疗策略需要临床上提高患者的全程管理能力,在患者一般状况合适的时候及时干预,才能得到更好的疗效。对于mUC一线治疗患者,除了延长OS之外,对于肿瘤的ORR和PFS的要求更高,目前已有的研究主要集中在化疗联合免疫治疗,已经公布的IMvigor130研究结果对此方向具有积极的推动作用,我们期待更多的化疗联合免疫的Ⅲ期研究结果报告(TPS 588)。
02 免疫治疗联合新型药物
在目前,mUC一线选择铂类化疗、二线选择免疫治疗的治疗模式下,加上患者管理改善,相当一部分患者会进入三线治疗阶段,因此该领域的选择也会成为未来临床研究热点。本次大会上,回顾性真实世界研究(abstract 458)显示,免疫治疗后选择紫杉类化疗,其ORR为18%,PFS 2.9个月。结果提示这些患者继续选择化疗疗效欠佳,需要研究新的治疗手段,其中抗体偶联药物(ADC)和靶向治疗是目前研究热点。针对尿路上皮肿瘤细胞表面表达Nectin-4蛋白比例很高的特点,研发了针对性药物。Enfortumab-vedotin(EV)是一种ADC型药物,由微管破坏剂MMAE和抗Nectin-4单克隆抗体连接组成。在2018年ASCO GU大会上公布了抗体偶联药物Enfortumab-vedotin用于治疗二、三线mUC患者的初步疗效,其ORR高到40%,给学术界留下了深刻影响。在2019年12月,美国食品和药物管理局(FDA)批准了EV用于mUC二线治疗的适应证。基于既往其它瘤种的研究经验,化疗联合免疫治疗是一个重要发展方向。因此采用ADC药物联合免疫在理论上既可以协同杀伤肿瘤细胞的,又能避免了全身化疗对免疫功能的抑制作用,更好地发挥免疫治疗的疗效,并且在更为早期的患者中疗效更为显著。EV-103研究:EV联合帕博利珠单抗治疗局部晚期或转移性UC的初步耐受性结果(Abstract: 441)
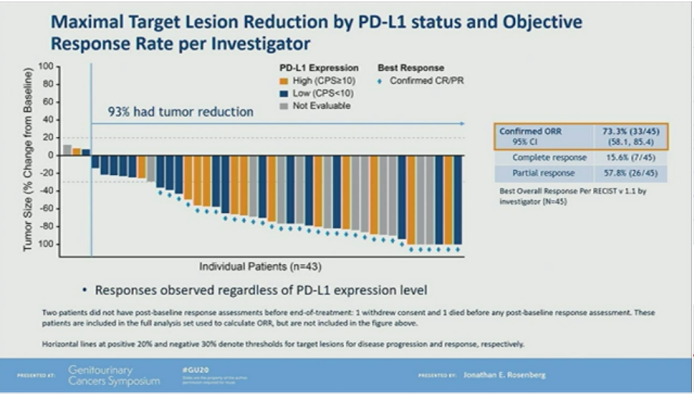
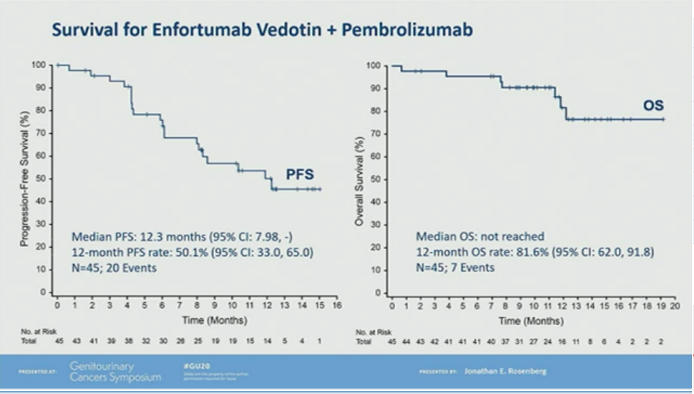
EV-103研究入组的是顺铂不耐受的一线治疗患者。中位随访11.5个月,研究者评估的ORR为73.3%,疾病控制率93%。肝转移患者的ORR为53.3%(8/15)。PD-L1高表达组和低表达组的ORR分别为78.6%和63.2%。中位PFS为12.3个月。最常见的AE为疲劳(58%,11%≥G3)、脱发(53%)和周围感觉神经病变(53%,4%≥G3)。有一位患者死于多器官衰竭相关AE。该研究显示,对于顺铂不耐受的一线治疗患者,EV+帕博利珠单抗具有良好的抗肿瘤活性和持久性,且安全性在可控范围内。对比同样都是顺铂不耐受患者的卡铂化疗方案和免疫治疗单药方案,EV+帕博利珠单抗无论是在ORR、PFS、1年OS率上的数据都显著优于目前的标准治疗,甚至优于目前一线顺铂治疗的数据,并且副反应发生率相对较低。因此,EV+帕博利珠单抗很可能会迅速进入mUC一线治疗研究领域,有望开启mUC无顺铂化疗的时代。
FGFR抑制剂erdafitinib是FDA批准用于mUC二线治疗中存在FGFR基因突变患者的靶向治疗。既往研究显示,对于二、三线治疗的患者,约40%存在FGFR的突变,而这部分患者使用erdafitinib后,ORR约为40%,PFS 5.5个月,OS为13.8个月。从基因组学研究来看,FGFR突变的患者肿瘤免疫可能较弱(Abstract 432,493),两种治疗策略可能存在互补性,但也有研究结果显示FGFR突变患者接受免疫治疗的疗效不存在显著差异(Abstract 560,570)。考虑到肿瘤的异质性,两者联合是否有可能带来更好的肿瘤控制仍有待研究证实。本次大会上公布了有关FGFR抑制剂与免疫治疗联合的临床研究计划(Abstract 511, TPS 590、592)。我们期待这些研究结果早日公布,以便为临床提供更多治疗选择。erdafitinib是多靶点药物,对于VEGFR、FGFR等通路均具有抑制作用。erdafitinib联合免疫治疗已经在肾癌、肝癌等瘤种展开了研究。在mUC方面,针对不能耐受顺铂一线治疗mUC患者的III期LEAP-011研究(TPS 597)正在进行之中。
作者 | 唐琦 虞巍(北京大学第一医院泌尿外科)
编辑 | 郝冉(中国医学论坛报)

查看更多