查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





卵巢癌易转移,预后差,是致死性最高的女性生殖系统恶性肿瘤,给女性的生命健康造成了严重威胁。不过由于缺乏有效的生物标志物,临床上及时诊断卵巢癌十分困难。实验室检验已广泛应用于常规健康检查,其中一些检验项目已被证明与卵巢癌的诊断和预后显著相关。
虽然常规实验室检验项目有可能成为卵巢癌生物标志物,但目前还没有一种项目能为个体卵巢癌预测提供足够的灵敏度或特异性。令人兴奋的是,新兴的人工智能(AI)技术可以整合来自多种检测的数据,从而帮助诊断。今年1月,The Lancet Digital Health在线发表了一项中国的多中心、回顾性队列研究,该研究旨在系统评估常规实验室检验对卵巢癌诊断的价值,并开发稳定、可推广的集合人工智能模型,以辅助诊断卵巢癌[1]。本文梳理该研究要点,以飨读者。
研究方法
这项回顾性多中心研究收集了三家医院2012年1月至2021年4月期间诊断为卵巢癌(包括原发性恶性卵巢癌、输卵管癌或腹膜癌)和子宫附件良性病变/正常体检女性患者的98项实验室检查和临床特征。华中科技大学同济医学院附属同济医院的受试者(TJ队列)被选为训练集,并对训练集进行了五折交叉验证。两个外部验证集分别来自浙江大学医学院附属妇产科医院(WHZJU队列)和中山大学肿瘤防治中心(SYSUCC队列)。有其他恶性肿瘤或癌前病变史者、过去6个月内怀孕或感染艾滋病毒者、非此3家医院新诊断者及无可用实验室检验结果者均被排除在外。最终研究共纳入10992例受试者(图1)。
图1 研究人群入选流程图
在数据预处理后,研究者基于人工智能融合方法构建了卵巢癌预测模型-基于多准则决策的分类融合(MCF)模型。该算法整合了20个人工智能基分类模型(图2),分别在一个内部验证集(3007人)和两个独立的外部验证集(5641人和2344人)中对模型进行了性能评估。研究主要结果为MCF模型的卵巢癌预测准确性,通过受试者工作特征曲线下的面积(AUC)、准确性、特异度、灵敏度、阳性预测值、阴性预测值和F1分数来量化。
图2 MCF构建及验证过程示意图
研究结果
研究人群的基线特征如表1所示。
表 1 研究人群基线特征
卵巢癌诊断MCF模型最终纳入52个特征(51项实验室检查和年龄),这52个特征的重要性排序如图3所示。其在内部和两个外部验证集上的表现如表2所示,AUC分别达0.949(95%CI 0.948-0.950)、0.882(95%CI 0.880-0.885)和0.884(95%CI 0.882-0.887)。
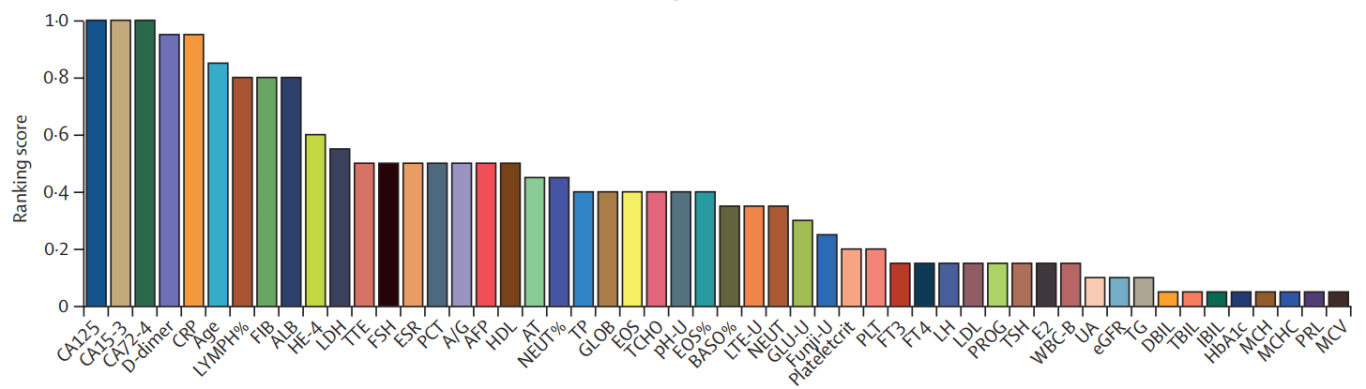
表2 MCF模型诊断卵巢癌的表现
与CA125、HE4及两者联合的诊断性能对比,MCF模型(MCFall)在识别卵巢癌患者(图4A-C)、特别是早期卵巢癌(图4D-F)患者时,显示出显著更高的AUC和灵敏度。即使在CA125和其他肿瘤标志物数值缺失的情况下,MCF模型使用不完整的常规实验室检验指标和年龄,依然可以对卵巢癌的风险进行较准确的预测,且预测效果优于目前已被报道的卵巢癌预测集成模型。
图4 不同模型表现对比
研究结论
基于常规实验室检验的卵巢癌诊断MCF模型在3个验证集中均取得了满意且较稳定的表现,为卵巢癌提供了低成本、易获取且准确的辅助诊断工具。不仅是对卵巢癌诊断重要性排名最高的CA125,最后纳入模型的检验指标均对识别卵巢癌患者有贡献。
该研究研发的MCF模型已封装成开源的卵巢癌预测工具,按照提示输入相应实验室检验数据和年龄即可计算卵巢癌的风险值。
参考文献:
1. Cai G ,Huang F ,Gao Y , et al.Artificial intelligence-based models enabling accurate diagnosis of ovarian cancer using laboratory tests in China: a multicentre, retrospective cohort study.[J].The Lancet. Digital health,2024,6(3):e176-e186.
声明:本文的发布由阿斯利康提供支持,仅供医疗卫生专业人士参考
审批编号:CN-133822
有效期至:2025-4-17
查看更多