查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





人工智能赋能乳腺癌个体化治疗专刊
Cancer Biology & Medicine
据统计,乳腺癌已成为全球女性发病率最高的恶性肿瘤,每年新发病例超过230万。面对这一沉重的疾病负担,乳腺癌诊疗领域正以前所未有的速度演进——精准医学不断深入临床实践,人工智能逐步赋能诊疗决策,国内外学者的研究步伐也在持续加快。在这一背景下,Cancer Biology & Medicine与中国人民解放军总医院江泽飞教授联合打造“人工智能赋能乳腺癌个体化治疗”专刊,旨在汇聚顶尖专家的智慧,系统呈现乳腺癌诊疗领域的新进展、新思考和新突破。
肿瘤患者是否存在淋巴结转移直接决定其手术范围、治疗策略与长期预后,是临床决策的关键指标。病理学诊断技术难以满足术中对淋巴结转移快速、准确、简便、低人力成本的诊断需求,无法真正实现手术台上“即查即诊”。动态全视野光学相干断层扫描(D-FFOCT)可实现亚细胞分辨率的“类病理”成像,以高分辨率捕捉组织微观结构与细胞动态变化。在本期专刊中,北京大学人民医院乳腺中心王殊教授团队发表研究性文章,该研究将D-FFOCT技术与深度学习算法深度融合,形成“光学成像+AI自动判读”的一体化诊断体系,成功实现对乳腺癌腋窝淋巴结转移的术中实时精准判定。该体系兼具无创、快速、准确率高、低人力成本等突出优势,为肿瘤患者术中淋巴结转移状态评估提供了可靠的解决方案。

Cite

Zhang S, Yang H, Zhang Y, Li X, Zhao J, Zhang Y, et al.Virtual histology imaging of lymph nodes via dynamic full-field opticalcoherence tomography and deep learning to differentiate metastasis. CancerBiol Med. 2026; 23: 418-429. doi: 10.20892/j.issn.2095-3941.2025.0747
内容介绍
本研究采用双中心、前瞻性设计,共采集新鲜腋窝淋巴结的D-FFOCT成像切片747张,将其分为训练/验证集(n=590)和独立测试集(n=157),并通过滑窗裁剪D-FFOCT图像,构建了超30000张的图像块数据集。研究使用病理组织学诊断作为金标准,分别评估了外科医生(人类专家)和深度学习模型的诊断效能。
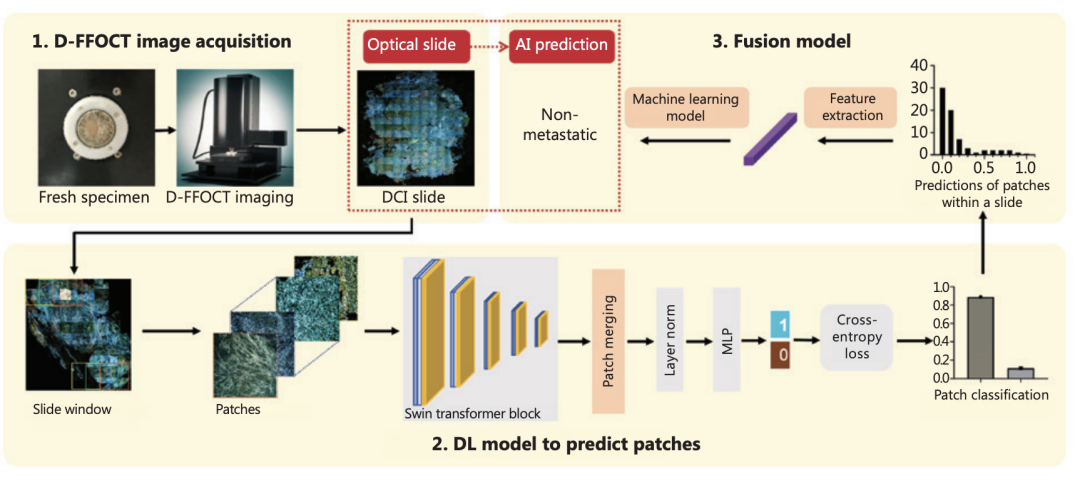
研究流程图
D-FFOCT实现虚拟组织学成像,精准识别淋巴结转移特征
D-FFOCT成像无需组织固定、染色及造影剂,可完整保留标本完整性,其成像结果与HE染色病理切片在组织和细胞水平高度吻合,能清晰显示转移和非转移淋巴结的典型特征。同时,D-FFOCT可识别不同乳腺癌类型的转移灶,可视化微转移灶,并可实现良恶性细胞的有效鉴别。
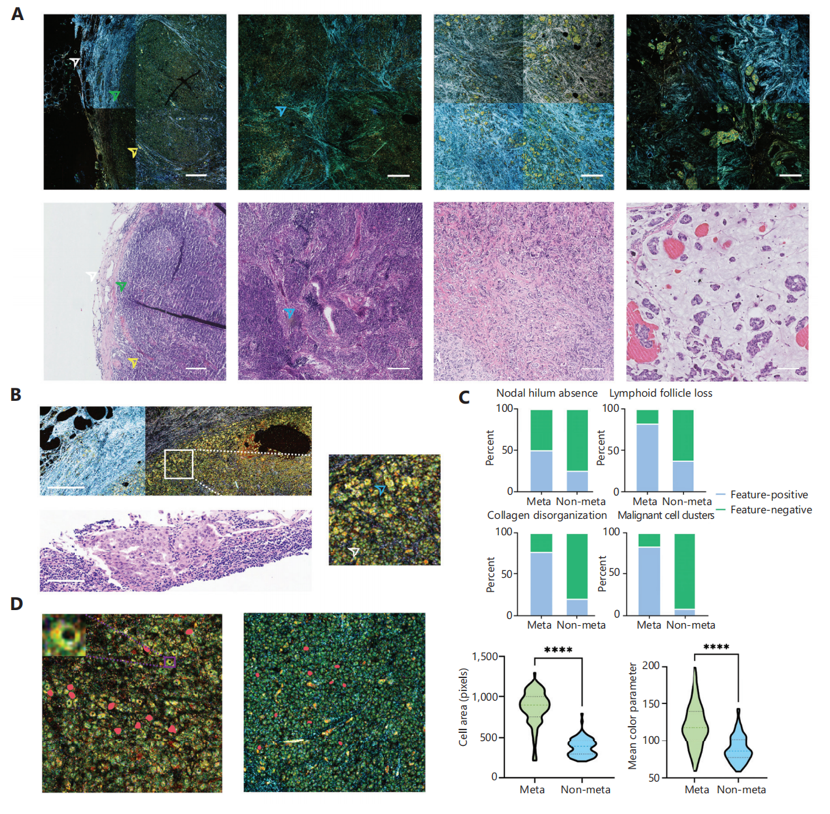
图1 D-FFOCT的淋巴结虚拟组织学成像
(A)正常淋巴结的皮质、髓质和被膜、淋巴滤泡、髓索结构显示,浸润性导管癌及黏液癌的转移淋巴结典型D-FFOCT图像;(B)D-FFOCT对微转移灶的识别;(C)转移性与非转移性淋巴结D-FFOCT图像的特征对比分析;(D)正常淋巴细胞与肿瘤细胞的细胞大小及色彩特征定量比较
深度学习模型性能媲美人类专家,诊断效能优异
研究团队基于Swin Transformer(Swin-T)架构构建深度学习模型,对28911张图像块进行训练,通过图像块分类与特征融合,实现切片水平的转移状态预测。Grad-CAM热图显示,模型诊断聚焦于恶性细胞簇集等关键区域,诊断经验与人类相似。
在独立测试集中,该深度学习模型在切片水平的诊断灵敏度为87.88%、特异度为91.94%,受试者工作特征曲线下面积(AUC)达0.899,诊断准确性为91.08%。模型诊断性能与经D-FFOCT培训的资深乳腺外科医师无统计学差异(P=0.627)。
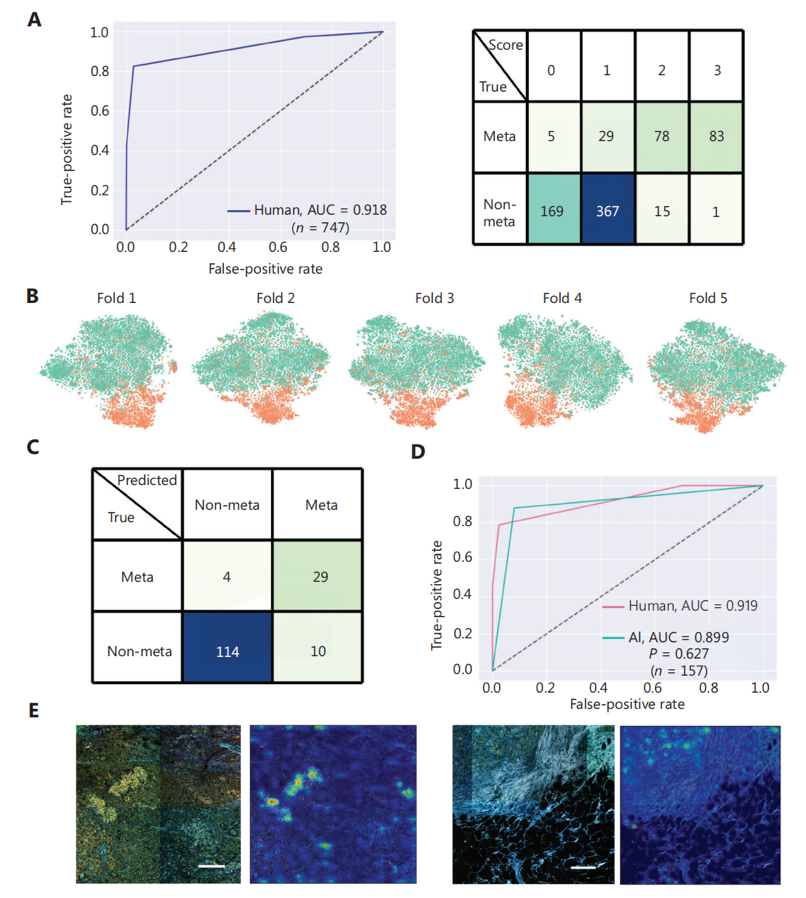
图2 专家与深度学习模型的诊断性能对比
(A)外科医生对747张切片的诊断结果;(B)测试集图像块特征表示的t-SNE可视化;(C)深度学习模型在157张测试集的诊断混淆矩阵;(D)测试集中模型与人类专家诊断的ROC曲线对比;(E)叠加Grad-CAM热图的D-FFOCT图像显示,模型可识别典型、非典型两种恶性细胞模式。
人机协同的新型诊断体系
鉴于人类专家诊断具有更高的诊断特异度,研究团队构建了人机协同诊断工作流:由深度学习模型完成初筛,仅对模型判定为阳性的病例交由医师复核确诊。该模式下,仅24.84%的淋巴结需人工读片,临床诊断工作量降低75%,同时使诊断特异度进一步提升至98.39%,整体准确率达93.63%。除微转移和孤立肿瘤细胞(ITC)亚组中诊断效能受限外,该协同诊断体系在各亚组中均表现优异,为后续模型优化指明了方向。
与传统淋巴结评估方法相比,D-FFOCT联合AI的联合诊断体系具有显著临床优势:成像分辨率达微米级;全程耗时约20分钟,快于冰冻病理和分子检测技术;完全保留组织样本;人工消耗低,设备与空间成本适中,更适合临床推广应用。
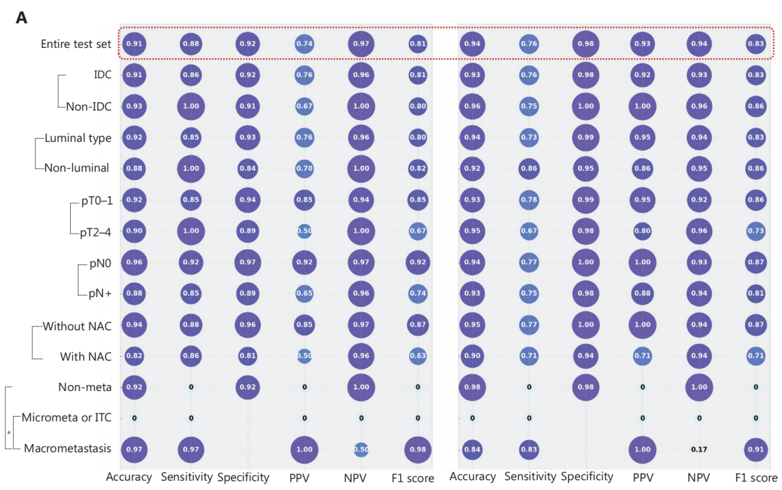
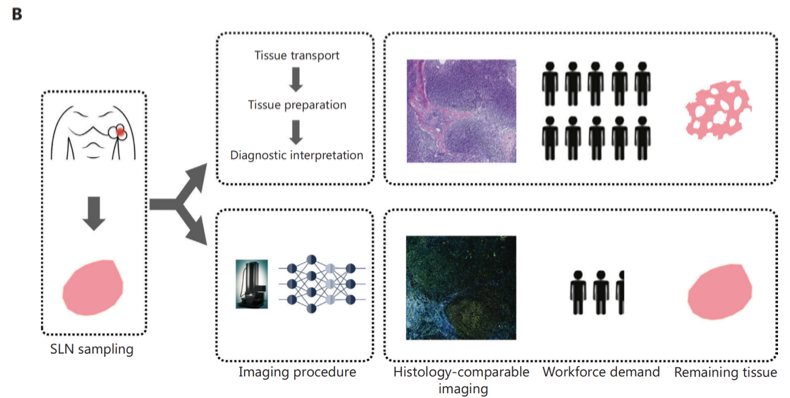
图 4 光学+人工智能结合诊断流程及亚组诊断结果
(A)深度学习模型(左)与人机协同模式(右)在测试集及各亚组中的各项性能指标对比;(B)基于D-FFOCT联合深度学习的淋巴结评估简化诊断流程可显著降低人力需求,无需组织制备,并能保留标本完整性用于后续其他检测。
小结
本研究通过大样本、双中心、前瞻性队列,首次系统验证了D-FFOCT联合深度学习在乳腺癌腋窝淋巴结转移诊断中的临床价值。该技术可实现无消耗、近病理级实时成像,AI诊断效能媲美人类专家;人机协同模式大幅降低临床工作量,并进一步提升诊断特异度,为术中淋巴结快速评估提供了全新方案。
作为新型光学成像技术,D-FFOCT兼具无标记、高分辨率、组织保留、实时成像等优势,与AI自动化分析结合,突破了传统病理诊断的瓶颈。结合团队前期成果,D-FFOCT技术已实现乳腺癌原发灶-手术切缘-淋巴结等术中诊断场景的全覆盖。此外,D-FFOCT所呈现的肿瘤细胞异型性、组织结构紊乱等关键特征与病理诊断的核心特征高度一致,未来可拓展至多种实体瘤淋巴结转移评估。
目前该技术仍存在一定优化空间,如微转移灶识别能力、成像伪影尚待改进等。团队未来将持续优化模型、改进成像技术,在开发三维立体成像与图像定量化解析方面继续深耕,推动该技术向临床转化与普及。
总之,本研究将光学成像与人工智能深度融合,为肿瘤术中无创快速精准诊断开辟了新路径。
通信作者
王殊 教授
北京大学人民医院
医学博士,主任医师,教授,博士生导师,北京大学二级教授
北京大学人民医院乳腺中心主任
中国临床肿瘤学会乳腺癌专业委员会(CSCO-BC) 副主任委员
中国抗癌协会乳腺癌专业委员会(CBCSG) 常务委员
中华医学会外科学分会乳腺学组 委员
北京医学会乳腺疾病分会 副主任委员
北京肿瘤学会乳腺外科专业委员会 副主任委员
北京医师协会乳腺疾病专家委员会 副主任委员
长期致力于乳腺癌精准诊疗技术研发与转化,以临床需求驱动技术革新,在术中智能诊断、基因组学分析、个体化治疗模型及行业标准制定等领域取得系统性突破。获省部级科技奖3项(北京市科学技术进步奖、华夏医学科技奖等),累计发表SCI论文100余篇(他引1400余次),主持国家级项目6项(含国家重点研发计划3项,国家自然科学基金3项),实现2项专利产业化,构建了从基础研究到临床实践再到产业转化的系统性创新生态,显著提升乳腺癌个体化诊疗水平。
来源:Cancer Biology Medicine
查看更多