查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过






无菌小鼠几乎不存在IgA
另外有趣的是,移植肠菌的不同使得表达的IgA也有所不同,这说明肠道微生物组的性质可以改变脑膜B细胞和抗体的特征。
那么这些B细胞会是肠道派过来的吗?
研究者对实验动物的脑膜和肠道中的B细胞受体(BCR)进行了测序对比,发现21.5%的脑膜克隆与小肠克隆有关,二者存在共同起源。显然,至少有相当一部分的脑膜B细胞是来自肠道的。
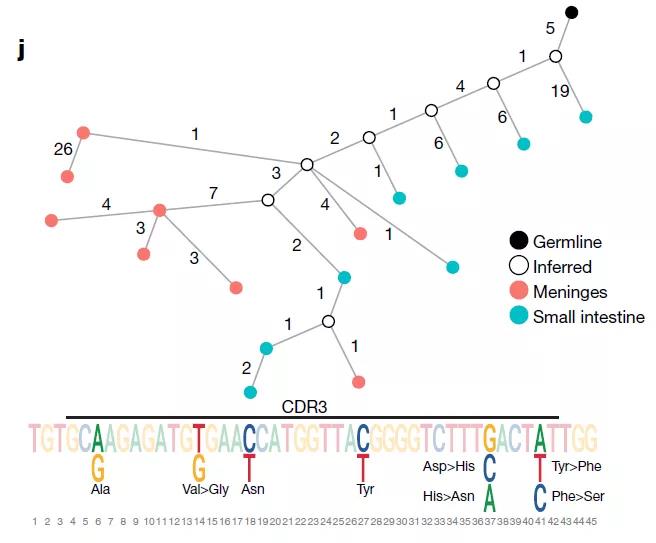
脑膜与肠道中抗体的谱系分析
在肠道中,IgA对维持屏障完整性非常重要,它可以将病原体“围困”在黏液层中,让它们远离上皮细胞。此外,在针对细菌、病毒和真菌的免疫活动发生后,IgA也能够起到保护作用。
而脑膜中的IgA+B细胞则主要聚集在硬脑膜静脉窦附近,所以研究者们猜测这些IgA可能构成了窦旁屏障的一部分,阻止静脉中的病原体向中枢神经系统散播。
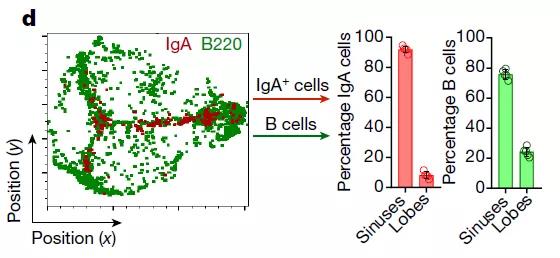
可见IgA出现比较集中
研究者们向小鼠静脉注射了白色念珠菌,发现小鼠硬脑膜静脉窦壁IgA+B细胞出现了明显的扩增,也能够观察到真菌被捕获。当研究者特异性减少了小鼠的脑膜B细胞,小鼠脑组织中的真菌负荷明显增加,小鼠死亡率也上升了。
本研究的通讯作者,剑桥大学的Menna Clatworthy教授也对这个发现有些惊讶,表示大脑的免疫已经不再神秘,但发现这道防御线竟然来自肠道仍然是很惊奇的。同时他也认为这很合理,毕竟肠道屏障的轻微破坏就会导致病原体进入血液,如果这些病原体进入大脑就会带来毁灭性的后果。通过识别肠道微生物的确能够确保防御最可能的入侵者。
来源:奇点网
查看更多