查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





现病史
33岁中年女性,主诉体重异常增加4年余。患者幼年体重正常,2019年起体重进行性增加,2020年节食减重后复胖,近3年体重增加32kg,伴有乏力、活动后气促。
既往史
高血压病史10余年,最高血压190/110mmHg,控制欠佳,否认糖尿病和冠心病史,夜间打鼾和呼吸暂停严重,未接受治疗。
辅助检查
查体:身高1.58m,体重116.1kg,BMI 46.51,腰围140cm,臀围142cm,腰臀比0.99。

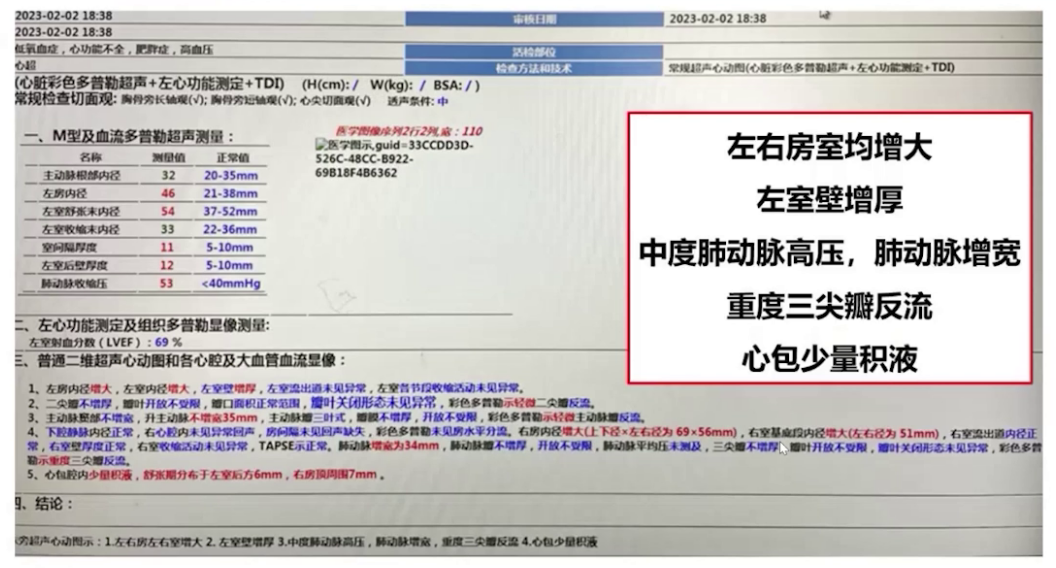
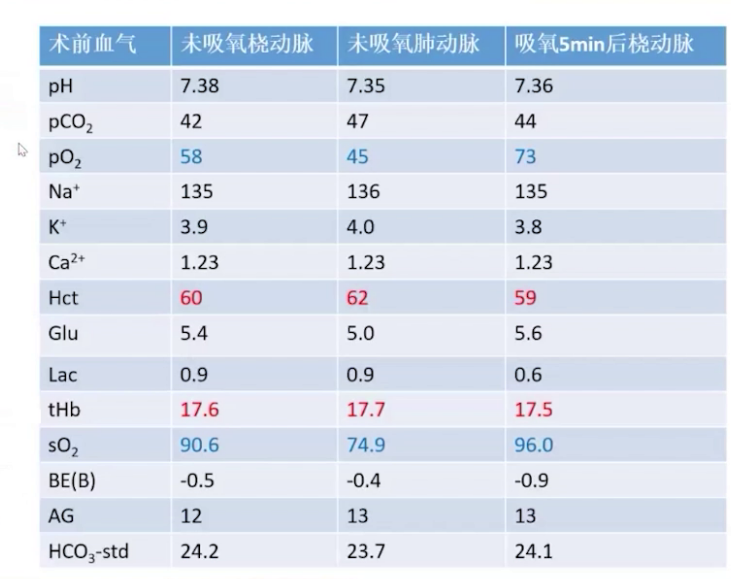
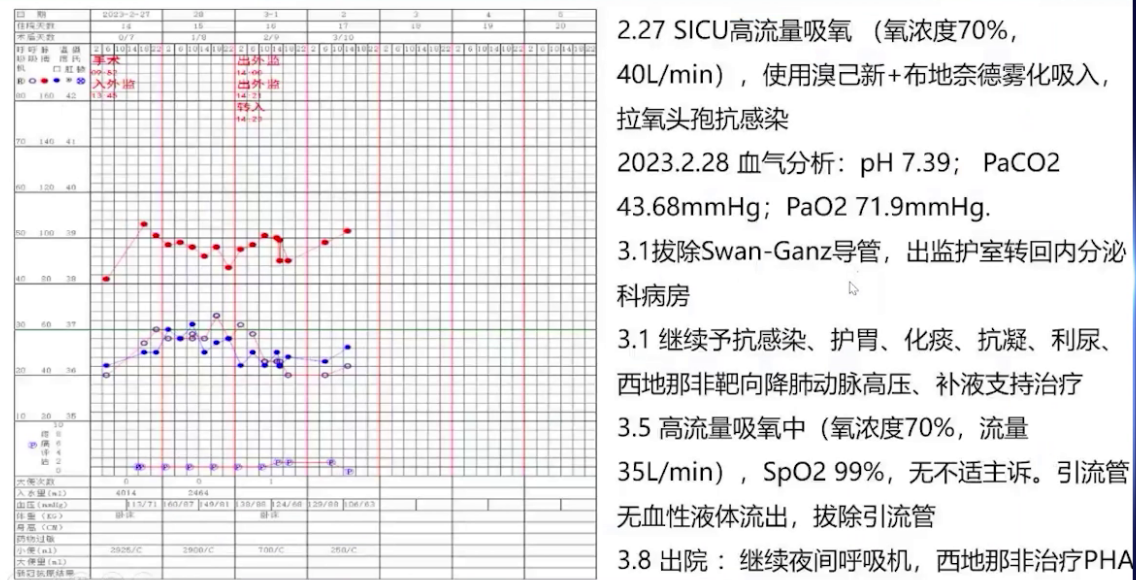
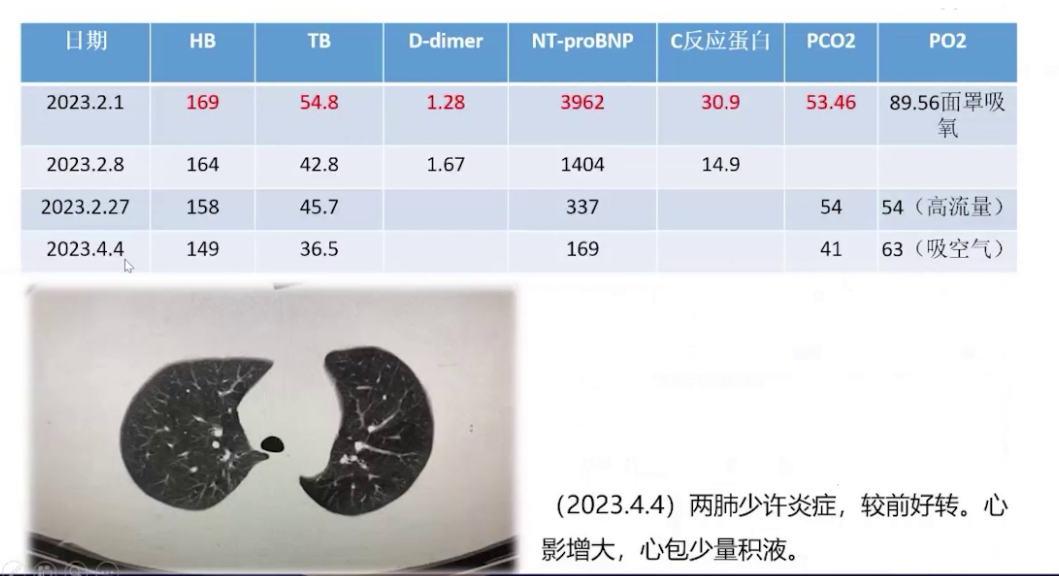
实验室检查:血红蛋白和红细胞升高,D-二聚体升高,总胆红素升高,提示右心功能不全,心肌标志物cTnT 0.013ng/mL,NT-proBNP 3962pg/mL,C反应蛋白升高;血气分析(面罩吸氧10L/min)示pH值7.34,二氧化碳分压53.46mmHg,氧分压89.56mmHg。

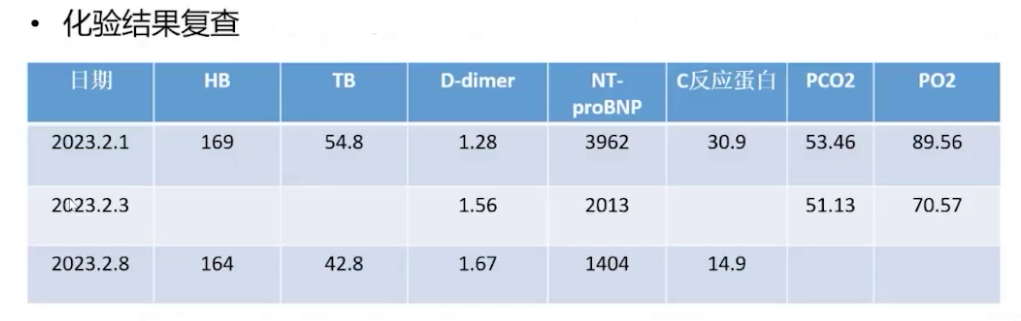
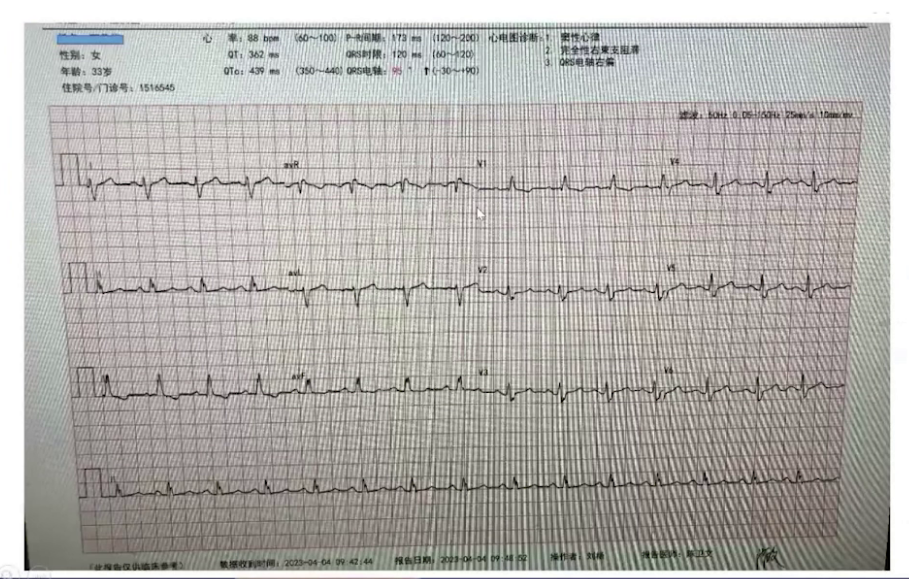
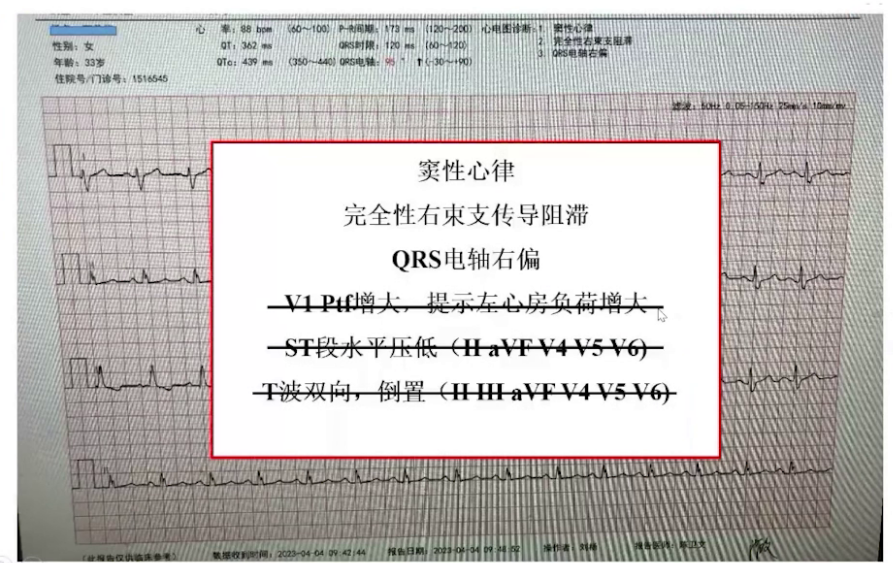
心电图:窦性心律,92次/分,完全性右束支传导阻滞,电轴右偏,P波导联增大,V4-V6导联ST段压低和T波双向,提示全心扩大、心肌缺血。
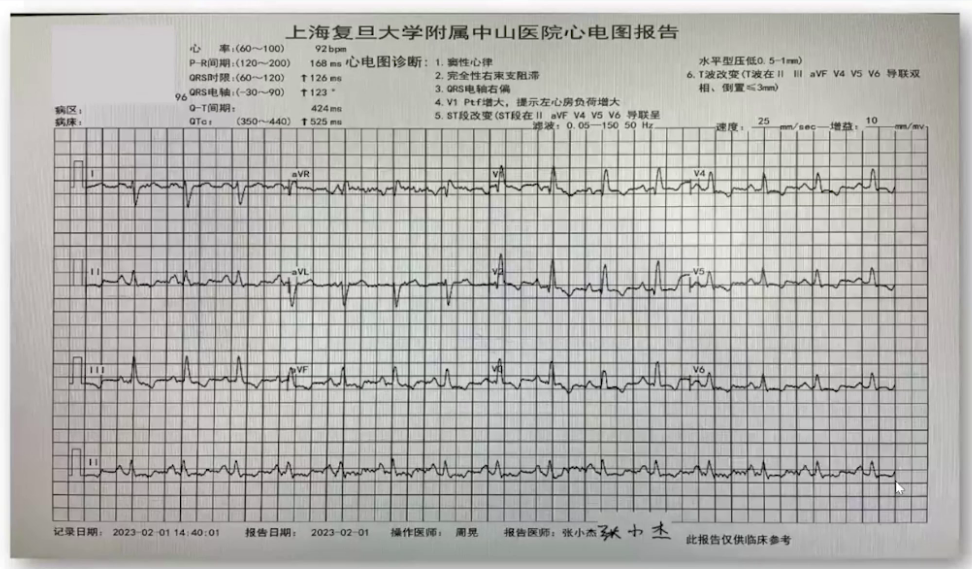
肺部CT:两肺散在炎症,左下肺斑片状实变,心影增大,少量心包积液。
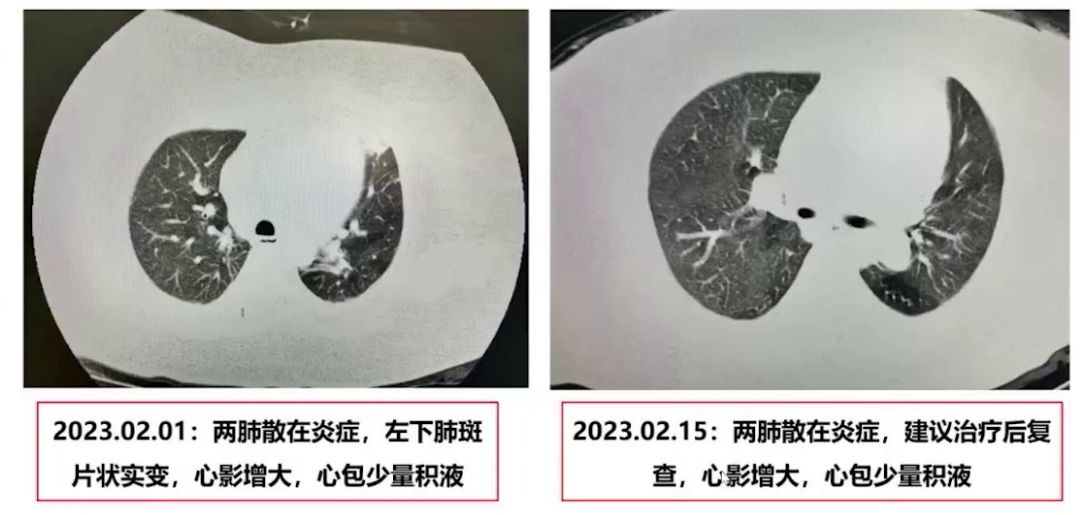
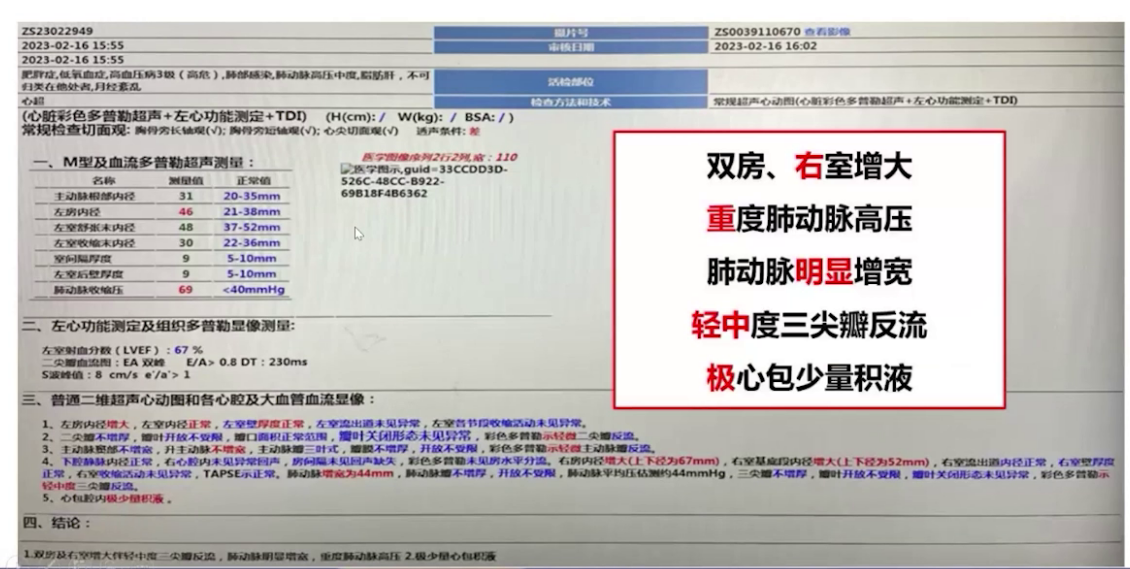
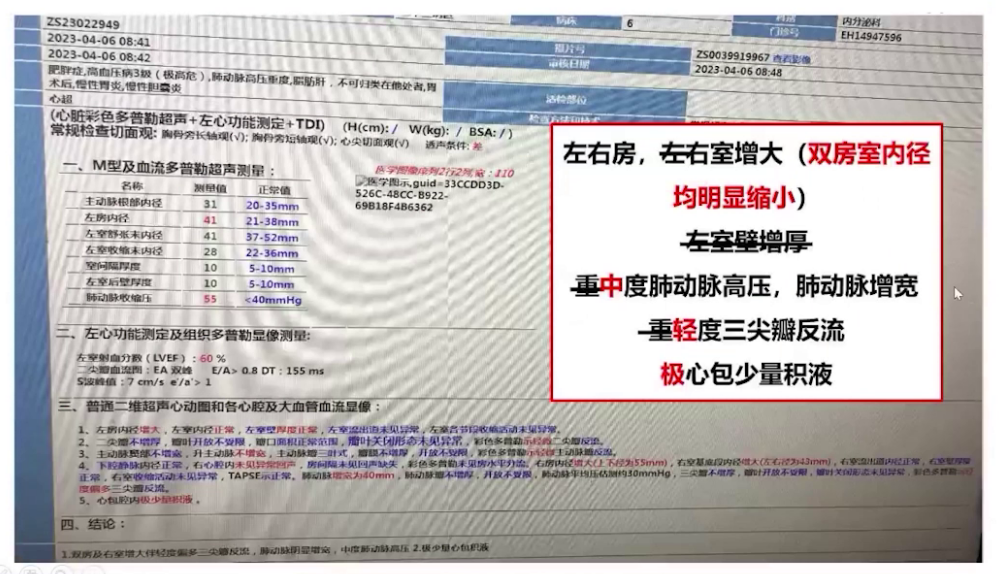
心脏超声:左右房室增大,左室壁增厚,中度肺动脉高压(肺动脉收缩压53mmHg),肺动脉增宽,重度三尖瓣反流和少量心包积液。
诊断
肥胖症;Ⅱ型呼衰;高血压病3级(高危);肺部感染;重度肺动脉高压;脂肪肝;月经紊乱
拟行手术
腹腔镜垂直(袖状)胃切除术+腹腔镜下胆囊切除术
术前评估
内分泌科召集减重手术MDT讨论,包括心内科、呼吸科、麻醉科、普外科和内分泌科,讨论建议:
2.夜间BiPAP辅助通气治疗;
3.完善右心导管测压,继续抗心衰治疗;
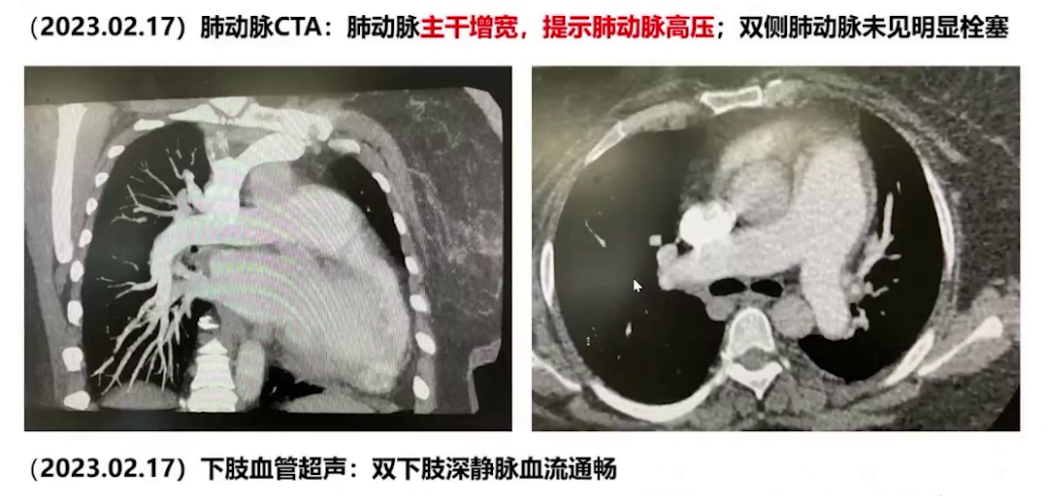
4.完善下肢静脉超声及肺动脉CTA检查,排除血栓和栓塞;
5.关注术后并发症,建议术后转监护室进一步治疗。
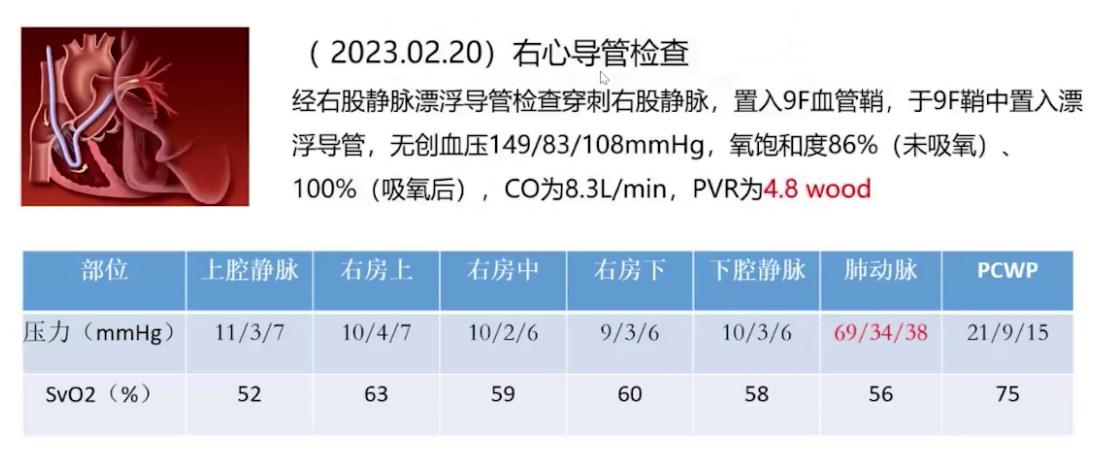
完善检查后,肺动脉CTA提示肺动脉高压,无栓塞,下肢深静脉通畅;右心导管检查肺动脉压力69/34/38mmHg,混合静脉血氧饱和度56%。
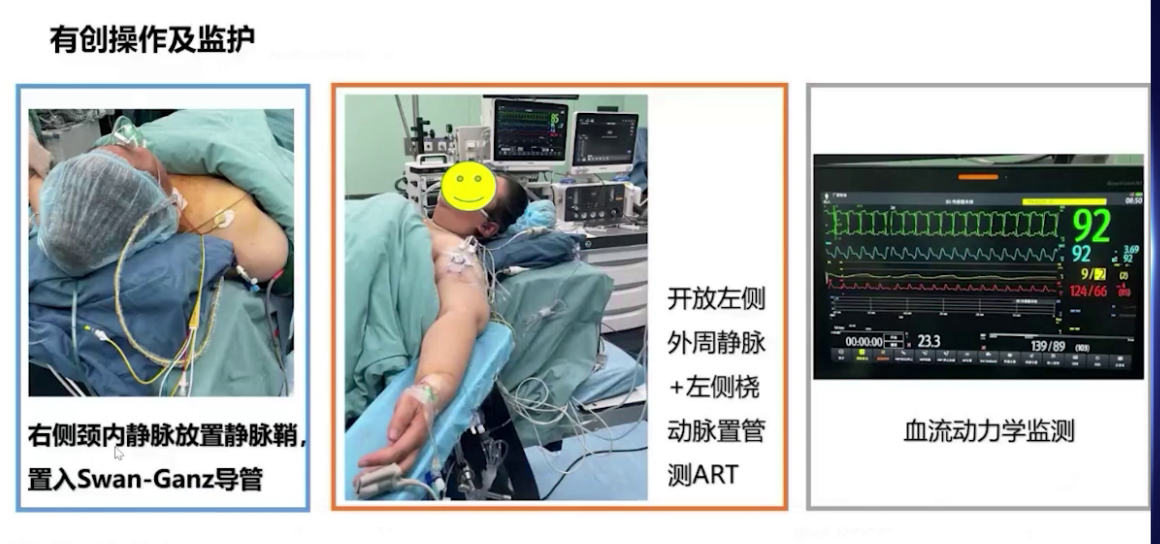
麻醉管理
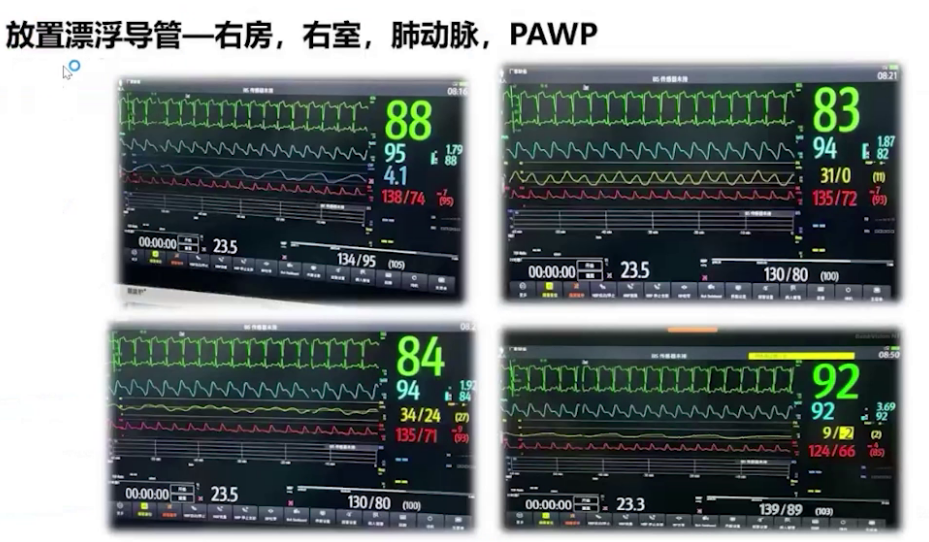
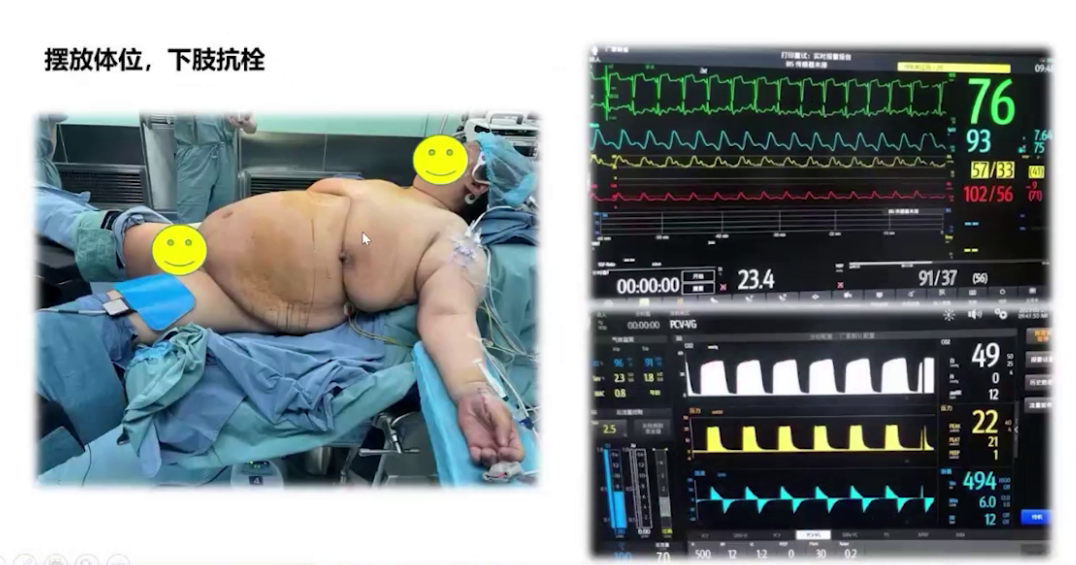
1.麻醉计划:采用全麻复合双侧腹横筋膜阻滞,以减少阿片类药物使用。通过漂浮导管全程监测心排量、肺动脉压力变化及混合静脉血氧饱和度。诱导前放置漂浮导管,右房压4mmHg,右室压31/0mmHg,肺动脉压34/24mmHg。插管方式为诱导前面罩高流量吸氧,诱导后置入鼻咽通气道,可视喉镜下插管。静脉泵注正性肌力药米力农,同时吸入一氧化氮,以降低肺血管阻力。维持体循环阻力和外周器官灌注,采用肺保护性通气策略。术后完善镇痛,采用高流量鼻导管或鼻罩面罩吸氧保障氧合,术后在外科监护室过渡1-2天。
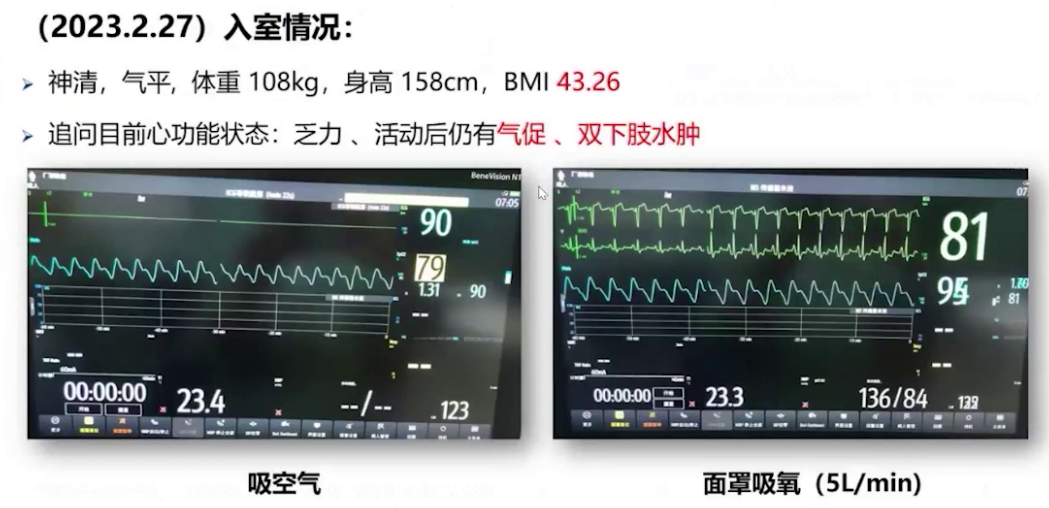
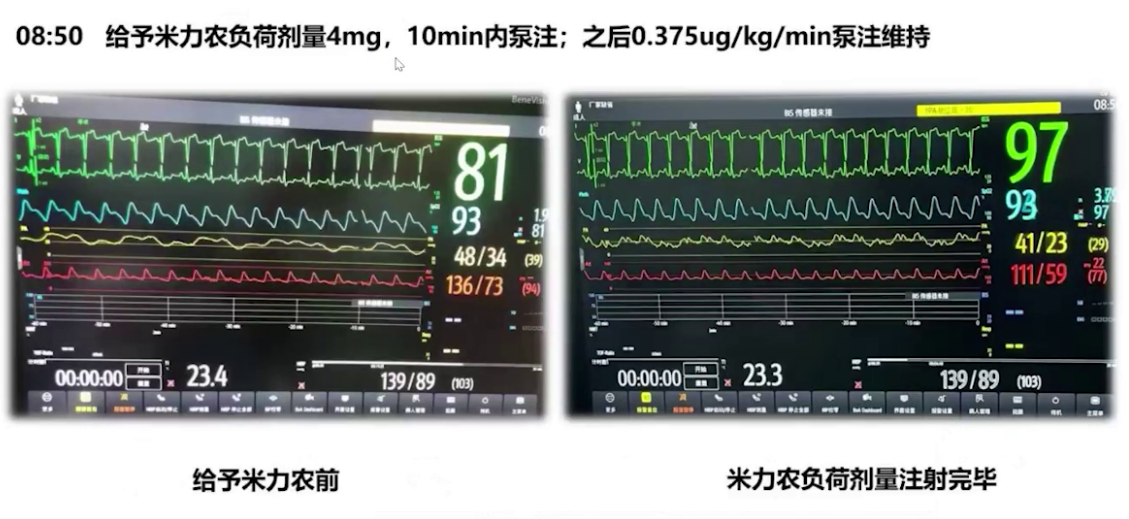
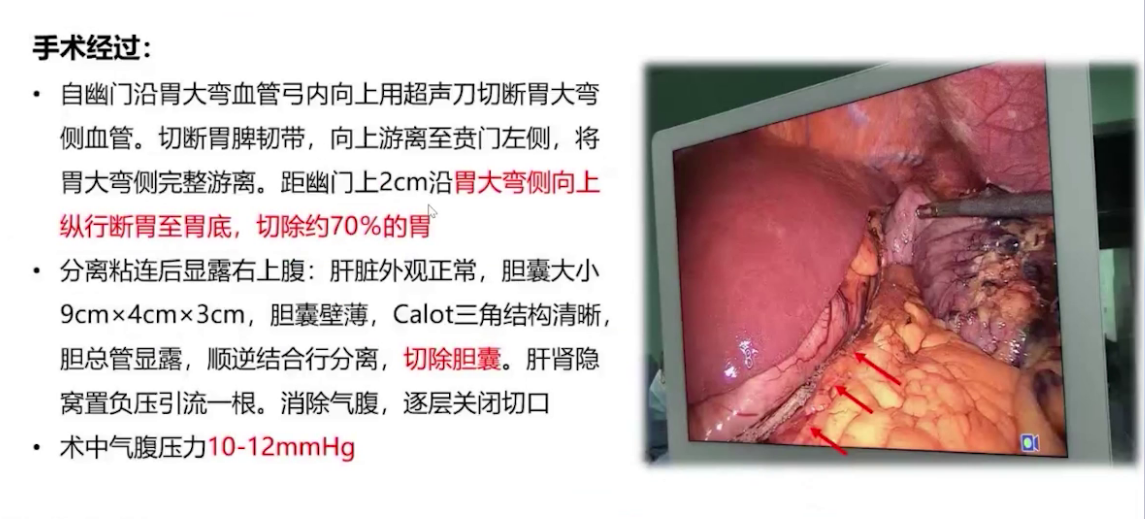
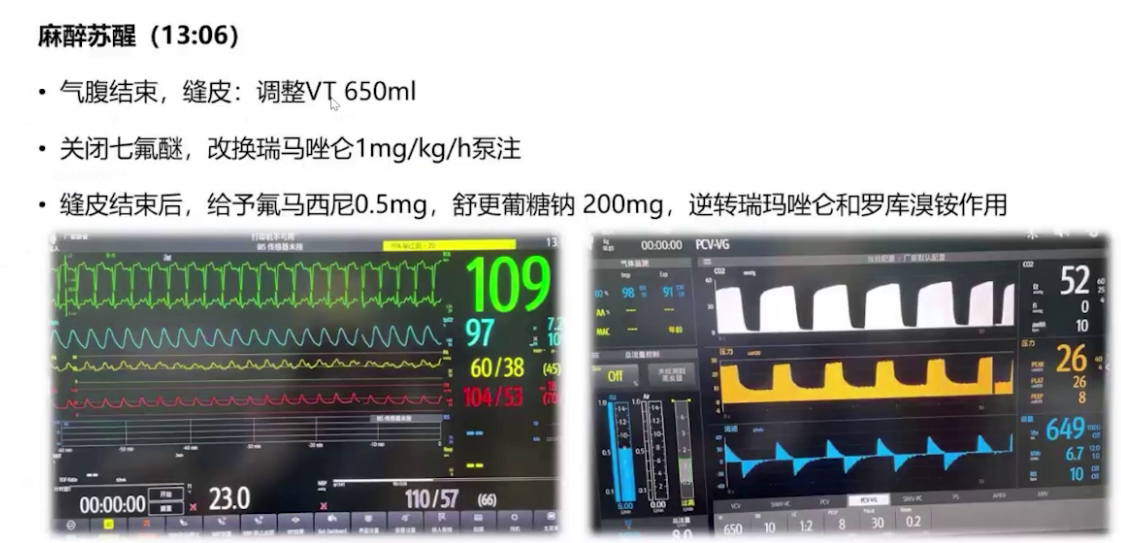
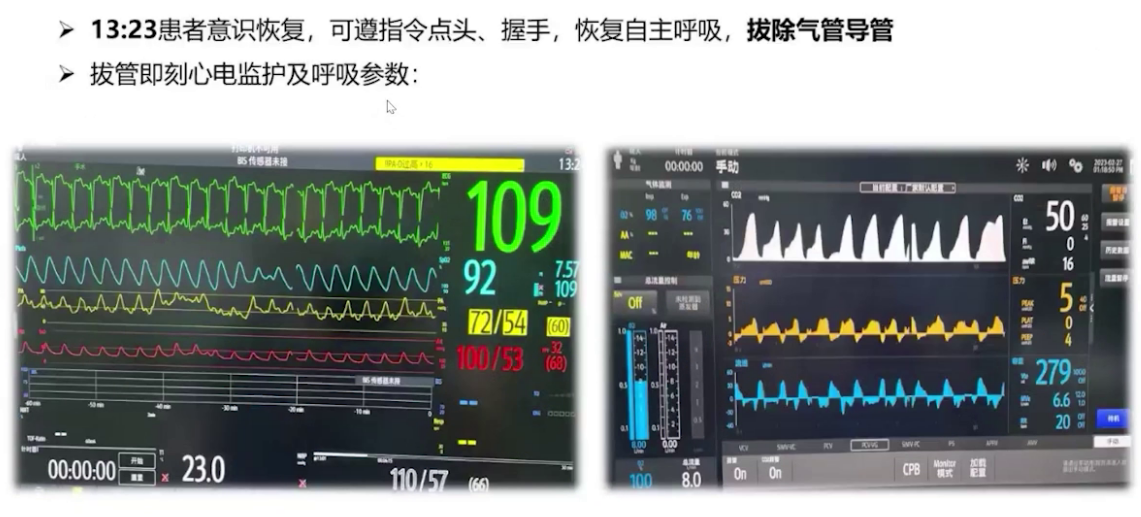
2.麻醉实施:诱导前给予米力农负荷剂量4mg,10分钟内泵注,后以0.375μg/kg/min速度持续泵注,肺动脉收缩压从48mmHg降至41mmHg。麻醉诱导使用瑞马唑仑、瑞芬太尼、舒芬太尼、罗库溴铵和利多卡因,气管插管后行双侧腹横筋膜阻滞和腹直肌后鞘阻滞。呼吸机设置为压力控制容量保证模式,潮气量500ml,频率14次/分,PEEP初始设为0。插管后肺动脉压升至60mmHg,接入一氧化氮10ppm持续吸入。术中维持纯氧七氟烷0-0.8-1.0 MAC,间断分次添加罗库溴铵,限制补液,持续泵注米力农并将NO吸入浓度从10ppm升至20ppm,调整去甲肾上腺素泵注速度维持体循环压力,微调呼吸机参数并间断手法肺复张。手术顺利,行胃大弯侧向上吻合,切除70%胃及胆囊,气腹压力10-12 mmHg 。术中血气分析显示气腹建立过程中二氧化碳分压高,最高达62mmHg,氧合不理想,电解质及酸碱平衡调控尚可。气腹结束后调大潮气量通气,关闭气腹,改用瑞马唑仑泵注,手术结束后给予氟马西尼、舒更葡糖钠逆转药物作用。患者1点23分意识恢复,拔除气管导管,虽术中采取多种降肺动脉压措施,但压力未达术前期望,好在未出现右心力衰竭等急性表现。



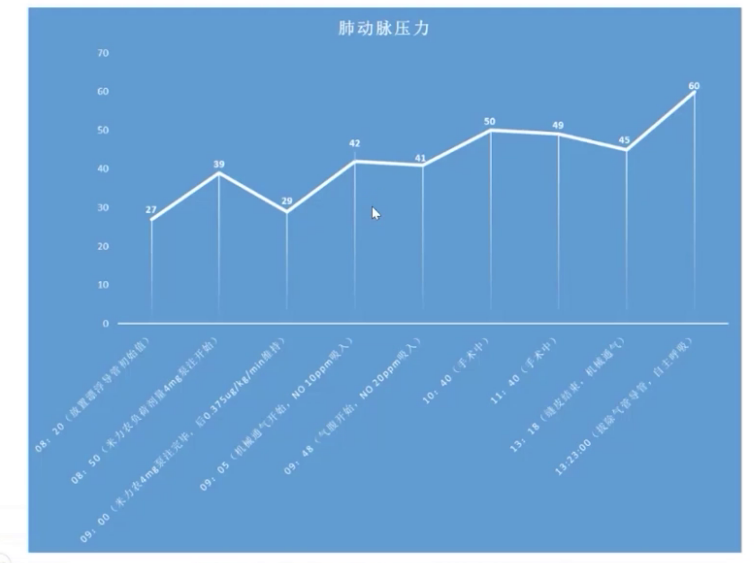
术后管理
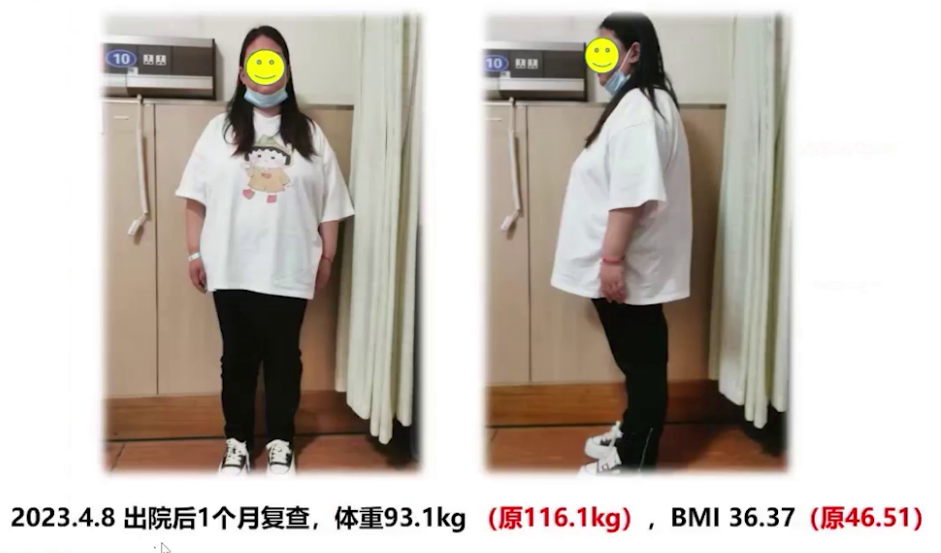
术后患者送至PACU,面罩吸氧后动脉血二氧化碳分压升高,改用无创正压通气治疗。苏醒室观察1小时后,由住院医生护送,持续吸氧监护转运至ICU。术后采用高流量吸氧、雾化吸入、抗感染等治疗,3月1日从监护室转回内分泌科病房,继续对症和支持治疗,3月8日出院。术后随访显示各项指标好转,胸部CT炎症减轻,心电图仅遗留窦性心律和完全性右束支传导阻滞,心脏超声显示房室内径缩小,肺动脉压力从重度降至中度,三尖瓣反流从重度降至轻度,少量心包积液,体重下降23kg,BMI降至36。
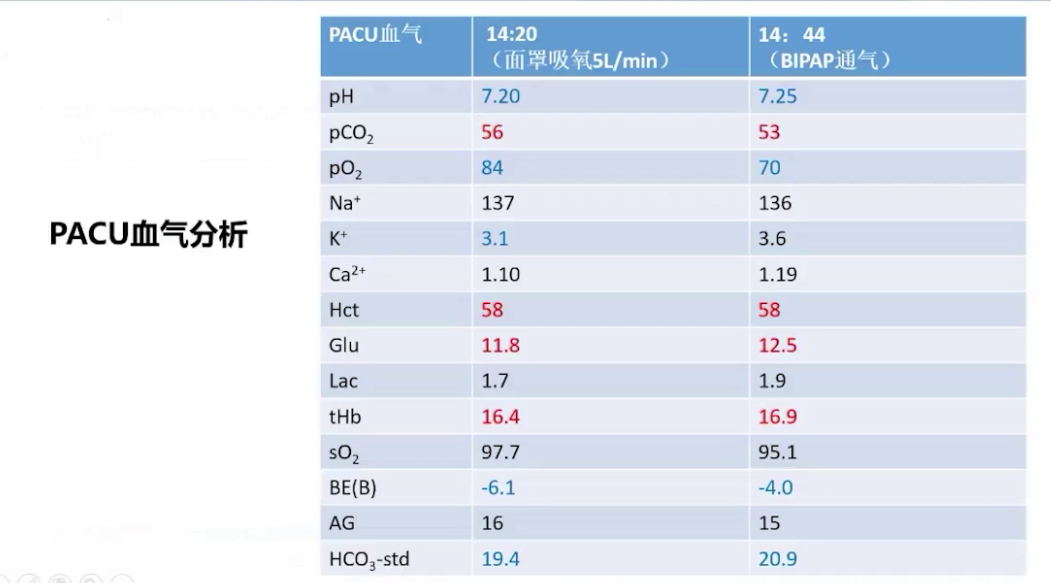
查看更多
专家点评
本病例是一位33岁女性减重手术患者,其核心特殊性在于合并了重度肺动脉高压,这使其区别于常规的肥胖减重患者。
针对该患者的术前评估,需要在肥胖患者的常规评估基础上,特别聚焦于重度肺动脉高压的专项评估,包括:评估患者已存在的呼吸功能不全、右心功能不全的典型症状与体征;通过右心导管检查精准测定肺动脉压力,并与超声心动图结果相互印证,同时明确右房压、混合静脉血氧饱和度等关键指标;通过六分钟步行试验评估其运动耐力及氧合变化,辅助进行风险分层;以及持续监测BNP等反映心功能的核心生化指标,为风险预判提供依据。
在围术期管理方面,核心策略是围绕“重度肺动脉高压管控”展开,并兼顾肥胖患者的常规管理要求。在血流动力学稳定方面,通过右颈内静脉漂浮导管监测中心静脉压,目标维持在8-12cmH₂O以优化前负荷,术中容量管理基本合理;使用米力农以维持右心收缩力;应用西地那非等药物尝试降低肺血管阻力。通气管理上,采用了肺保护性通气策略。此外,也实施了选择短效麻醉药物、术后多模式镇痛等常规管理。
然而,本次管理也存在一些不足之处。首要问题是肺血管阻力控制未达预期目标,术中肺动脉压力不降反升,未能实现肺血管阻力与体循环阻力比值小于0.5的理想状态。其核心原因可能在于术中氧合持续偏低、存在二氧化碳潴留和酸中毒,加之患者肺血管可能存在器质性改变,使得药物效果有限。同时,由于腔镜手术中驱动压已较高,无法通过增加潮气量来改善通气,进一步加剧了问题。其次,体循环压力的维持也不理想,所使用的去甲肾上腺素浓度相对偏低。最后,在监测方面存在缺陷,虽然放置了Swan-Ganz导管,但未持续监测心输出量指数,导致关键数据缺失,影响了临床决策的完整性。
总结而言,本例患者虽最终转归良好,属于成功病例,但仍凸显了核心临床难点:对于合并重度肺动脉高压及右心功能不全的患者,其围术期管理仍是麻醉领域的重大挑战。即使是经验丰富的减重手术麻醉团队,在面对此类高危患者时,在系统性靶向管理,尤其是循环与通气的协同管控方面,仍有优化空间。对于此类患者,需进一步完善围术期监测体系,优化血管活性药物方案,并精准平衡通气需求与肺高压管控,从而更好地降低围术期风险。