查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





美国时间2021年2月5日,美国FDA宣布:第4款CAR(嵌合抗原受体)-T细胞疗法获批上市!
此次批准的是百时美施贵宝(BMS)旗下的Juno Therapeutics公司研发的CAR-T细胞疗法——Breyanzi(lisocabtagene maraleucel),用于治疗至少2种其他全身疗法后无应答、或治疗后复发的某些大B细胞淋巴瘤成人患者。
图片来源:FDA官网
作为FDA第4款CAR-T细胞疗法,此次获批的Breyanzi其适应证也是血液肿瘤。作为最常见的恶性淋巴瘤,弥漫性大B细胞淋巴瘤(DLBCL)患者有接近30%~40%在一线治疗后无法缓解,或者复发,因此,对于这一类患者来说,新的治疗方式尤为迫切。
而新获批的Breyanzi则是基于TRANSCEND NHL 001临床试验的最终结果,在接受Breyanzi治疗的可以评估的超过250多名一线治疗无效或复发的DLBCL患者中,有54%的患者达到完全缓解,这个治疗的数据是相当不错的。
而在副作用方面,Breyanzi治疗也和其他的CAR-T细胞疗法一样,可能会产生细胞因子风暴和神经毒性的风险,所以在接受Breyanzi治疗的时候,需要密切关注患者的生命体征,不过从目前来看,CAR-T细胞疗法的副作用可以通过积极的专业医疗人员的介入,降低危害。
在2017年10月份,FDA批准了全球首款CAR-T细胞疗法的上市,此后的12月,FDA批准了第二款CAR-T细胞疗法的上市,但是在此后时隔近三年,我们才在2020年的7月份迎来了第三款CAR-T细胞疗法的上市,然而幸运的是,第四款CAR-T细胞疗法并没有让我们等太久,在短短的几个月之后的今天,我们就迎来了第四款CAR-T细胞疗法的上市,我们可以一起来看看已经上市的CAR-T的细胞疗法的信息:
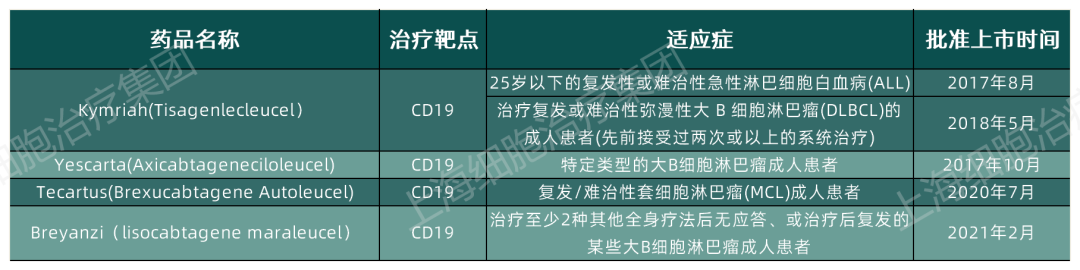
截至今日,FDA一共批准了4款CAR-T细胞疗法上市,这些细胞疗法都是针对血液肿瘤,并且都是以CD19为治疗靶点,取得了相当好的治疗效果。而正是因为如此,CAR-T细胞疗法也被人们寄予厚望,希望其在肿瘤治疗领域发挥更强大的治疗效果。
我们在全球临床试验中心中以“CAR-T”和“肿瘤”为关键词进行临床试验的搜索,一共可以搜索到798项相关的临床研究,从研究数量上来看,中国的CAR-T细胞疗法已经超过美国,成为如今世界上CAR-T细胞疗法临床研究数量最多的国家。
与此同时,在对这798项试验进行2期和3期临床试验的筛选,目前也有近300项的CAR-T细胞疗法的临床研究,这里面的很多CAR-T细胞疗法都有了相当长的研究时间,并且这些CAR-T细胞疗法并不仅仅是针对血液肿瘤,还有很多是针对实体肿瘤的研究。
在对这些2期和3期的临床试验进行分析的时候,我们就发现多种实体肿瘤也在进行CAR-T疗法的治疗,包括:宫颈癌、食道癌、卵巢癌、子宫内膜癌、乳腺癌、胰腺癌肝转移、结直肠癌等,这些临床研究也在持续招募当中。
伴随着美国CAR-T细胞疗法的上市,全球范围内尤其是中国的CAR-T细胞治疗审批也将持续跟进。中国的CAR-T细胞治疗公司也在不断研发新的治疗技术,相信如此多的临床研究进入2期和3期,2021年,我们或将有望迎来CAR-T细胞疗法的大暴发,并且在未来的2~3年内,我们将看到越来越多的CAR-T细胞疗法获批上市,帮助更多的患者对抗癌症。
本文首发于生物世界公众号
查看更多