查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





导读:围术期免疫治疗重塑了早期可切除非小细胞肺癌(NSCLC)的治疗格局,免疫新辅助、辅助、新辅助+辅助三明治治疗模式成为患者的新选择;2024年12月基于KEYNOTE-671研究,帕博利珠单抗围术期三明治治疗模式(新辅助+辅助治疗)获国家药品监督管理局(NMPA)批准上市,为患者带来新的希望;随着围术期免疫治疗的广泛应用,如何进一步优化免疫策略为更广泛的患者带来更多获益成为临床热点;本文就2025欧洲肺癌大会(ELCC)中围术期免疫治疗相关的研究热点进行系统梳理。
辅助免疫治疗最佳时长探索
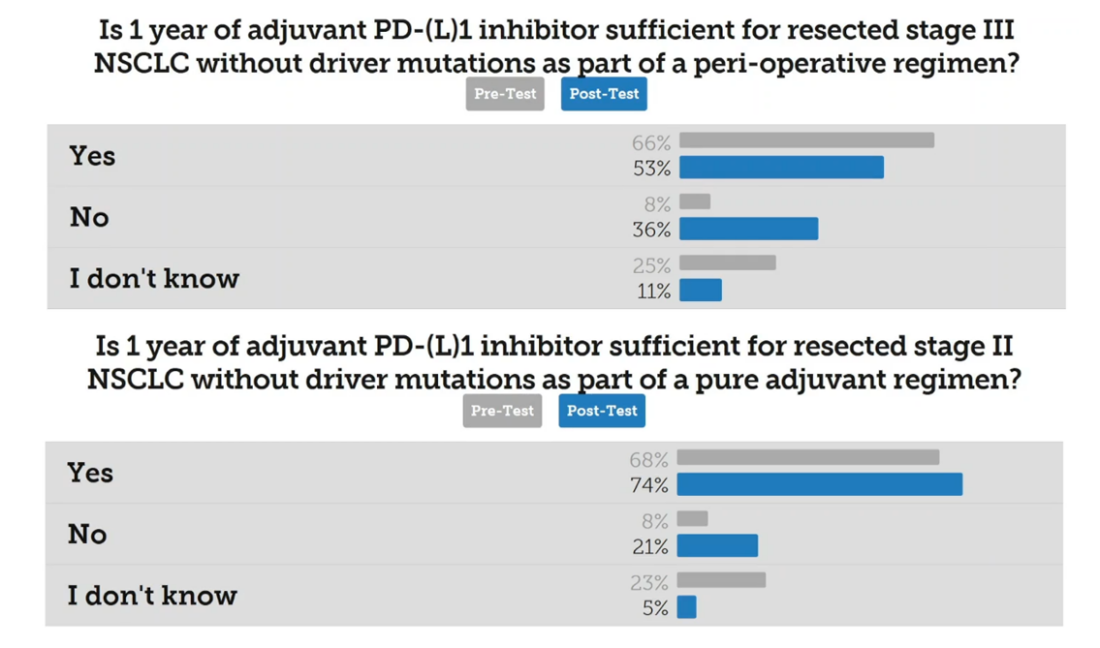
辅助免疫治疗的最佳时长是临床讨论的热点话题,目前关键Ⅲ期研究中辅助免疫治疗多为1年。2025 ELCC的争议话题讨论板块针对可手术Ⅱ期和Ⅲ期NSCLC患者单纯辅助模式或三明治模式中辅助免疫治疗时间为“尽可能长”还是“有限时间”进行了辩论并投票1,部分学者认为“辅助免疫治疗时长仅1年不够,需要尽可能长”,主要基于术后2年的复发风险最高,三明治免疫治疗中辅助治疗阶段具有一致获益,免疫长期治疗的安全性可控,且基线高复发风险患者和术后或辅助化疗后ctDNA持续阳性的患者可能需要更长时间的辅助治疗。而认为“辅助免疫治疗时长是有限的”则主要基于:目前尚无直接证据可以确定辅助免疫治疗的最佳持续时间,在没有前瞻性数据之前,医生可选择最方便、毒性最小和最经济的治疗方案。第二轮投票结果显示:对于Ⅱ期患者,74%的医生认为纯辅助免疫模式中1年辅助治疗足矣,而对于Ⅲ期患者,53%的医生认为三明治模式中1年辅助免疫治疗足矣。
新辅助免疫治疗对手术的影响探究
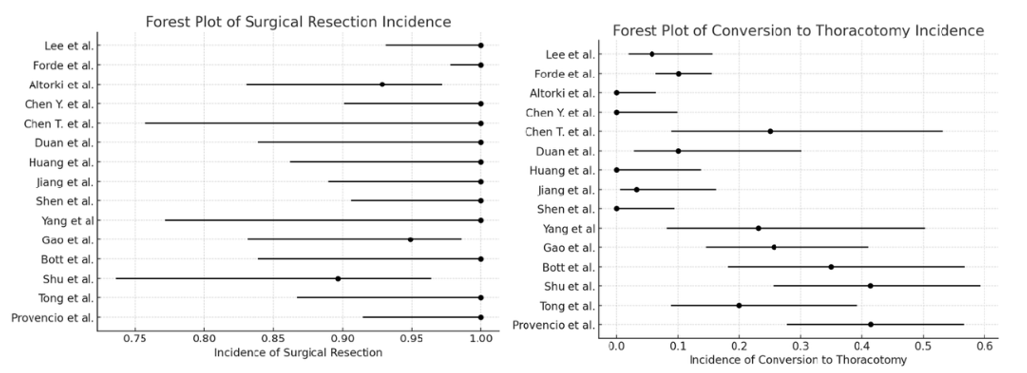
关于新辅助免疫治疗是否会增加手术复杂度,2025 ELCC 中Aigner Clemens 教授2认为新辅助免疫治疗是安全可行的,长期疗效优异,但新辅助治疗后手术比单纯手术更具挑战性,可能出现胸膜/纵隔组织瘢痕和纤维化以及淋巴结肿大等,同时需要注意免疫相关不良反应(irAE)管理,对于边缘可切除患者,可先行新辅助免疫治疗再重新评估可切除性。此外,纳入15项研究的荟萃分析(meta分析)显示,新辅助免疫化疗治疗安全可行,手术切除率较高(98.96%),不同研究至手术时间、手术时长和出血量结果一致性较高,但在微创手术率和开胸手术转化率方面异质性较高3。对于手术复杂性的生物标志物(biomarker)探索也有新发现,回顾性研究显示,基于淋巴结分期、淋巴结应答和程序性死亡受体配体1(PD-L1)表达水平生成的加权风险评分4可预测新辅助化疗免疫治疗后肺切除手术的复杂度。
围术期免疫治疗临床终点的选择
无论从审评或研究设计角度,总生存期(OS)是最能代表NSCLC患者真实获益的金标准,也是最可靠的临床研究终点;病理完全缓解(pCR)是目前讨论比较多的替代终点,回顾性队列研究显示,新辅助免疫治疗后达到pCR的患者仍有一定复发风险5,pCR≠治愈,患者仍需要严格监测。此外,有meta分析显示6,在结局水平,达到pCR和主要病理缓解(MPR)患者的无事件生存期(EFS)/OS更好,但在试验水平,pCR/MPR与生存终点的相关仍不充分,不足以支持两者作为早期NSCLC免疫治疗的完全替代终点常规应用。随着新型治疗手段的不断涌现,患者更加追求“有质量”地活着,生活质量相关结局指标越来越受到重视,至生活质量明确恶化时间(TTD)是否会成为新的关键终点?7 肺癌患者的社会和情感方面存在未被满足的需求,健康相关生活质量(HRQoL)评估有重要意义,但其在酪氨酸激酶抑制剂(TKI)或免疫检查点抑制剂(ICI)研究中作为次要终点评估的比例仅52%;TTD在一些肺癌研究中已作为次要或探索性终点应用,可根据研究问题和预期效果进行量身定制,是有前景的终点,但同时仍需要对患者报告结局(PROs)的解释进一步进行教育或支持。除OS以外,pCR/MPR/EFS等疗效终点的标准化评估也是亟待解决的问题,DATECAN倡议8是针对早期NSCLC 随机对照试验(RCT)的关键疗效终点标准化定义提出的第一个国际性、多步骤共识过程,该倡议将有利于保证不同研究的同质性,提高研究设计和报告的质量。
图3.试验水平,pCR/MPR与EFS或OS相关性仍不足
围术期免疫三明治模式 vs 新辅助免疫模式孰优孰劣
何为围术期免疫治疗的最佳模式目前仍不明确。2025 ELCC公布的一项真实世界回顾性研究发现9,与新辅助免疫治疗相比,围术期免疫三明治模式可显著提高可切除ⅠB-ⅢB NSCLC患者的生存预后,非pCR患者可能从三明治模式中获益更多。对5项围术期免疫治疗研究的个体患者数据(IPD)进行分析发现10,基于新辅助治疗后病理缓解状态的治疗具有一定的价值,为适应性辅助治疗策略提供参考,辅助ICI治疗在pCR患者中可能是非必须的,对于未达到MPR的患者则可能需要免疫“加法”策略。治疗依从性方面,纳入30项前瞻性RCT研究的meta分析11发现,围术期三明治模式中不同治疗阶段的依从性与对应单纯新辅助或辅助治疗的依从性相似。
图4. 围术期免疫三明治模式(PT) vs新辅助免疫治疗模式(NT)可显著提高可切除ⅠB-ⅢB NSCLC患者的生存预后
目前围术期免疫治疗有三种治疗模式,结合本次ELCC公布的数据及您的临床经验,您如何看待这三种治疗模式?
马海涛教授
苏州大学附属第一医院

对于外科医生来讲,我们一般会根据患者的具体情况,从以下角度权衡治疗模式的选择。
第一,对于新辅助免疫治疗,会优先考虑需降期或需要提高R0切除率的患者,若肿瘤体积大、侵犯关键结构(如血管、主支气管),或存在多站淋巴结转移(如N2),新辅助免疫联合化疗可能提高R0切除率。在新辅助治疗过程中,需要严格监测irAEs,比如术前每2周评估免疫相关毒性(如肺功能、心肌酶谱等),避免AE导致手术延迟。若新辅助后肿瘤缩小,优先选择胸腔镜/机器人手术,减少创伤,加快术后恢复。
第二,对于辅助免疫治疗,优先考虑术后高危患者,如淋巴结阳性(N1/N2)、脉管癌栓、胸膜侵犯,或切缘接近(<1mm)。新辅助治疗禁忌的患者我们也会考虑进行辅助治疗,如合并活动性自身免疫病、严重心肺功能不全,无法耐受术前新辅助治疗。辅助免疫周期通常1年,临床上也需平衡长期毒性与复发风险,未来需要探索biomarker指导辅助治疗。
第三,三明治模式是新辅助+辅助治疗,机制上应该是新辅助和辅助治疗的优势集合,能不能取得1+1>2的效果,当前的一些数据,KEYNOTE- 671, CheckMate-77T,AEGEAN,Neotorch,RATIONALE-315确实显示出,三明治模式可以给患者带来生存获益。不仅如此,多项探索性研究,无论是去年公布的 CheckMate-77T vs CheckMate-816*,还是今年ELCC公布的真实世界回顾性研究,或是5项围术期免疫治疗研究的个体患者数据分析都显示,相比于新辅助免疫治疗,三明治模式或许可以给患者带来更多的获益。当然,未来需要三种模式的头对头研究给出确定答案。
最后,临床上,外科医生不是单打独斗的,我们会与肿瘤科,呼吸科,病理科通过多学科协作给患者选择最适合的治疗,最终目标是通过个体化治疗,在确保手术安全性和根治性的基础上,降低复发风险。
作为外科医生,结合本次ELCC公布的数据和您的临床经验,您认为新辅助治疗会对手术产生何种影响?
马海涛教授
苏州大学附属第一医院

对于不同分期的NSCLC,新辅助对手术的影响可能不同。新辅助免疫治疗在NSCLC中的应用正逐渐改变不同分期患者的手术策略和预后。
对于可切除的II期患者,KEYNOTE-671研究亚组分析显示,围术期免疫治疗可以给II期患者带来EFS的获益。 AEGEAN和RATIONALE-315手术结果也显示,相比于新辅助化疗,新辅助免疫治疗并没有影响II期患者手术的实施,这提示我们,对于II期患者,新辅助免疫治疗相比于新辅助化疗,似乎可以在提升患者预后的同时不会增加患者的手术风险。对于外科医生,我们还非常关注的一个点是,如果患者不需要任何新辅助治疗就可以直接手术,其实是可以保证100%的手术R0切除,那新辅助免疫治疗相对于不进行新辅助治疗直接手术,是否会增加手术风险?是否可以缩小手术范围,减少术后疼痛及呼吸功能损失,提升生活质量?如果有数据能回答这个问题,将会给临床带来非常有价值的参考。
对于可手术III期患者,新辅助免疫治疗证据非常充分,多项研究都显示,新辅助免疫治疗及三明治的围术期免疫治疗能给III期患者带来生存获益。且与单纯新辅助化疗相比,新辅助免疫联合化疗在不影响手术方式选择、不延迟手术、不延长住院时间的同时,可以提高 R0 切除率和淋巴结降期比例。所以,对于可手术III期患者使用新辅助免疫治疗证据比较充分,可以给临床非常有力的参考。对于临界可切/不可切的NSCLC,也有证据显示,新辅助免疫治疗可以使不可切的患者转化为可切除状态,新辅助治疗非常有意义的点之一就在于手术降期转化,我们也期待更多数据的公布可以使新辅助免疫治疗惠及更多的患者。
本次ELCC公布的meta分析也显示,新辅助免疫联合化疗安全可行。当然,我们在进行新辅助免疫治疗时需要密切关注患者的情况,MDT合作,及时调整治疗策略,处理irAE等,使新辅助免疫治疗对手术不良影响最小化。未来需通过个体化biomarker、优化治疗周期及多学科协作,使患者生存获益最大化并保障患者生活质量。
您认为围术期研究应该如何进行终点的选择?
李高峰教授
云南省肿瘤医院

围术期研究的终点选择一直是非常重要的学术和伦理问题,从临床研究评审和疾病治愈的角度而言,OS一直被认为是评估肿瘤治疗疗效的金标准,也是临床研究设计的最终目标,更是我们要持续关注的;pCR等替代终点可能在短期内反应患者的病理缓解情况,但pCR获益不一定转化为EFS和OS获益,可以作为临床终点使用,但无法完全替代OS。
OS 作为临床研究终点的优点在于测量方法简单,可以直接反映生存获益,且数据精准可靠。KEYNOTE系列研究多以OS为研究终点,KEYNOTE-671是目前唯一一个以 EFS和OS为主要终点的NSCLC围手术期治疗研究,坚持付出长期时间的随访作为代价,探索OS作为金标准为临床研究带来的指导意义,开启了围术期NSCLC免疫治疗长期生存探索的新格局,为验证免疫疗法在围手术期治疗价值提供更直接、更有力的证据。
目前,一些新型的研究重点如至生活质量明确恶化时间等,反映了我们对临床研究试验终点设置的思考和改进,具有一定的参考价值,但未来应用还是需要与OS等终点有机结合,兼顾不同获益群体和终极指标改善,做好研究设计,提高研究质量,真正为患者带来更好的治疗选择。
对于早期NSCLC,您认为还有哪些方向值得进一步探索?
李高峰教授
云南省肿瘤医院

肺癌围术期研究的重点应聚焦于个体化治疗、免疫治疗的优化、新型药物的探索以及精准外科技术的结合。通过多学科协作和大规模临床试验,未来有望为患者提供更精准、更高效的治疗方案,显著提升生存获益。
目前围术期研究在biomarker方向的探索仍然需要继续努力,从目前探索中,可以看到持续监测ctDNA清除等能够在一定程度上帮助临床医生做出治疗决策,但是仍然缺乏大样本的验证或是寻找到更优的生物标志物进行患者筛选。另外,随着精准化治疗时代的到来,MDT得到广泛推广与建立,不仅限于阶段性的诊疗,还在于其可以为患者提供全方位的疗效支持。
近年来免疫治疗取得长足进展,已经为早期可手术NSCLC患者带来许多新的治疗选择,未来的重点将是如何进一步优化和升级。优化现有策略,首先,关注biomarker探索,预测新辅助治疗后AE发生或疾病进展的biomarker,可以使临床医生更早的发现和处理相关情况,及时应对,最小化对手术的影响;其次,提升辅助治疗的患者依从性,找到需要持续辅助免疫治疗的患者,或针对不同患者特点制定合理的辅助治疗期限,以患者为中心进行个体化治疗;升级免疫治疗,可以从新辅助治疗和辅助治疗阶段的更多免疫联合策略探索出发,如何结合最新的治疗手段以及抗体偶联药物(ADC)类、程序性死亡受体1(PD-1)/血管内皮生长因子(VEGF)双抗等,为目前治疗应答不佳的患者带来更多选择。
马海涛 教授
苏州大学附属第一医院胸外科首席专家,学科带头人
苏州大学附属第四医院(苏州市独墅湖医院)胸心大血管外科主任,大外科主任
中国医师协会胸外科分会常务委员
中国医药教育协会肺癌医学教育委员会副主任委员
中国医师协会内镜医师分会胸腔镜专业委员会常委
中国医疗保健国际交流促进会胸外科分会常委
中华医学会胸心血管外科肺癌学组委员
CSCO非小细胞肺癌专家委员会委员
江苏省医学会胸外科分会常务委员
江苏省医师协会胸外科分会常务委员
江苏省医师协会肿瘤多学科诊疗专委会副主任委员
江苏省抗癌协会肺癌专业委员会副主任委员
江苏省抗癌协会肿瘤微创治疗专业委员会常委、腔镜学组组长
江苏省医学会肿瘤学分会食管癌学组副组长
江苏省肿瘤防治联盟食管癌专业委员会副主委
中国医师协会《全国医师定期考核胸外科编辑委员会》委员
李高峰 教授
二级教授、主任医师
博士研究生导师、博士后合作导师
云南省肿瘤医院、昆明医科大学第三附属医院 副院长
全国优秀科技工作者、享受国务院特殊津贴专家
全国五一劳动奖章获得者、云南省医学领军人才、云岭名医
云南省有突出贡献优秀专业技术人才、省委联系专家
云南健康卫士、省科协优秀学会工作者
学术任职:中国抗癌协会纵隔肿瘤专业委员会 常务委员、中华医学会胸心血管外科学分会胸腔镜外科学组 委员、中国医院协会医疗联合体工作委员会 委员、全国肺癌MDT专家委员会 委员、胸外科国家级医疗质量控制中心纵隔肿瘤亚专业组 委员、云南省转化医学学会 会长、云南省抗癌协会 副理事长、 云南省医学会胸心血管外科学分会 主任委员、云南省抗癌协会胸部肿瘤微创治疗专业委员会 主任委员、云南省预防医学会 常务理事兼肺癌专业委员会 主任委员等职务
研究方向:胸部肿瘤基础研究及以微创外科治疗为主的个体化治疗
主持国家自然科学基金及科技部国家重点研发项目4项、国际合作研究项目3项、云南省应用基础及重点项目4项 ,在国内、外权威学术期刊发表论文130余篇,主编副主编教材及专著10部 ,研究成果获教育部科技进步二等奖、云南省科技进步一、二等奖等14项。
1. Wakelee H, et al. 2025 ELCC.
2. Aigner C, et al. 2025 ELCC.
3. Bardoni C, et al. 2025 ELCC.#213p.
4. Nardini M, et al. 2025 ELCC.#187O.
5. Lin Y, et al. 2025 ELCC.#212p.
6. Tagliamento M, et al. 2025 ELCC.#150P.
7. Pompili C, et al. 2025 ELCC.
8. Cascetta P, et al. 2025 ELCC.#439p.
9.Fan Y, et al. 2025 ELCC.#149p.
10. Nuccio A, et al. 2025 ELCC.#167p.
11. Guerrera F, et al. 2025 ELCC.#234p.
*非头对头研究不可直接比较,仅供参考
声明:
本资讯由默沙东医学团队编辑提供,旨在用于医学专业人士间的学术交流,请勿随意转发或转载。文中相关内容不能以任何方式取代专业的医疗指导,也不应被视为治疗建议。医学专业人士对文中提到的任何药品进行处方时,请严格遵循该药品在中国批准使用的说明书。默沙东不承担相应的有关责任。
审批号:MI-PD1-7189-CN
Expiration Date:03 Apr 2026
本文由马海涛教授、李高峰教授审校
查看更多