查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





作者:首都医科大学附属北京天坛医院神经病学中心 赵家慧

研究背景
阿替普酶是目前唯一被批准用于急性缺血性卒中治疗的溶栓药物。替奈普酶是一种改良的组织型纤溶酶原激活剂,与阿替普酶相比具有药理方面的优势,例如更长的半衰期和较高的纤维蛋白特异性。在2019年AHA/ASA指南中推荐替奈普酶作为阿替普酶的替代药物。2017年,来自挪威的替奈普酶卒中试验(Norwegian Tenecteplase Stroke Trial, NOR-TEST)作为首个研究替奈普酶的3期优效性试验,发现0.4 mg/kg替奈普酶与0.9 mg/kg阿替普酶在治疗急性缺血性卒中患者中的安全性相似,但未证明阿替普酶的疗效优于替奈普酶。一项荟萃分析通过纳入NOR-TEST与另外4项2期试验(TNK-S2B、Australian TNK、ATTEST、EXTEND-IA TNK)共计1585例患者,虽然没有任何一项试验显示替奈普酶相较于阿替普酶的优效性或非劣效性,但荟萃分析表明,替奈普酶在大血管闭塞患者血管再通治疗中的优效性及3个月后无残疾方面的非劣效性,且未增加症状性颅内出血的发生率或死亡率。然而,此项荟萃分析的患者主要来自NOR-TEST研究,而NOR-TEST研究中大部分患者为轻型卒中患者,因其自然转归较好的特性可能较难证明替奈普酶的优越性。因此,本研究旨在证明在中重度急性缺血性卒中患者中,替奈普酶非劣于阿替普酶。
研究方法
NORTEST 2是一项3期、随机、开放标签、盲法终点、非劣效性研究,在挪威的11家卒中中心进行。NIHSS评分≥6分、发病4.5小时内的急性缺血性卒中患者被纳入本研究,DWI与FLAIR存在错配(mismatch)的醒后卒中患者及接受溶栓作为桥接治疗的患者也被纳入本研究。患者被随机(1:1)分配至替奈普酶组(0.4 mg/kg,一次静脉注射剂量最大为40 mg)和阿替普酶组(0.9 mg/kg,最大剂量90 mg,其中10%的剂量作为初始药量静脉团注,其余90%的剂量静脉滴注1 h)。主要研究终点为3个月时功能结局良好,定义为mRS评分为0~1分;如果卒中前mRS评分为2分,则为恢复至基线水平。次要结局包括治疗后24~48小时内出现的任何颅内出血、症状性颅内出血,3个月时mRS评分,3个月时功能结局不良(mRS评分5~6分或3个月内死亡)。主要神经功能改善定义为24小时NIHSS评分较基线减小4分以上。
本研究为非劣效性研究,非劣效界值定义为3%,主要基于阿替普酶与安慰剂对比治疗效果的绝对差异为8.7%。在NOR-TEST的研究数据中,阿替普酶与替奈普酶在功能结局良好的绝对差异为7.6%。本研究选择更为保守的7%作为阿替普酶与替奈普酶在主要结局中所占比例的绝对差异。本研究最终估计样本例数为1036例。如果主要结局功能结局良好患者的绝对比例(替奈普酶与阿替普酶)的两侧95%CI的下限大于-3.0%,则认为替奈普酶不劣于阿替普酶。
每入组200例患者或15例NIHSS评分>15分的患者后进行安全性评估,若两组间颅内出血比例差异>5%,实验将提前终止,并进一步分析出替奈普酶组中出血风险增加的亚组。
研究结果
本研究从2019年10月28日开始入组,在对前200例患者进行安全性评估时,两组患者的症状性颅内出血比例失衡,替奈普酶组出血事件明显偏多,遂于2021年9月26日提前终止入组。经过分析并未在研究人群中发现出血风险增加的特定亚组。因此本研究的第一部分作为part A在此进行结果展示及分析。
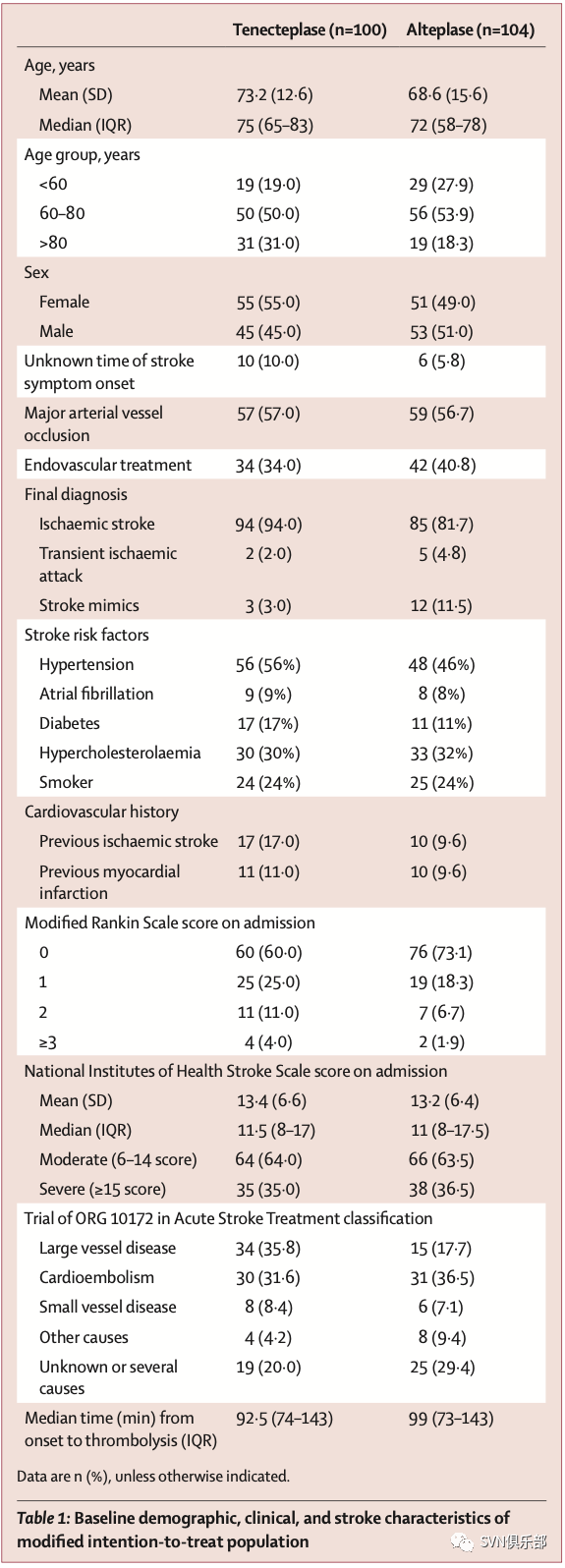
最终,共204例患者被纳入意向性分析(intention-to-treat, ITT),其中替奈普酶组100例,阿替普酶组104例。在单因素分析中,替奈普酶组患者相较于阿替普酶组患者年龄更大,入院时mRS评分为0的比例更低。此外,与阿替普酶组相比,替奈普酶组最终诊断为缺血性卒中的患者比例更高,而诊断为假性卒中的患者比例更低。其他基线特征在两治疗组间无显著差异(Table 1)。
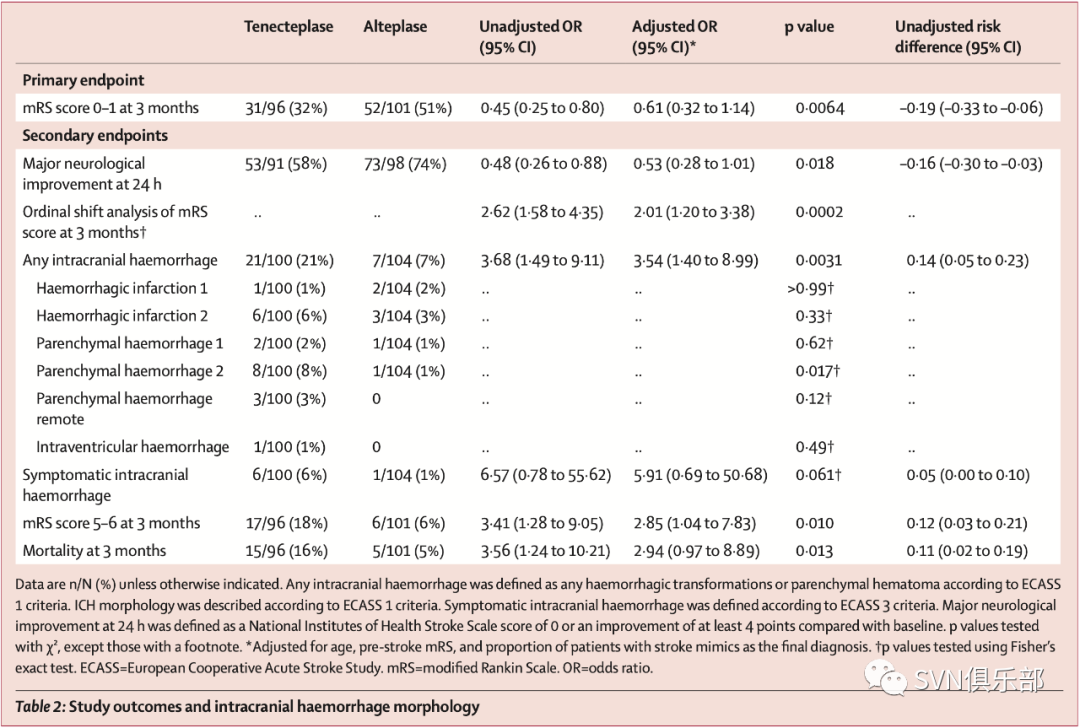
3个月后功能结局良好的患者比例在阿替普酶组较替奈普酶组更高(51% vs 32%, unadjusted OR 0.45 [95%CI 0.25-0.80]; p=0.0064),24小时后的主要神经功能改善比例在替奈普酶组更高(74% vs 58%, unadjusted OR 0.48 [95%CI 0.26-0.88]; p=0.018)。任何颅内出血在替奈普酶组的比例更高(21% vs 7%, unadjusted OR 3.68 [95%CI 1.49-9.11]; p=0.003),症状性颅内出血的患者比例也更多(6% vs 1%, unadjusted OR 6.57 [95%CI 0.78-55.62]; p=0.061)。替奈普酶组3个月后功能结局不良比例更高(18% vs 6%, unadjusted OR 3.41 [95%CI 1.28-9.05]; p=0.010),3个月时死亡率也更高(16% vs 5%, unadjusted OR 3.56 [95%CI 1.24-10.21]; p=0.013)。当校正了年龄、卒中前mRS评分、假性卒中比例的差异后,mRS评分的漂移分析(shift analysis)提示替奈普酶组3个月后功能结局更差(Table 2)。
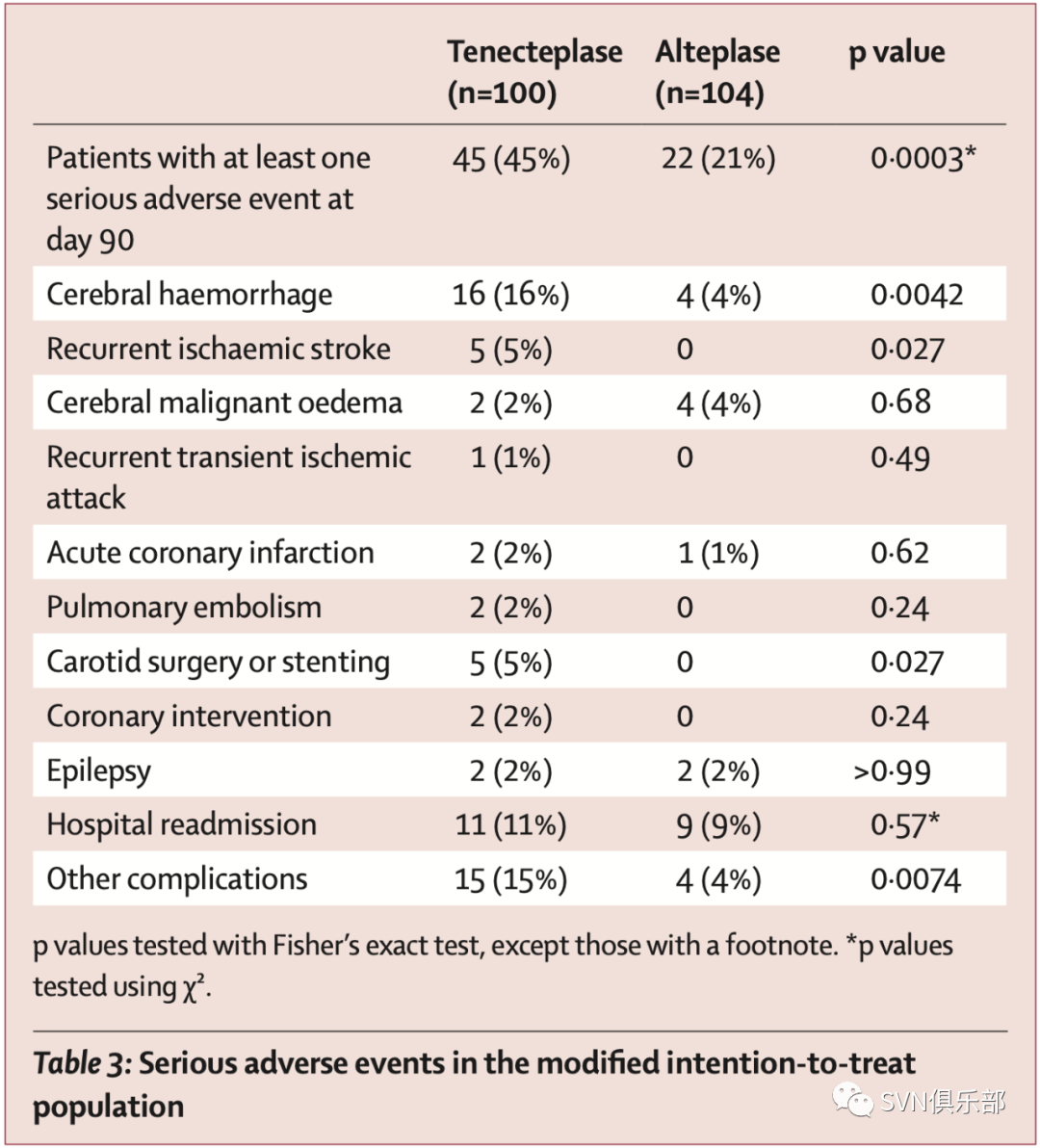
与阿替普酶组相比,替奈普酶组在第90天发生至少1次严重不良事件的患者更多(45% vs 21%, p=0.0003),颅内出血(16% vs 4%, p=0.0042)、复发性缺血性卒中(0 vs 5%, p=0.027)和其他并发症(4% vs 15%, p=0.0074)的比例在替奈普酶组均更高(Table 3)。
研究结论
在这项提前终止的研究中,0.4 mg/kg剂量的替奈普酶相较于0.9 mg/kg标准剂量使用的阿替普酶的安全性和功能结局均较差。本研究未能证明在中重度急性缺血性卒中患者中,0.4 mg/kg的替奈普酶非劣于0.9 mg/kg的阿替普酶。未来的卒中试验应进一步开展更低剂量的替奈普酶与阿替普酶在中重度卒中患者中的比较研究。
01
本研究非劣效界值为3%,是否过于严格,是否会对结果产生影响?
常规确定非劣效界值必须建立在临床判断和统计合理的基础上。在统计方面,非劣效界值应小于对照疗效的95%可信区间下限,以保证新治疗的疗效大于最低对照疗效。这里的对照疗效指该非劣效性试验中的疗效,但因为界值是提前确定的,所以一般使用对照药物既往的安慰剂对照试验中的疗效,由此设定的界值称为M1。然而,在临床判断方面,非劣效界值必须小于最小的有临床意义的差值M1。所以试验选择的界值往往比上述界值更小,即基于临床判断的最大的临床可接受的非劣效差异。非劣效界值一般取M1的一半,由此设定的界值称M2。
本研究非劣效界值的选择基于一项阿替普酶和安慰剂疗效对比的既往研究,其中阿替普酶实现功能独立的比例相较于安慰剂增加8.7%,95%CI下限为6%(M1)。选择95%CI下限的一半即3%(M2)作为本研究的非劣界值。一项研究发现非劣性界值定在3%~5%较为合理1,然而实际的临床研究中非劣效价值通常高于此范围,可能因为需要考量可行性。本研究的非劣界值为3%,相对比较严格,因此本研究原本估计的样本量也较大,为1036例。
02
若证明了非劣效性,是否可以用本研究数据进一步证明优效性?界值是否一样?
本研究未证明非劣效性。如果非劣效性被证明后,可开展证明优效性的研究,但界值不同。本研究中所提出的当两侧95%CI的下限大于0时即可被证明优效性,即替奈普酶在改善3个月后功能结局方面优于阿替普酶。
03
本研究为何选择0.4 mg/kg作为替奈普酶剂量?
NOR-TEST研究中比较了替奈普酶0.4 mg/kg与阿替普酶标准剂量的疗效,虽未证明其优效性,但证明了安全性相似,本研究主要在NOR-TEST研究的基础上,设计了非劣效性研究。在急性心肌梗死中,替奈普酶0.5 mg/kg是标准剂量,但这种剂量在卒中患者中可能是有害的。根据阿替普酶的使用经验,将用于心肌梗死治疗的剂量降低20%用于卒中可能是合理的,即尝试在卒中患者中应用0.4 mg/kg的替奈普酶。在2020年国际卒中大会(ISC)上,EXTEND-IA TNK Part 2的结果在JAMA同期在线发表。该研究结果提示,在颅内大血管闭塞缺血性卒中患者中,与0.25 mg/kg相比,在取栓前使用0.4 mg/kg的替奈普酶并未显著改善脑灌注。更低的替奈普酶剂量是否更具优势?未来还需要更多高质量的证据来回答这个问题。
04
如何解释Table 2中的“unadjusted risk difference”值?
Risk difference(RD)指两组的绝对差异,表示与对照组相比,治疗组效应减少或增加的绝对值。与相对效应值(如优势比 [odds ratio, OR])相比,绝对效应值更具有临床意义,特别是当某一结果发生率较低时。因为无论OR降低多少,若RD较低,意味着实际效应还是很低,此时OR无明显意义。在本研究中RD是用于与非劣效界值作比较的,主要结局指标中,RD的95%CI下限为-0.33,远大于非劣效界值。

来源:SVN俱乐部
转载已获授权,其他账号转载请联系原账号
最新指南 | 2022 AAN实践指南:症状性颅内大动脉粥样硬化性卒中预防
【PDF下载】急性脑梗死缺血半暗带临床评估和治疗中国专家共识
Neurology:中年时期进行中到剧烈运动有益于晚年的脑血管健康
查看更多