查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





近日,顶级医学期刊《新英格兰医学杂志》(NEJM)就nerandomilast,一种新型的口服选择性PDE4B抑制剂,治疗特发性肺纤维化(IPF)的Ⅲ期临床试验——FIBRONEER-IPF研究的52周结果发表文章《Nerandomilast in Patients with Idiopathic Pulmonary Fibrosis》1。文章指出,FIBRONEER-IPF研究是IPF领域近十年来首个达到研究终点的Ⅲ期试验,研究结果表明,在52周的治疗时间内,nerandomilast组较安慰剂组用力肺活量(FVC)下降幅度更少,且nerandomilast具有可接受的安全性。

FIBRONEER-IPF(NCT05321069)是迄今为止IPF领域已达研究终点的规模最大的Ⅲ期临床研究1-6,共计纳入来自全球30多个国家和地区、332个中心的1177名IPF患者,按照1:1:1的比例随机接受nerandomilast 9mg、18mg或安慰剂每日两次治疗,旨在评估nerandomilast单药或与背景抗纤维化药物联合治疗IPF患者在至少52周时的有效性和安全性1。

R, 根据背景抗纤维化药物使用情况(尼达尼布/吡非尼酮vs无)进行分层随机化。*每12周进行一次访视,直到最后1例患者完成52周的治疗。
图1. FIBRONEER-IPF研究设计无论是否接受背景抗纤维化治疗,患者的基线人口统计学特征相似1;但疾病特征方面,接受背景抗纤维化治疗的患者在基线时病程更长、疾病更严重7。
FIBRONEER-IPF研究纳入了年龄≥40岁,FVC占预计值%≥45%,一氧化碳弥散量(DLco)占预计值%≥25%的IPF患者1。
与以往的IPF临床试验2,3相比,本研究的年龄和肺功能纳入标准涵盖了更广泛的患者群体,年龄和FVC未设置上限,这可能更能代表现实世界中的IPF患者8。
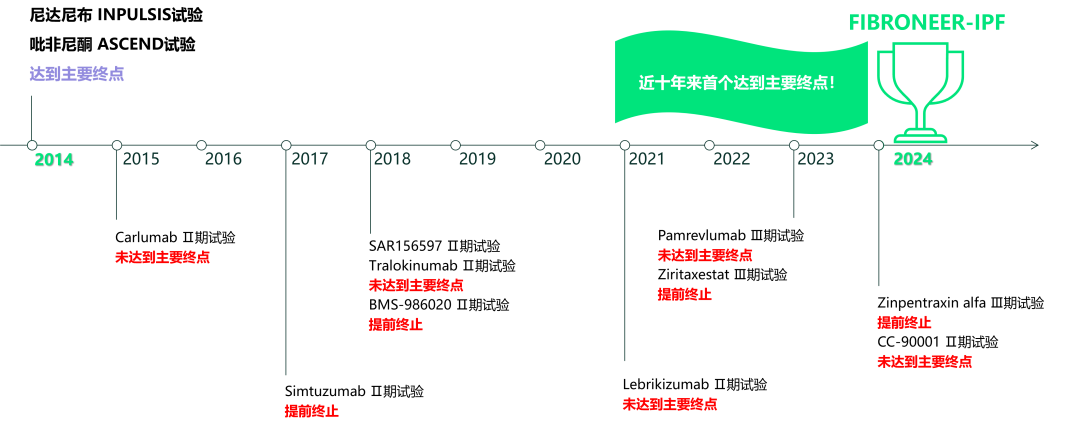
图2. 近十年来,IPF新药研发进展1-6
1)总体人群中,治疗第52周时,与安慰剂组相比,nerandomilast两种剂量组均显著减少了FVC绝对值(mL)的下降:nerandomilast 9mg组FVC绝对值的下降减少了44.9mL(95% CI:6.4,83.3;P=0.02),nerandomilast 18mg组FVC绝对值的下降减少了68.8mL(95% CI:30.3,107.4;P<0.001)1。

图3. 第52周时,总人群FVC(mL)较基线的变化
2)总体人群中,治疗52周内,nerandomilast两种剂量组FVC绝对值在治疗早期就呈现出较安慰剂组更缓慢的下降趋势,且在整个治疗期间,下降速度始终低于安慰剂组7。
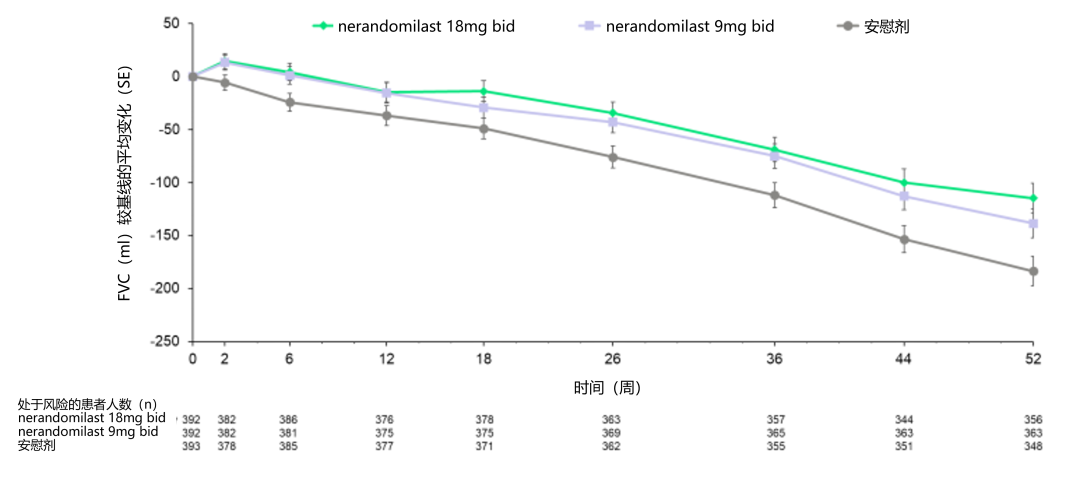
图4. 52周内各治疗组FVC曲线的变化
3)亚组分析结果显示,治疗第52周时,与安慰剂组相比,无背景抗纤维化治疗、nerandomilast联合尼达尼布背景治疗、nerandomilast 18mg联合吡非尼酮背景治疗组的FVC绝对值的下降均有减少1。
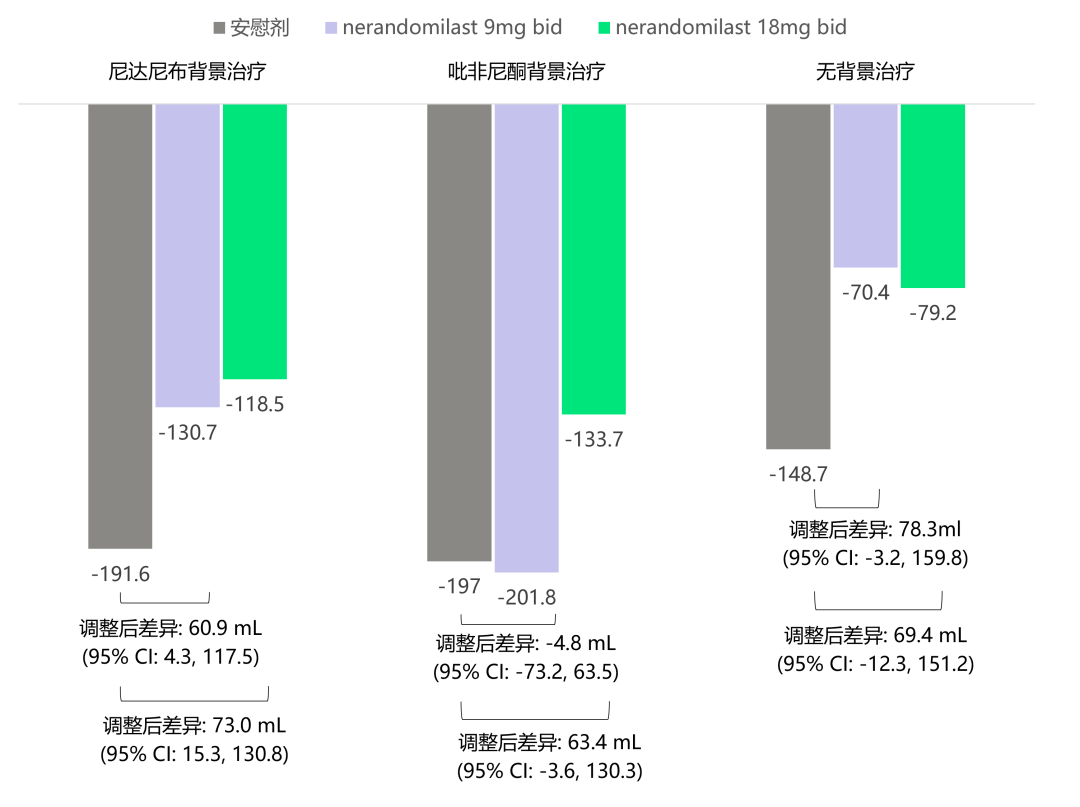
图5. 第52周时,是否接受背景抗纤维化治疗亚组FVC(mL)较基线的变化
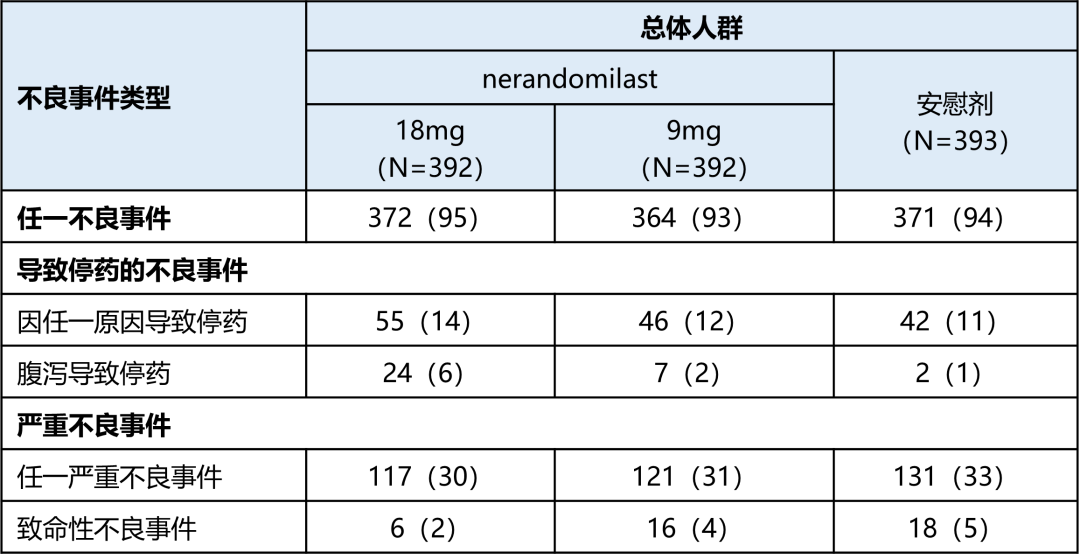
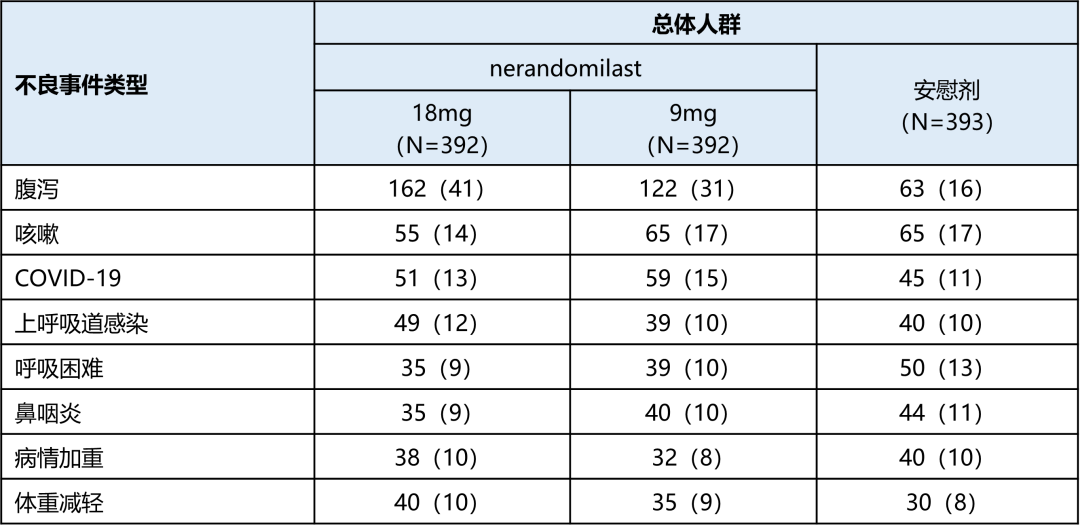
表2. 总体人群中各常见不良事件(定义为发生率≥10%)汇总(n,%)
Nerandomilast作为一款治疗IPF的创新药物,在临床试验中展现出了令人鼓舞的疗效和良好的安全性,为IPF患者的治疗开辟了新的方向,期待未来nerandomilast能够产生更多亮眼的数据,并最终转化为患者的长期获益,早日造福中国IPF患者。
参考文献
仅供相关医药专业人士进行医学科学交流
PART
↓↓↓
查看更多