查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





王贵强 教授
北京大学第一医院感染疾病科暨肝病中心主任
2022年5月16日,北京医学会感染病学分会2022年第一次学术会议在线上召开。北京大学第一医院感染疾病科王贵强主任围绕“发热伴血小板减少综合征”(SFTS)进行了详细介绍。
王贵强教授首先谈到,《发热伴血小板减少综合征经接触传播预防控制要点》发布于2011年,新版诊疗指南已在筹备制定中,将于近期发布。王贵强教授介绍,可引起发热伴血小板减少的感染性疾病很多,包括各种病毒性出血热、立克次体类疾病及严重的细菌或真菌感染。
2006年以前,在浙江、安徽、山东和江苏等地有零星报告不明原因发热伴血小板减少病例。2006年,安徽确诊人粒细胞无形体病聚集性疫情,并且出现人际传播。一例有明确蜱叮咬史的老年女性患者疑似出血热,最终多发出血死亡,其亲属5人及参与抢救的医护人员4人续发感染。2008年2月,原卫生部下发《人粒细胞无形体病预防控制技术指南(试行)》。
2009年底,中国疾病预防控制中心(CDC)在1例湖北病例标本中分离嗜吞噬细胞无形体未果后,开始从病毒方向入手进行病毒分离和鉴定等研究工作,在全球首次发现并最终证实,新型布尼亚病毒感染是导致发热伴血小板减少综合征的病因。
2010年5月,CDC制定了《发热伴血小板减少综合征监测方案》,并在湖北、河南两省开展监测工作,定期通报工作进展,同年9月启动全国22省扩大监测工作。2011年9月,原卫生部派专家组到河南商城调查并启动《发热伴血小板减少综合征防治指南》编写工作,并于2010年10月发布。2011年8月,原卫生部发布《发热伴血小板减少综合征经接触传播预防控制要点》。
发热伴血小板综合征病毒(SFTS virus, SFTSV)按照国际病毒分类委员会(ICTV)最新分类属于布尼亚病毒目白蛉纤细病毒科班达病毒属,分类名为大别班达病毒。SFTS病毒为单股负链RNA病毒,多种哺乳动物细胞对SFTS病毒敏感。病毒接种不同的细胞后,所产生的细胞病变效应不完全相同。SFTS病毒对热敏感,60℃30分钟能够完全灭活病毒,对紫外线、乙醚、氯仿等有机溶剂,以及β-丙内酯、甲醛和常用有机氯消毒剂敏感。
宿主和传染源 家养和野生动物,如牛、羊、猪、狗、鸡和黑线姬鼠等可作为宿主和传染源,患者也可以作为传染源。
传播途径 传播途径包括蜱虫叮咬以及感染者的人-人传播途径(接触患者尿液、粪便、咽喉分泌物、血液、呼吸道分泌物甚至气溶胶等)。我国此前有家庭内接触死者尸体、用品而群体性发病的相关报道。SFTS的人-人传播特点:① 人际传播频繁发生; ② 指示病例绝大部分为死亡病例;③ 指示病例病毒载量高;④ 继发感染者都存在无防护直接接触患者血液和(或)分泌物的情况;⑤ 有医务人员感染。
地理和人群分布 我国20省份均有病例报告,韩国、日本、阿拉伯联合酋长国、印度及美国也有SFTS病例报告。我国SFTS病例主要为山区和丘陵地带的农村,呈高度散发。湖北、浙江及江苏等地的人群SFTSV抗体阳性率分别为6.4%、5.5%~7.1%和0.44%,湖北抗体阳性率高代表可能存在一部分隐性感染人群。SFTSV有6个基因型,不同基因型分布于候鸟迁徙可能存在一定关系。
当前SFTS未列入我国法定传染病,所以关于我国每年的SFTS病例数尚未得到完全统计。根据中国疾病预防控制中心的相关数据,2021年全国年报告SFTS临床和确诊病例数为2681例,死亡133例(另报告疑似病例327例,死亡1例),超过既往最高年份(2016年报告病例2600例,死亡69例),较2020年报告病例数2504例和死亡病例数128例分别增高了7.07%和3.91%。近年来,我国SFTS病例的死亡率维持在5%左右。我国99%病例发生在山东(29%)、河南(28%)、安徽(18%)、湖北(13%)、辽宁(5%)、浙江(3%)和江苏(3%)。
SFTS病例在我国多发于春夏季,疾病的流行季节为3~11月,发病高峰多见于5月前后。国内相关研究显示,随着发病年龄增加,病死率也逐渐增加;SFTS病例职业分布以农民为主(86%)。我国7个SFTS高发省份中,浙江和山东的报告病死率最高,其次为江苏、安徽、湖北、辽宁和河南。死亡病例出现在35岁以上人群,≥80岁人群病死率最高(约11%)。总体来看,男女性别比为1.13:1,男性略多于女性。
当前SFTSV的实验室特异性检测方法主要是核酸检测、抗原检测、病毒分离和抗体检测。
SFTS病程约20天,IgM抗体一般在感染3~5天后出现,IgG抗体出现相对较晚,病原检测以核酸为主。病毒分离在急性期患者的血清中即可检出,核酸检测在感染后即可出现,确切核酸定量检测可动态监测病情变化。
SFTS的发病机制并不完全清楚,可能是由于病毒感染后免疫介导的炎症损伤。脾脏可能是SFTSV的重要靶器官,通过脾巨噬细胞清除SFTSV结合的血小板。此外,病毒诱导产生弥散性血管内凝血或由于严重全身炎症引起的内皮损伤导致外周血小板的消耗。
SFTS的潜伏期为1~2周。患者大多急性起病,发热,体温多在38℃以上,重者持续高热达40℃以上。部分病例热程可长达10天以上。伴乏力、明显纳差、恶心、呕吐等,部分有头痛、肌肉酸痛腹泻等。常有颈部及腹股沟等浅表淋巴结肿大伴压痛、上腹部压痛及相对缓脉。少数病例病情危重、出现意识障碍,皮肤瘀斑、消化道出血及肺出血等。患者可因休克、呼吸衰竭和弥散性血管内凝血(DIC)等多器官功能衰竭而死亡。绝大多数患者预后良好,但既往有基础疾病、老年患者、出现精神神经症状、出血倾向明显、低钠血症等提示病重,预后较差。
SFTS的临床分型
SFTS临床分4型(表1),轻型以儿童和青壮年多见,重型多见于老年患者。血小板计数是SFTS患者分型的重要指标,所有患者的血小板都会减少,LDH、AST、ALT及CK等血清酶均是患者预后较差的预测指标。除此之外,王贵强教授指出,铁蛋白增加尤其能提示SFTS患者失血的风险增加。病情越重,病程越长。
表1 SFTS的临床分型


SFTS的临床分期
SFTS病程可分为3个重叠的阶段,分别为发热期、多器官功能损害期(也称为极期)和恢复期(表2)。其中,多器官功能衰竭一般发生在1周之后,MODS早期指标包括血小板计数、白细胞计数、病毒载量、LDH、CK、AST和铁蛋白。王贵强教授介绍,AST(谷草转氨酶)不仅仅代表肝脏原发损害,而是全身多器官功能损害的一种标志。患者在感染SFTSV后发生炎症因子风暴时,多伴随着AST快速持续的增加。因此AST也常常是预后不良的表现。
表2 SFTS的临床分期
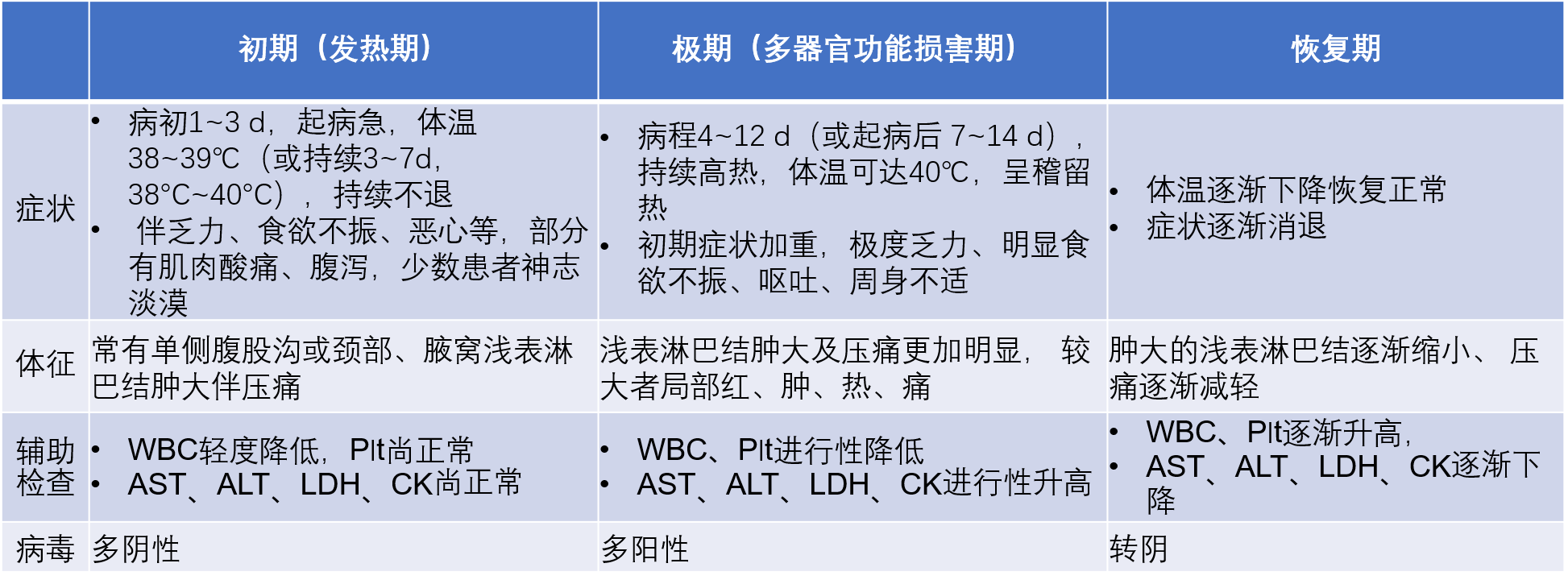

从免疫学角度,初期包括发热期和脑炎期,均为高炎症状态;后期处于免疫抑制状态。因此,STFS早期可以利用激素进行抗炎治疗,但激素使用的时机和用量仍然有待商榷。
重症早期的预警指标
重症SFTS的高风险人群具有以下特点:体温高达39 ℃,持续48~72 h以上;年龄>60岁;有糖尿病、肿瘤等基础疾病;有神经系统整整;血小板计数<30×10^9/L,中性粒细胞计数≤1.0×10^9/L;肌酸激酶、肌酸激酶同工酶、乳酸脱氢酶≥2倍正常值;铁蛋白明显升高等。
预后不佳的相关指标
高龄、基础病、发病至入院时间长;精神神经症状;出血倾向明显;严重低钠血症;铁蛋白明显升高(噬血细胞综合征);高水平LDH、CK;外周血T淋巴细胞总数和CD4+ T淋巴细胞显著减少,NK细胞显著增加;髓样树突状细胞减少;高水平IL-6、IL-10;高水平血浆病毒核酸载量;血清血管紧张素升高等;
SFTS的并发症包括继发感染、出血及弥散性血管内凝血(DIC)、急性胰腺炎、电解质失衡(如低钠和低钙)、病毒性脑炎、噬血细胞综合征和多器官功能障碍等。
疑似病例、确诊病例和聚集性病例的相关诊断条件与前版指南变动不大。关于SFTS的鉴别诊断,需要与以下四类疾病相鉴别(表3)。
表3 SFTS的常见鉴别诊断疾病
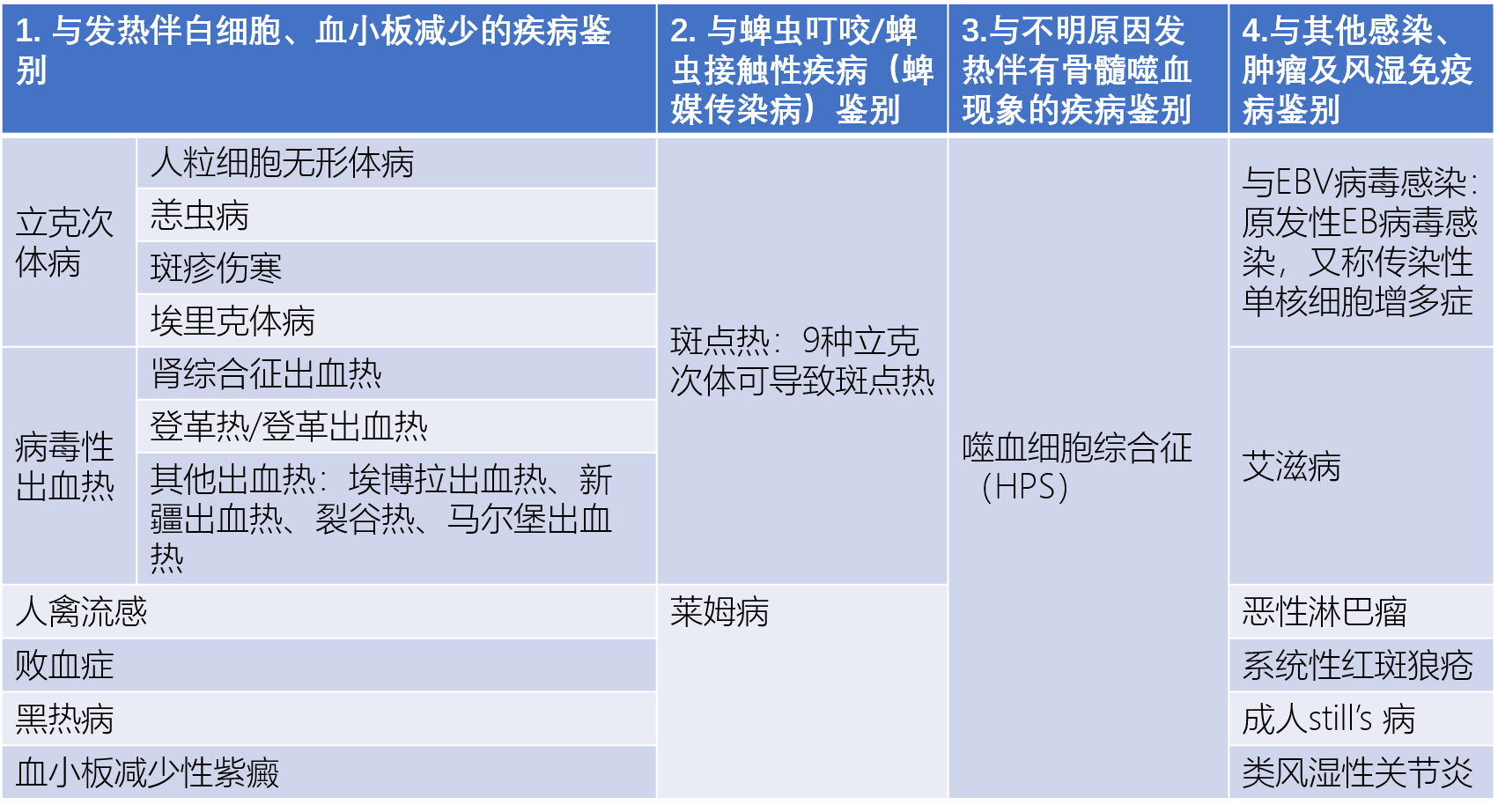

本病尚无特异性治疗手段,主要为对症支持治疗、继发感染和基础疾病的治疗。
病原学治疗
针对SFTSV治疗,有潜在治疗价值的药物包括法匹拉韦、六氯酚、钙通道阻滞剂、2-氟-2脱氧胞苷、咖啡酸、阿莫地喹、γ-干扰素(IFN-γ)。此外,尽管体外试验显示利巴韦林对SFTSV有抑制作用,但临床试验并无治疗效果,不推荐使用利巴韦林治疗SFTS。
糖皮质激素使用
糖皮质激素使用需要注意使用时机,应在感染早期,即炎症反应阶段及时使用糖皮质激素。具体适应证包括炎症因子风暴、继发噬血细胞综合征或伴发病毒性脑炎等。王贵强教授认为,大剂量激素冲击治疗不一定能改善预后,关键仍需要聚焦于糖皮质激素使用的时机。
此外还有康复期血浆、血液净化等也可以作为有效治疗手段。
具体措施可参考2011年版《发热伴血小板减少综合征经接触传播预防控制要点》。由于SFTS可以通过接触传播且有人传人特点,因此尤其要加强医护人员的防护。
当前,我国发热伴血小板减少综合征的危害没有引起足够的重视,近年的发病率不断在增加,疫区逐渐扩大。尽管原疫区已对SFTS的诊治具有一定经验,但新疫区病死率较高,因此需要相关地区的医务人员和群众加强对该病的认识。
关于SFTS,其流行病学、发病机制、早期诊断方法标准化、重症高风险人群、重症病例的早期预警指标、抗病毒治疗药物、糖皮质激素治疗及相关疫苗均存在空白等待研发解决。王贵强教授强调,治未病是预防,治未重是临床。治未重的理念是在病情未加重前就要预见性干预,根据客观的预测预警指标进行病情评估并进行相应干预。早期关注重症高风险人群和研究预测预警指标是改善SFTS患者预后的重中之重。
本文由中国医学论坛报原创整理,王贵强教授审阅

查看更多