查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





本文作者:杭州市红十字会医院临床药学科 王怀冲
指导专家:南京大学医学院附属金陵医院呼吸与危重症医学科 施毅
本文通过对1例支扩伴PA感染病例的治疗提出问题,特别邀请南京大学医学院附属金陵医院施毅教授答疑解惑,以期为目前医疗机构特别是基层医院如何治疗PA感染,如何优化抗菌药物治疗方案指点迷津。
患者基本情况:患者男,61岁,因“咳嗽咳痰伴发热气急3天”,于2020-12-21由急诊入院。
现病史:患者3天前受凉后出现咳嗽咳痰,黄脓痰,量多,偶有痰中带血,伴有胸闷气急,体温最高37.8℃,诊断“肺部感染”,予头孢哌酮/舒巴坦(CPZ/SBT)静脉滴注(简称静滴)治疗3天,咳嗽咳痰、胸闷气急未见明显好转。为求进一步诊治,以“社区获得性肺炎”收治入院。
既往患者“支扩伴感染”病史50余年,2年余前行肺减容术,现长期吸入茚达特罗/格隆溴铵1吸/天改善肺功能,自诉症状控制一般。
专科检查:T 36.7℃,P 107次/分,R 24次/分,BP 160/81mmHg,双侧颊黏膜可见白斑。桶状胸,双肺呼吸音粗,双肺可及干啰音。余无殊。
入院诊断:社区获得性肺炎,非重症;支扩伴感染;支气管哮喘;肺大疱;高血压1级;前列腺增生;阻塞性肺气肿。
出院诊断:社区获得性肺炎,非重症;慢性呼吸衰竭;耐碳青霉烯类PA感染(CRPA);支扩伴感染;支气管哮喘;阻塞性肺气肿;肺大疱;高血压1级;前列腺增生。
治疗经过:入院后完善相关辅助检查,2020-12-25检查:红细胞沉降率 45.00 mm/1h;血常规 白细胞 5.6×109/L,中性粒细胞% 60.70%;全量程超敏C反应蛋白(CRP)51.18 mg/L;余无殊。2020-12-27 痰培养报告:PA +++,阿米卡星(AMK) 敏感(S),CPZ/SBT 耐药(R),美罗培南(MEM) 中敏(I)。2021-1-9 痰培养报告:PA ++,AMK敏感(S) ,CPZ/SBT (I),MEM ≤1 (S)。入院后予CPZ/SBT 2.0 g q8h静滴联合AMK 0.4 g QD静滴抗感染。治疗过程中出现发热38.1℃,于2021-1-4方案改为MEM针1.0 q8h静滴抗感染治疗,后患者体温恢复正常,复查血炎症指标下降。
附表:患者住院期间抗菌药物治疗方案
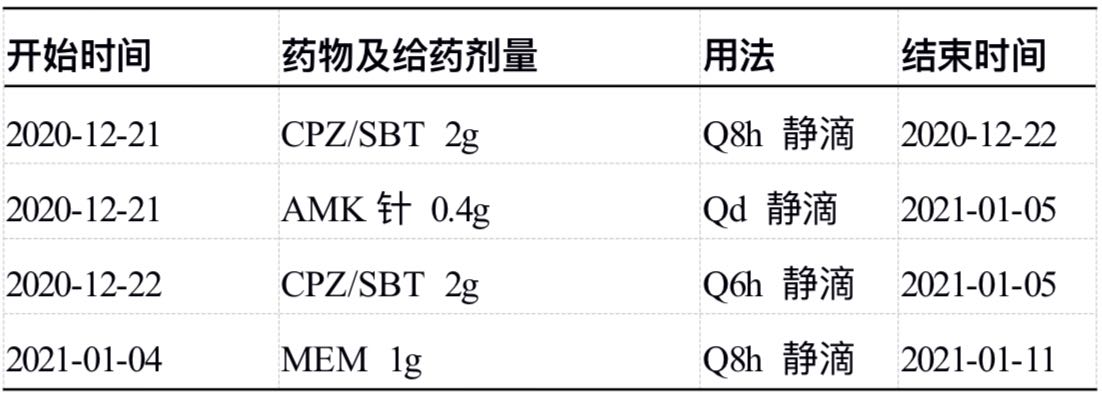
一、患者初始的治疗方案是否需要根据药敏报告调整?
首先,我们要搞清楚MDR、泛耐药(XDR)和全耐药(PDR)的概念。MDR是指细菌对于常见抗菌药物(包括头孢菌素类、碳青霉烯类、β-内酰胺酶抑制剂复方制剂、氟喹诺酮类和氨基糖苷类)中3类或3类以上的药物耐药,XDR是指细菌仅对1~2种抗菌药物敏感(通常指多黏菌素和替加环素),而PDR则是指对目前临床应用的有代表性的各类抗菌药物均耐药的菌株。临床上常用的具有抗PA活性的抗菌药物包括:头孢菌素类、碳青霉烯类、喹诺酮类、氨基糖苷类、加酶抑制剂、多黏菌素类。对于耐药菌的治疗可以采用双药方案或者三药方案,每个治疗方案尽量做到至少有一种药物是敏感的。
PA是临床最常见的MDR和PDR致病菌之一,其耐药机制涉及多个方面:
① 产生灭活酶:PA可产生β-内酰胺酶、氨基糖苷类修饰酶、氯霉素乙酰转移酶等。
② 膜通透性下降:主动外排系统过度表达和膜孔蛋白丢失或表达下降。
③ 靶位改变:拓扑异构酶基因突变和细菌核糖体16S rRNA甲基化。
④ 细菌生物被膜形成:细菌附着于惰性物体表面后,繁殖并分泌一些多糖基质和纤维蛋白等复合物,将细菌粘连包裹其中而形成的膜样物。细菌能够通过生物被膜的形式生存,逃避机体免疫和抗菌药物的杀伤作用。
⑤ 整合子作用:通过接合、转化、转导和转座等方法在细菌间转移,成为细菌MDR迅速发展的重要原因。
在治疗前,首先应明确是PA感染还是定植。有无感染的临床表现最为重要,即使是合格痰标本分离到多量单一PA,但临床并不存在任何下呼吸道感染的表现,也无需针对PA的治疗。如果同时分离到其他细菌,又有下呼吸道感染的临床表现,则需要明确真正的致病原或为混合感染。当针对单一PA治疗后疗效满意时较易确定是PA感染,但当疗效不满意时也难以完全否定,因为尚有剂量、疗程、联合用药与否、是否有混合感染(特别是厌氧菌)等许多问题的干扰,也可能在治疗过程中产生急性耐药(以单药治疗最为常见)。
PA下呼吸道感染的治疗应该遵循以下原则:
① 选择有抗PA活性的抗菌药物,通常需要联合治疗;
②根据药代动力学/药效学(PK/PD)理论选择正确的给药剂量和用药方式;
③ 充分的疗程;
④ 消除危险因素;
⑤ 重视抗感染外的综合治疗。
本患者的初始治疗方案选用CPZ/SBT联合AMK是合理的。对于MDR-PA,β-内酰胺类抗菌药物与氨基糖苷类或氟喹诺酮类抗菌药物联合后均可提高对PA的抗菌活性,但氨基糖苷类对β-内酰胺类抗菌药物的增效作用略强于氟喹诺酮类。关于治疗过程中需不需要更换治疗方案的问题,需要结合治疗效果综合考虑。本患者在治疗的过程中痰培养显示CPZ/SBT从耐药变成了中介,MEM从中介变成了敏感。如果初始治疗方案剂量足够,治疗结果好转就不需要更换方案;如果临床症状没有改善,就需要考虑更换方案。需要注意的是药敏虽然给了临床很多提示信息,但临床效果是最重要的决策依据之一,因为体外和体内可能不完全一样,况且对于联合方案体内还可能有协同作用。本患者治疗过程中虽然出现了发热和CRP升高情况,由于抗菌药物起始治疗剂量不足,所以不能判定为药物选择欠佳。当然,如果培养出MEM是敏感的,可以考虑更换为MEM联合方案。
二、MEM、CPZ/SBT和AMK剂量是否足量,如果病情加重后续的抗菌方案如何考虑?
抗菌药物的选择和使用剂量,药敏报告的解读很重要,尤其是药物的最低抑菌浓度(MIC)。优先选择敏感且远离MIC折点的药物,对于XDR或者PDR,药物选择有限时也可以考虑MIC中介的药物联合。MEM为时间性依赖抗生素,抗菌疗效取决于体内药物浓度大于MIC时间(fT>MIC),碳青霉烯类fT>MIC的期望值应达到给药间隔的40%。本患者MEM最后一次痰培养MIC为1 mg/L,单次1.0 g q8h给药时,有研究得出fT>MIC占给药间隔的百分比达到86.07%,此时用药剂量是可以的。当MIC为2、4、8 mg/L时,可以通过增加给药剂量、缩短给药间隔、延长给药时间等措施提高fT>MIC。对于本患者如果MEM改为2 g q8h、1 g q6h或者单次滴注时间延长到3h,是可以进一步提高fT>MIC的。
需要注意的是,进口的CPZ/SBT有两个规格,即CPZ∶SBT=1∶1或者2:1,在治疗PA中最好选择2:1的规格,这样可以充分利用CPZ对PA的杀菌效果。本患者采用的是=1∶1的规格,如果采用2 g q8h方案给药,其中CPZ一天的剂量仅为3 g,治疗剂量可能不足,方案改为2 g q6h,CPZ的剂量达到4 g,以延长药物与PA的接触时间,加强杀菌作用,提高临床疗效。
初始治疗方案中的AMK是敏感的,但临床微生物室并没有给出它的MIC,这是比较遗憾的地方,临床希望在给出敏感性的时候最好能给出具体的MIC,特别是治疗药物选择困难的情况下,具体的MIC可以帮助临床估算给药剂量。当AMK MIC≤2 mg/L时,可以根据说明书常规给药;当AMK MIC>2 mg/L时,就需要提高AMK剂量才能发挥最大效果。另外,AMK的使用需要考虑患者的肾功能情况:对于肾小球滤过率(eGFR)>80 ml/min的患者,AMK的用量为15 mg/kg qd,且通常需要联合用药;肾功能受损患者的给药剂量建议参考《抗微生物治疗指南》具体调整。本患者年龄61岁,体重55 kg,肾功能正常,采用0.4 g qd给药剂量不足,达不到预期的治疗目的。关于AMK的给药频次,由于氨基糖苷类药物是浓度依赖性抗生素,Cmax/MIC与细菌清除率和临床有效率密切相关,同时肾小管上皮细胞与耳蜗毛细胞对较高浓度的氨基糖苷类摄取有“饱和”现象,因此,日剂量单次给药可保证疗效,减少耳、肾毒性,遏制细菌耐药。但鉴于我国生产的氨基糖苷类药物药品说明书尚未按照PK/PD特点来修正,临床应用时需要全面斟酌。如果患者确实担心肾毒性和耳毒性问题,建议AMK的剂量不应少于0.6~0.8 g qd。AMK的肾毒性和耳毒性与使用疗程相关,建议联合用药的时间一般为7d,根据临床需要最长疗程可以用到14d,症状好转即可停药。
三、双β-内酰胺类联合方案治疗PA的地位如何?
四、慢性感染是否需要做到PA的清除?
以上问题的精彩解答明日发布,
请持续关注壹生APP资讯—“感染”频道~~
点击下图观看以上问答内容的直播回放↓↓
查看更多