查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





急性呼吸窘迫综合征(ARDS)仍然是高死亡率的综合征,目前尚无有效的治疗方法。我们对这种复杂的肺部损伤的潜在机制的认识有提高,并发现许多途径和靶标,这些途径和靶标有成为治疗方法的潜力,目前其中一些正在进行临床前测试。鉴于ARDS临床综合征的多样性,表型分析技术或工具(例如“精准药物”)可能能确定从某些疗法中受益的患者群体。潜在的新疗法,例如间充质干细胞在ARDS中表现出巨大的潜力。其他潜在的治疗方法(其中一些已经存在多年)尚不确定其在ARDS中的使用情况,仍然值得进一步研究。在这里,我们讨论ARDS疗法的最新发现和当前状态。
间充质干细胞(MSC)是免疫调节的成熟细胞,可以促使损伤的消退和肺组织的修复。
作用机制
MSC通过旁分泌和细胞间接触与免疫细胞进行交流,从而发挥作用。Zhang等研究证明在小鼠内毒素(LPS)急性肺损伤(ALI)模型中,MSC介导的PGE2可以增加乙酰胆碱的分泌,从而减少炎症反应。Chen等证明了MSC介导的肝细胞生长因子(HGF)的体外分泌促进了促炎性Th17细胞向抗炎性T调节细胞(Tregs)的分化。同样,肺内的MSC在小鼠中可下调Th17细胞,上调Tregs并改善ALI。另一项研究表明,间充质干细胞通过旁分泌HGF的释放促进树突状细胞向调节性树突状细胞的分化,并减轻LPS诱导的小鼠ALI。调节性树突状细胞具有更高的吞噬活性并抑制T细胞增殖。
最近的一项研究在HARP-2他汀类药物试验中利用了来自ARDS患者的支气管肺泡灌洗液(BAL),从而通过事后潜伏期重新分析确定了患有高炎症性或低炎症性ARDS的患者的两种表型。将这些BAL添加至人肺上皮细胞和肺微血管内皮细胞,并评估线粒体损伤和屏障功能。只有从具有功能线粒体的多发间质干细胞中衍生出来的细胞外囊泡才能恢复上皮细胞和内皮细胞的线粒体功能和屏障完整性,而细胞外囊泡在低炎症环境中更有效。该研究还表明,在两种鼠类ARDS模型中,MSC在解决肺损伤方面比细胞外囊泡更有效。最后,在内毒素性肺损伤模型中,MSC衍生的条件培养基能够通过抑制NF-kB降低肺损伤的严重程度。
供体多样性
来自不同年龄和健康状况的供体的MSC基因表达,分化潜能和下游治疗功效方面可能具有显著不同的特征。组织来源,细胞分离和培养技术也可能产生异质MSC产物。Trivedi等人观察到,从三个不同的供体中分离出的MSC显示出MSC标记的同质性存在活性差异。HUANG等人研究中,人类MSC来源的细胞外囊泡是从年轻的供体获得的,而不是老的供体,它们能够在鼠ARDS模型中减轻肺损伤。另一项研究表明,使用CD362表面标记选择的脐带来源MSCs的亚群可以改善啮齿类动物大肠杆菌肺炎,并发现该细胞分离技术可能提供更明确和有效的MSC群体。
微环境对间质基质细胞的影响
MSC的表达取决于它们所暴露的特定微环境。Abreu等人将MSC暴露于来自不同ARDS患者的BAL,并观察这些MSC的促炎细胞因子和抗炎细胞因子的差异基因表达。Rolandsson Enes等人的研究不仅发现临床使用的MSC更具促炎性,而且ARDS或囊性纤维化患者接触BAL后,MSC会引发不同的炎症反应。Fergie等进一步表明,高碳酸血症性酸中毒环境会抑制MSC介导的上皮保护。最近,Islam等分析了不同急性肺损伤(ALI)模型中接受启动或转基因MSC的肺蛋白组学特征,表明损伤类型和启动方法可以确定MSC的影响是有利的还是有害的。因此,特制的MSC可能是增强其体内治疗效果的有用技术。
XU等发现,MSC暴露于ARDS的动物血清中,其MSC具有增强的治疗作用。另一项研究表明,在呼吸机诱发的肺损伤(VILI)模型中,用促炎性细胞因子预激活MSC可抑制肺部炎症并增强肺修复能力。与源自幼稚MSC的细胞外囊泡相比,IFN-β引发的MSC的细胞外囊泡在大鼠模型中能更好地减轻大肠杆菌肺炎,体外试验中源自Poly(I:C)预活化MSC的细胞外囊泡可减轻人体中的严重大肠杆菌肺炎损伤。最后,血红素加氧酶-1,IL-10或p130 / E2F4在MSC中的过表达可以改善内毒素或大肠杆菌诱导的ALI。
间充质干细胞临床试验
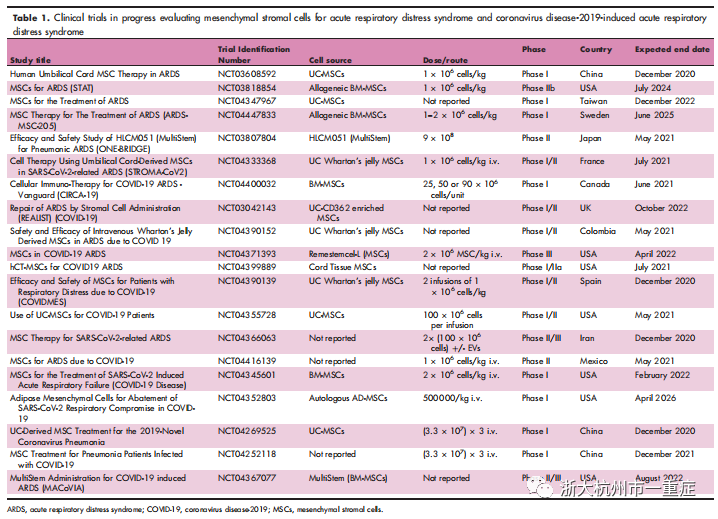
在STAT IIA期试验中,ARDS患者对10×106骨髓来源(BM)-MSC/kg耐受性良好;然而,最重要的预后没有明显改善,这是由于治疗组患者不良的MSC生存能力和较严重的基线损伤。还没有完全发表的多系统BMSC细胞治疗I/II期试验(NCT02611609)的初步结果提示:ARDS患者使用MSC是安全的,并有可能能降低28天的死亡率和降低呼吸机支持需求。单臂研究的初步报告中,22名患者接受1×106UC-MSC/kg治疗,记录无副作用,并观察到MSC用药可以改善氧合和减少肺损伤。目前,一些临床试验正在进一步研究用于ARDS的MSC,包括REALIST试验(NCT03042143)和STAT试验(NCT03818854)(如图)。
SARS-CoV-2诱导的ARDS发生在5%的感染病毒的患者中,在其发病机制中具有较强的促炎成分,这是MSC临床试验的原理。Leng等人发现,7例COVID-19患者的ACE-/-MSC(10×106/kg)降低了C反应蛋白和TNF-a水平,提高了氧合和IL-10水平。目前有大量研究用于COVID-19 ARDS的MSC的临床试验(如图)。
本文首发于浙大杭州市一重症公众号 作者陈嘉伊
查看更多