查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





韩国研发了一种新的核苷酸类抗乙型肝炎病毒新药——贝西福韦(besifovir),最近发布了该药治疗慢性乙型肝炎192周的数据。
贝西福韦是一种新型无环核苷酸磷酸酯,其化学结构与阿德福韦和替诺福韦相似,通过一种活性代谢物(三磷酸鸟苷的核苷酸类似物)抑制HBV复制。马来酸贝西福韦酯(besifovir dipivoxil maleate)是贝西福韦的前体药,口服可迅速被胃肠道吸收,原药及其代谢产物主要通过肾脏排泄。>60 mg/d的剂量即可有效抑制人体内的HBV,临床试验的剂量为150 mg/d。
这项研究入组的情况见图1。共197例患者参加随机入组,0~48周为双盲期,患者被随机分为贝西福韦组和替诺福韦组,分别服用贝西福韦150 mg/d或替诺福韦300 mg/d治疗,48周后为开放期所有患者都服用贝西福韦150 mg/d治疗。
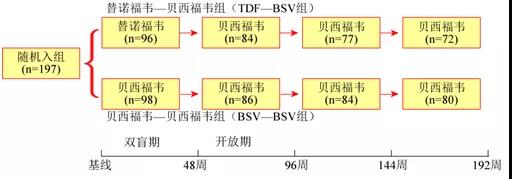
图1 贝西福韦治疗慢性乙型肝炎192周3期临床试验入组情况
2019年11月和2020年8月分别公布了该项研究96周和144周的结果。贝西福韦—贝西福韦组(BSV—BSV组)和替诺福韦—贝西福韦组(TDF—BSV组)HBV DNA<20 IU/ml患者的比例在双盲期结束时分别为63.8%和68.8%(P=0.47),在96周时分别为81.4%和77.4%(P=0.52),在144周时分别为80.3%和85.5%(P=0.38)。见图2[4]。两组患者HBV DNA阴转率的差异无统计学意义。
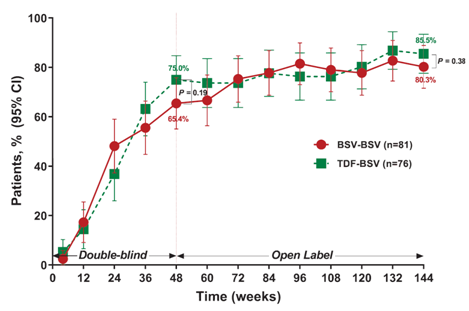
图2 贝西福韦治疗慢性乙型肝炎144周HBV DNA阴转率
2021年1月4日,贝西福韦治疗慢性乙型肝炎192周的结果被公布(未提供图),两组患者HBV DNA<20 IU/ml的比例均为87.5%(70/80比63/72,P=1.00)。治疗192周仍有明显的抗病毒作用,且没有发现耐药的证据。由此看来,贝西福韦的抗病毒作用与替诺福韦相似,但是两组152例患者中仅1例HBsAg阴转,HBeAg血清转换率也只有10.2%~12.5%。
安全性方面,在双盲期贝西福韦组和替诺福韦组各有1例患者发生肌酸激酶(CK)升高>5倍正常值上限,其中1例(替诺福韦组)退出研究;在开放期96周时,两组各有1例因结核性结肠炎和血小板增多症退出研究,但研究者认为与治疗药物无关;在96-144周期间,没有新的严重药物不良反应。在肾脏和骨髓安全方面,192周的结果显示贝西福韦—贝西福韦组(BSV—BSV组)的肾功能和骨密度保持良好,替诺福韦—贝西福韦组(TDF—BSV组)在双盲期因替诺福韦导致的肾损伤和骨密度下降在开放期换用贝西福韦治疗后逐渐恢复。144周研究中两组患者肾小球滤过率和骨密度的改变见图3-5(192周的数据未提供图)。
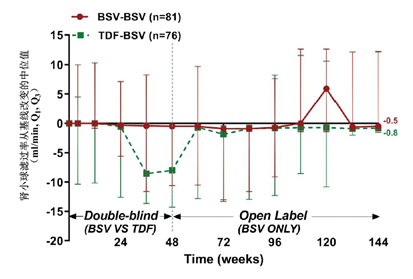
图3 贝西福韦治疗慢性乙型肝炎144周临床试验中两组患者肾小球滤过率的改变
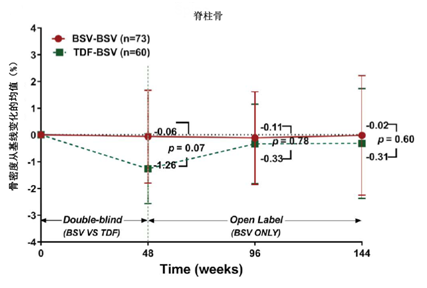
图4 贝西福韦治疗慢性乙型肝炎144周临床试验中两组患者脊柱骨密度的改变
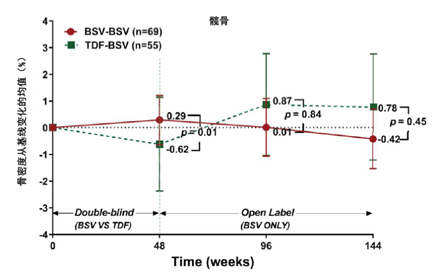
图5 贝西福韦治疗慢性乙型肝炎144周临床试验中两组患者髋骨骨密度的改变
但是,贝西福韦最常见的不良反应是肉碱消耗,这种不良反应在以往上市的几种核苷(酸)类抗HBV药均未见报道。在脂质分解过程中,L-肉碱是脂肪酸从细胞质转运到线粒体产生代谢能所必需的。与阿德福韦相似,贝西福韦也有一个肽基。当新戊酸进入细胞时,会形成新戊酰辅酶A,新戊酰部分会从辅酶A转移到肉碱,形成新戊酰肉碱,它直接在尿液中排出,而不是通常的能量生成途径。总左旋肉碱和游离左旋肉碱的正常范围分别为37~78 μmol/L和25~54 μmol/L。在Ⅱb期研究中,94.1%服用贝西福韦的患者血清左旋肉碱消耗,与90 mg相比,服用150 mg的患者血清左旋肉碱消耗更多。总左旋肉碱和游离左旋肉碱的最低浓度分别为23.6 μmol/L和<20 μmol/L,83.9%和100%每天服用90mg贝西福韦和150mg贝西福韦的患者持续肉碱消耗,需要每天补充肉碱。所以,在192周3期临床试验中,所有患者均同时服用左旋肉碱660 mg/d。在192周时,有7例患者(BSV–BSV组2例患者和TDF–BSV组5例患者)的左旋肉碱水平下降,且无任何与肉碱缺乏相关的临床症状。
总体看来,贝西福韦虽然抗病毒的作用较强,但与替诺福韦相差无几,从疗效上无显著突破;尽管无明显肾毒性和骨毒性,但肉碱消耗、每天必须服用左旋肉碱补充和定期进行肉碱水平的检测也会给患者的心理和经济上带来很大压力。
作者:北京地坛医院 蔡浩东
文章转载自药物不良反应ADR
查看更多