查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过






当下allo-SCT通常用于高危复发 MM 年轻患者,但总体疗效不一,且随着近十年来新药的发展,allo-SCT 的作用越来越难以定义。近日,来自梅奥团队的一项研究为这一问题提供了新答案。
对于 MM 这一无法治愈的克隆性浆细胞疾病,allo-SCT 仍存在争议。
对于部分患者来说,由于移植物 vs 骨髓瘤效应,它提供了一种潜在的治愈方式,但对更多患者来说,由于移植物抗宿主病 (GVHD),它会引起相当大的毒性。因此allo-SCT并不常规用于 MM 患者,但在过去30年中其利用率确实有所增加。
如今allo-SCT通常用于高危复发 MM 年轻患者,但总体疗效不一,且随着近十年来新药的发展,allo-SCT的作用越来越难以定义。

Walker M. Schmidt教授牵头回顾性分析了梅奥诊所2000-2022年间85例接受 allo-SCT 的MM患者中位随访11.5年的结局和预后标志物,并确定了 allo-SCT 后有利结局延长的患者。
这是既往随访时间较短的研究无法检测到的,而更多地了解 allo-SCT 患者结局和预后因素有助于指导这一可能延长生命甚至可能是治愈性手段的治疗决策。研究结果近日发表于Blood Cancer Journal。(文末可查看研究pdf原文)

该研究共纳入85例患者进行最终分析,基线特征见表1。allo-SCT时的中位年龄为51.2岁,从 MM 诊断至 allo-SCT 的中位时间为2.7年。72.6%(N=61) 为男性,27.4%(N=24) 为女性。大多数为白色人种 (89.4%,N=76)。
81例患者 (95.3%) 接受过一次或多次自体SCT,仅4例患者 (4.7%) 既往未接受过自体SCT。
大多数患者 (56.5%,N=48) 是在 MM 诊断后2-5年接受allo-SCT。
在既往接受过自体 SCT 的患者中,大多数患者是在接受自体 SCT 后2年内接受allo-SCT (55.6%,N=45)。
94.1%的患者 (N=80) 在诊断时具有细胞遗传学风险特征,其中66.3%(N=53)为标危,33.8%(N=27)为高危。
约半数患者 (N=47,55.3%) 接受清髓性 (MA) 预处理方案,而其余患者 (N=38,44.7%) 接受降低强度 (RIC) 或非清髓性 (NMA) 方案。Allo-SCT 前患者接受的既往治疗线中位数为4。队列的中位随访时间为11.5年。
表1 患者特征、治疗特征和疾病特征
整个队列的中位 OS 为1.7年,3年 OS 为37.9%,5年 OS 为22.2%,10年 OS 为16.8%。PFS 为0.71年,3年 PFS 为22.0%,5年 PFS 为15.1%,10年 PFS 为10.4%(图1)。异基因移植后1年治疗相关死亡率 (TRM)为23.5%。
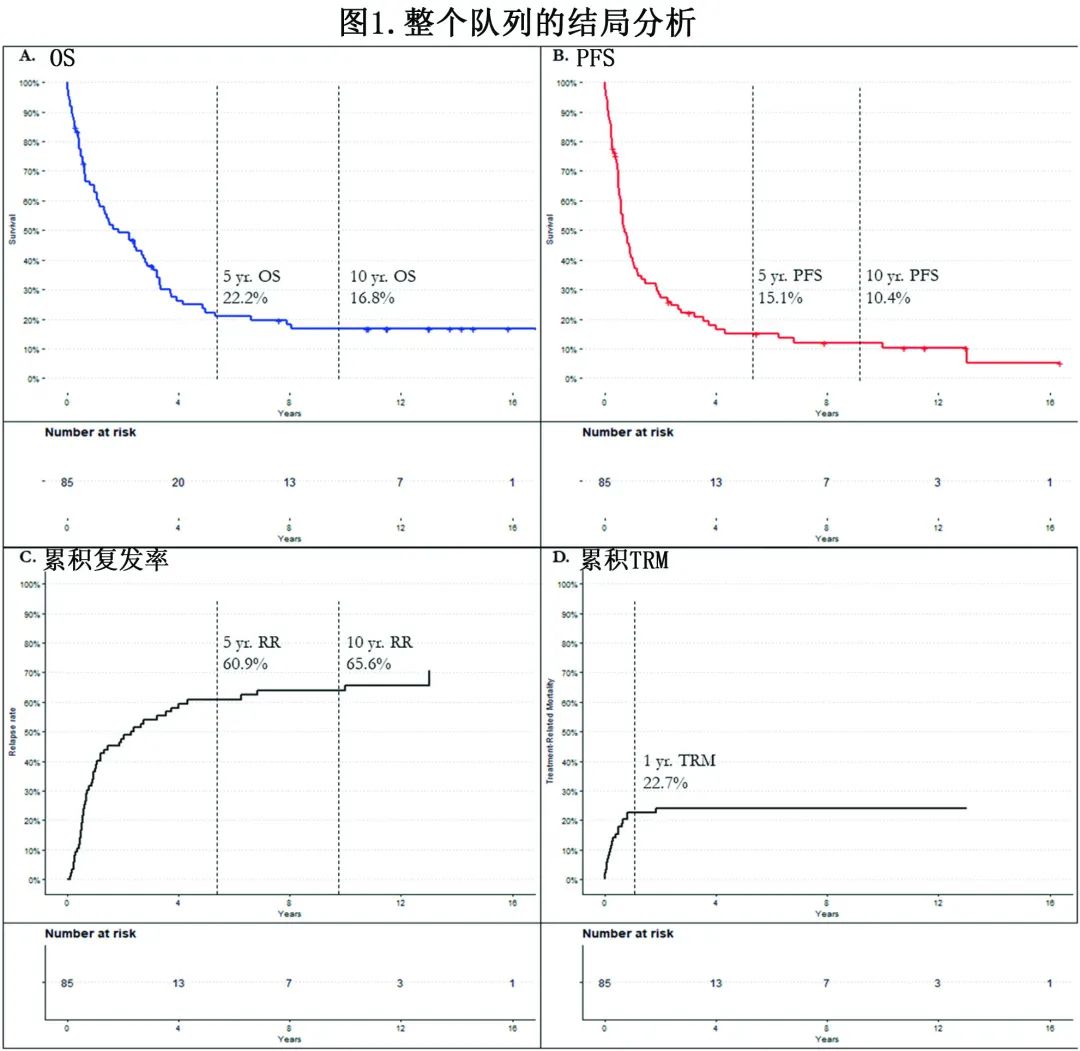
图1 队列结局分析
2022年5月数据分析时,18例患者(21.2%)仍存活。5年OS和PFS按患者、疾病和治疗特征分层,单变量分析结果见表2。

与 allo-SCT 时完全缓解的患者相比,活动性进展是 OS 的显著预后因素 (HR=3.39,p≤0.01)。
发生慢性GVHD (cGVHD)(p=0.04) 和既往自体SCT 次数(p=0.02) 也是 OS 的预后因素,但部分亚组较小。
PFS 的预后因素遵循相似的模式,allo-SCT时进展是最显著的不良预后因素 (HR=4.39,p≤0.01),此外既往自体 SCT 的次数也是预后因素 (p=0.02)。
表2 OS和PFS的单变量分析(基于患者特征、治疗特征和疾病特征)
12例患者 (14%) 表现出持久OS,allo-SCT后存活超过10年,表1显示了存活<10年与10+年的患者、治疗和疾病特征对比。
既往自体 SCT 次数和allo-SCT时期在两组之间存在统计学显著差异,存活10+年亚组更有可能既往接受过0或1次自体SCT(p=0.03),并在2000年至2010年间接受移植 (p=0.03)。
其他特征中则未发现差异,如基线细胞遗传学风险、骨髓消融方案或既往治疗线数;性别因素未达到统计学显著性 (p=0.07),存活10+年患者中男性的比例较高。

本研究表明,接受 allo-SCT 治疗多发性骨髓瘤的患者的总体生存结局较差,中位 OS 和 PFS 分别为1.7和0.71年,5年 OS 和 PFS 分别为22.2%和15.1%,即只有不到25%的患者可实现长期生存(>5年)。
到2年时近75%的患者发生疾病进展或死亡,1年 TRM 较高,为23.5%。但仍有部分患者在接受 allo-SCT 后进入持续缓解并可能实现治愈,从 allo-SCT 中获益的患者更有可能在 allo-SCT 时为完全缓解、既往未接受过或仅接受过一次自体SCT(p=0.03),并在2000年至2010年间接受移植 (p=0.03)。
除了特定的少数患者,allo-SCT作为 MM 的治疗获益极小。抗CD38、BiTE和其他新型治疗具有更好的结局和耐受性,应作为首选,而非allo-SCT。

作者:赵龙飞
首发:聊聊血液
查看更多