查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过






2026年3月27日,北京大学人民医院检验科与北京大学集成电路学院团队合作的研究发表在国际学术期刊Science Advances,题目为“EnvZ/OmpR-driven cooperative behavior promotes cefiderocol resistance in a hanging-droplet evolution system”。
该研究成功构建了具有高度工程创新性的微生物演化悬滴系统(Microbial Evolution Hanging-droplet System, MEHS),并在此基础上深入探讨了肺炎克雷伯菌在面对药物头孢德罗(Cefiderocol, CFDC)时的群体演化动力学,揭示了由EnvZ/OmpR双组分系统介导的罕见“群体合作行为”。这一发现打破了耐药演化的传统单克隆取代认知,为应对日益严峻的临床多重耐药危机提供了全新的理论视角与干预靶点。
本文的第一作者为北京大学人民医院在读博士研究生李博文。主要通讯作者为北京大学人民医院检验科的王辉教授,合作通讯作者为北京大学集成电路学院的王玮教授与申诗涛博士。
科学问题:新药耐药的“潜伏”与群体适应度代价
面对全球日益严峻的抗生素耐药性危机,CFDC作为一种新型的铁载体偶联头孢菌素,对碳青霉烯类耐药革兰氏阴性菌(如CRKP)表现出极其强大的抗菌效力。然而,近年来的临床报告揭示了一个令人担忧的科学问题:即使在从未广泛使用过CFDC的地区,也分离出了对CFDC天然耐药的肺炎克雷伯菌株。这引发了人们对潜在、隐匿耐药途径的极大担忧。
更深层次的科学问题在于:细菌在获得极高耐药突变时,往往会伴随巨大的适应度代价(Fitness costs,即生长变慢、竞争力下降)。在真实且波动的临床药物压力下,细菌群体是如何克服这种代价,并在药物的围剿中快速存活并演化的?传统的“优胜劣汰、单克隆绝对优势取代”理论,似乎无法完美解释那些尚未接触药物就已潜伏耐药潜力的复杂演化路径。
工程问题:传统演化模型的局限与破局
为了探究上述科学问题,研究人员通常依赖适应性实验室演化(ALE)模型。然而,现有的体外模型存在巨大的工程瓶颈:
1.传统摇瓶/批次培养:处于均匀混合的环境,完全无法模拟真实临床感染中复杂的空间结构和动态波动的药代动力学特征。
2.现有的微流控/液滴芯片平台:虽然能模拟微环境,但由于空间高度受限,极易发生细菌堵塞,导致培养周期短、生物量产出极低、采样不灵活,且很难维持长时间、动态波动的药物浓度梯度。
因此,亟需在工程学上开发一种既能提供微观结构,又能长期维持大规模细菌指数级生长,且能完美模拟临床给药波动的全新体外培养平台。
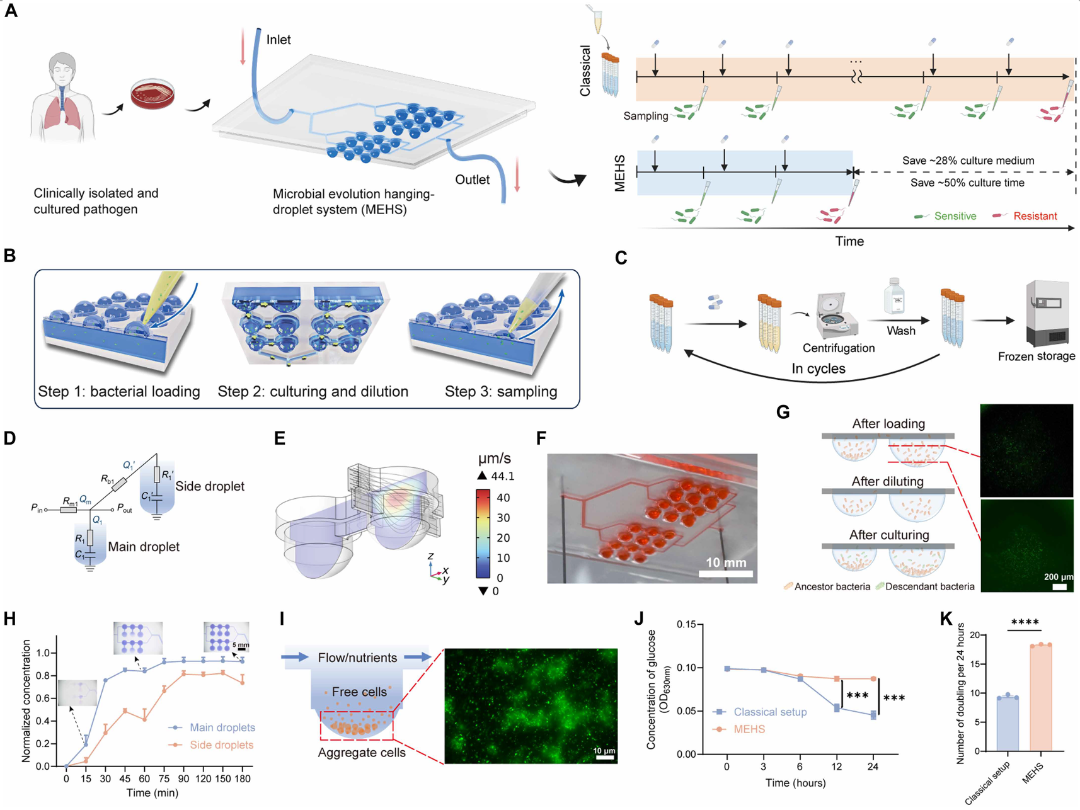
研究方法:首次提出悬滴培养细菌并实现耐药演化
针对上述工程痛点,医工交叉团队联手打造了一项极其巧妙的平台技术革新——MEHS。该方法摒弃了传统的封闭微通道,采用重力驱动流体技术在开放式的悬滴中进行细菌培养。
■ 连续指数生长:悬滴系统能持续洗脱“衰老”的细菌并输入新鲜营养,将细菌每日的繁殖代数翻倍。
■ 动态药代动力学模拟:系统可以精准调控流体,完美重现患者体内CFDC浓度高低起伏的波动状态。依托这一强大的MEHS平台,研究团队将肺炎克雷伯菌置于波动的CFDC药物压力下进行长期的演化实验,并结合群体基因组学、转录组学以及复杂的共培养竞争实验,对演化轨迹进行高分辨率解析。
核心研究结果:群体“合作演化”耐药机制
利用MEHS平台,研究团队取得了多项颠覆性的重要发现:
1.极速适应与“少数派”耐药:在波动的CFDC暴露下,肺炎克雷伯菌群体迅速获得了耐药性。但令人震惊的是,全基因组测序显示,真正发生基因突变的耐药克隆在演化后的总群体中仅占极小一部分,绝大多数细菌依然是基因型上的“敏感株”。
2.锁定临床高度相关的核心靶点:这些“少数派”携带的突变,与真实临床实践中观察到的变异高度重合,特别是集中在EnvZ/OmpR双组分系统上。
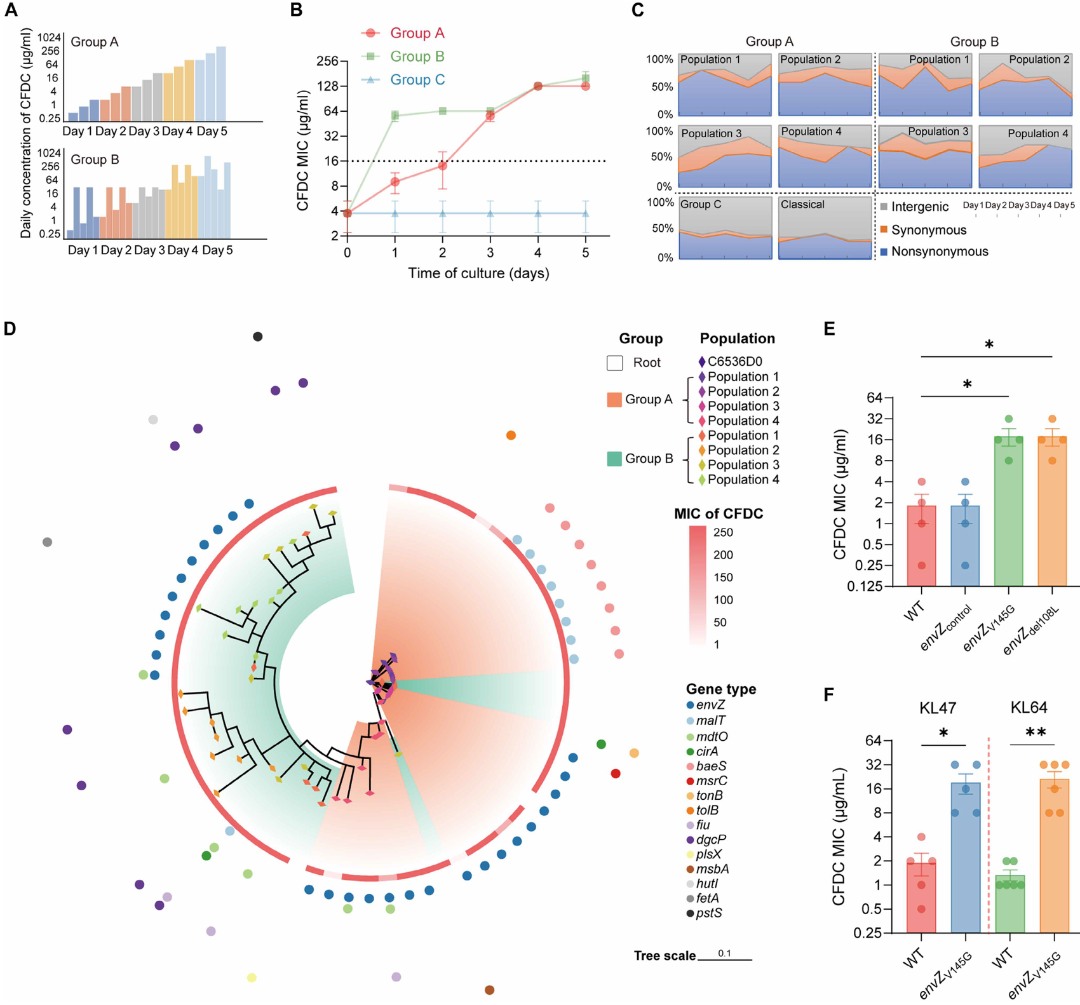
3.群体适应能力增加:这种“牺牲小我,保护大群体”的合作行为,极大地减轻了细菌因为获得耐药突变而本该承受的适应度代价。少数英雄挺身而出,带领整个群体在致死药物浓度下繁衍生息,实现了群体水平的适应。
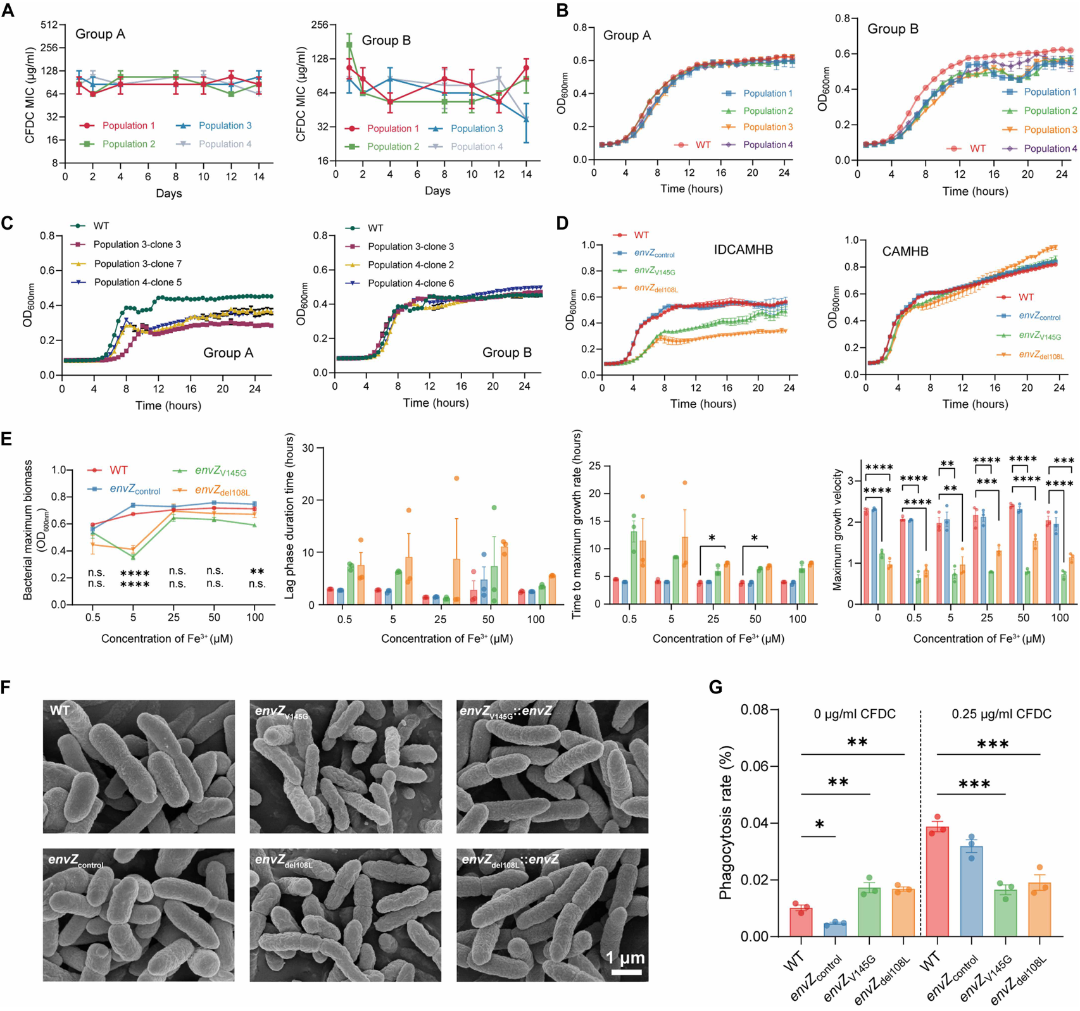
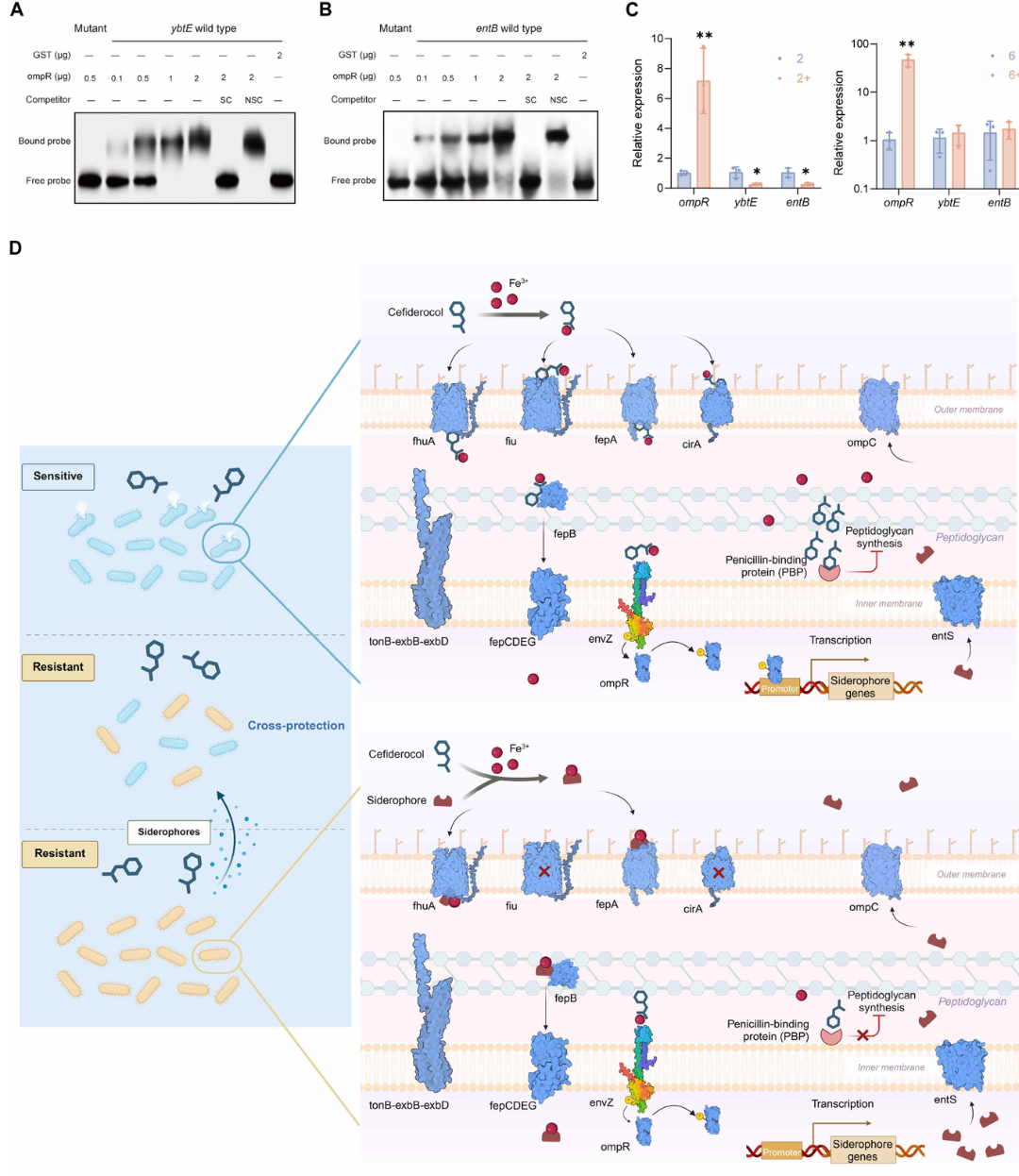
4.铁载体通路的重编程与群体“合作行为”:EnvZ/OmpR的突变导致了细菌铁载体生物合成途径的转录重配。这极少数的耐药突变株通过改变铁载体的代谢,竟然为周围原本脆弱的敏感亚群提供了强大的交叉保护。
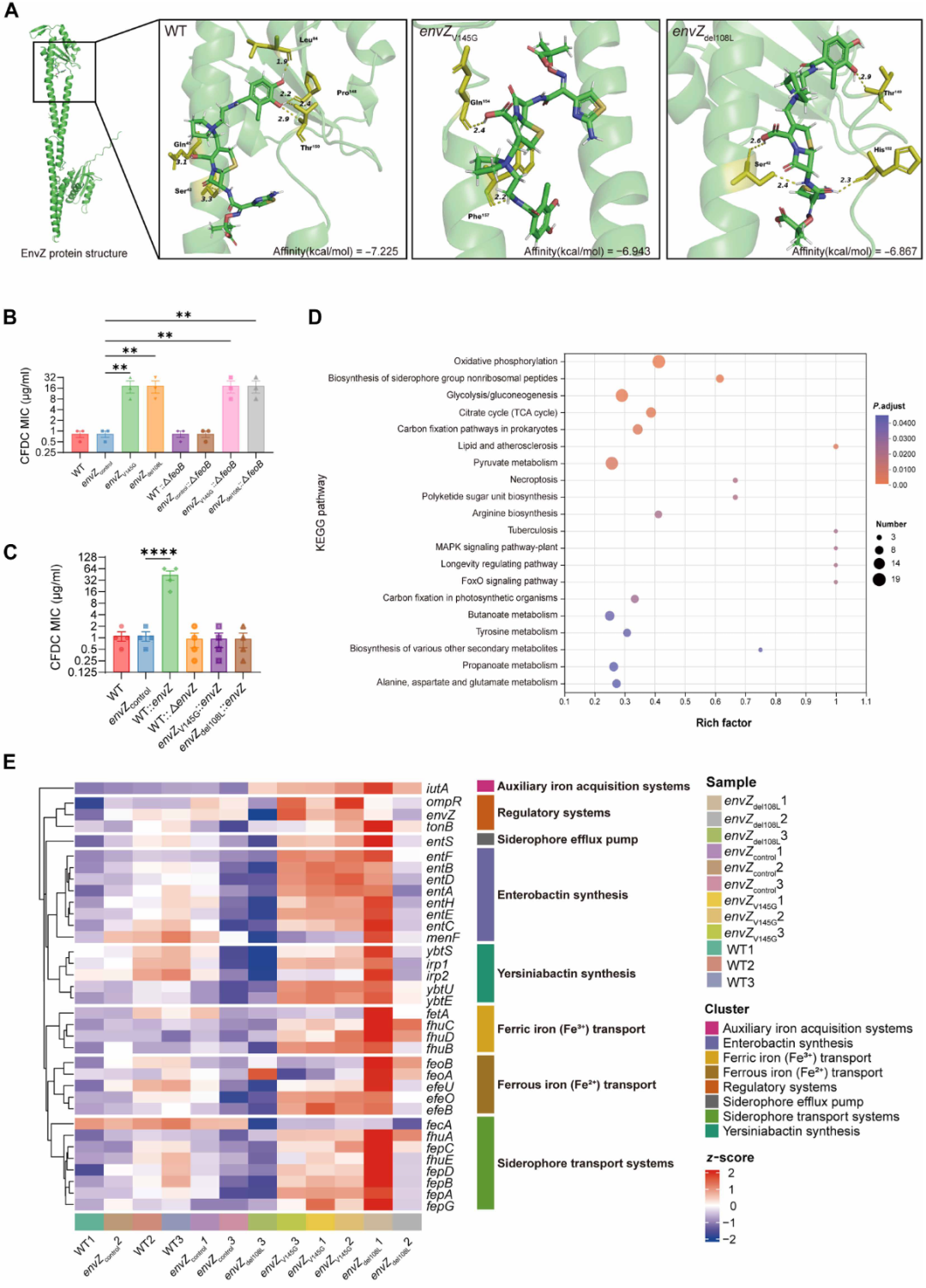
5.临床预警:研究团队进一步在CFDC正式投入临床使用之前收集的历史临床分离株中,也检测到了类似的EnvZ/OmpR变异。这凸显了病原体早已具备在特定选择压力下快速演化的隐性潜力。
研究结论与深远临床意义
本研究完美地融合了工程硬件创新与前沿微生物演化生物学,得出了以下核心结论:
1.技术层面:MEHS悬滴系统的成功开发,为体外高通量、高仿真地解析临床高度相关的耐药演化轨迹提供了一个极其强大的革命性平台。
2.理论层面:打破了抗生素耐药演化仅靠“耐药克隆单打独斗、赢者通吃”的刻板印象。证实了在特定药物压力下,病原体可以通过精妙的“合作行为”来实现整体的存活与演化。
3.临床干预新策略:这一机制为未来的抗感染治疗指明了新方向——未来的药物研发或许不应仅仅关注如何直接杀死细菌,而是可以靶向关键的调控节点(如EnvZ/OmpR)。通过“破坏”这种细菌间的社会化合作行为,瓦解群体的交叉保护网,从而恢复现有抗生素的强大疗效。
本研究由北京大学人民医院与北京大学集成电路学院团队强强联手完成。

第一作者:Bowen Li(李博文)
北京大学人民医院在读博士。主要聚焦微流控技术在医学检验中的应用,包括采用微流控等新技术探究微生物耐药及快速检测方面的研究。

合作通讯作者:Shitao Shen(申诗涛)
博士,北京大学集成电路学院

合作通讯作者:Wei Wang(王玮)
北京大学博雅特聘教授,博导,教育部长江学者特聘教授,国家卓青、微米/纳米加工技术国家级创新团队学术带头人。长期从事微系统相关技术研究,主持国家重点研发计划等多项国家级项目,在Lab Chip、IEEE MEMS、ECTC等领域重要期刊和会议上发表学术论文190余篇,授权发明专利40余项(美国专利2项)。担任微米纳米加工技术全国重点实验室主任,中国微米纳米技术学会副秘书长,中国仪器仪表学会微纳器件与系统技术分会、中国机械工程学会微纳制造技术分会、中国微米纳米技术学会微纳流控技术分会和微纳米制造及装备分会等学会理事,国家集成电路标准委员会委员、特种元器件标准委员会委员(微系统专项组组长),《Microfluidics and Nanofluidics》副主编、《Microsystems & Nanoengineering》编辑等社会和学术职务。

主要通讯作者:Hui Wang(王辉)
医学博士、长聘教授、博士生导师。北京大学人民医院检验科主任、北京大学医学部医学检验学系主任。
国家杰青、国家卫生健康委中青年突贡专家;中国医促会临床微生物分会主任委员;中华医学会微生物学和免疫学分会副主任委员;中华医学会检验医学分会常委兼临床免疫学组组长;《中华检验医学杂志》副总编辑;Microbiology Spectrum高级编委,Science Bulletin等多个杂志编委。连续四年(2022-2025)入选全球前2%顶尖科学家榜单“年度科学影响力排行榜”。研究方向:感染性疾病病原诊断、细菌耐药机制研究等。主持国家重点研发计划、国自然、北自然等30多项课题。获华夏医学科技奖科学技术奖一等奖(排1)、中华预防医学会科学技术奖科技进步二等奖(排1),获国家医学科技奖科学技术奖二等奖(排3)。
END
来源 京港感染论坛
查看更多