查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





2024年9月17日,瑞波西利在激素受体阳性(HR+)/人表皮生长因子受体-2阴性(HER2-)早期乳腺癌辅助治疗适应症在FDA正式获批。该适应症的获批是基于NATALEE研究阳性成果,该研究从临床实际需求出发,几乎纳入所有II-III期HR+/HER2-乳腺癌患者,包括以下三类人群:1)所有淋巴结阳性患者 2)N0合并肿瘤≥5cm患者 3)N0且肿瘤大小2-5cm,但合并高危复发因素(G3或Ki-67≥20%或基因组高风险),这意味着CDK4/6抑制剂辅助强化治疗覆盖人群将扩大近一倍,为更多HR+/HER2-早期乳腺癌患者带来治愈希望。本文特邀中国医学科学院肿瘤医院徐兵河院士(NATALEE研究中国主要研究者)深入解读瑞波西利早期HR+/HER2-乳腺癌辅助治疗适应症在FDA基于NATALEE研究全人群获批对于临床实践的意义。
肿瘤内科专家,北京协和医学院长聘教授、博士生导师
曾任中国医学科学院肿瘤医院大内科主任
现任国家新药(抗肿瘤)临床研究中心主任
国家肿瘤质控中心乳腺癌专家委员会主任委员
国家抗肿瘤药物临床监测专家委员会主任委员
中国抗癌协会肿瘤药物临床研究专业委员会主任委员
中国抗癌协会乳腺癌专业委员会名誉主任委员
中国医药教育协会肿瘤临床科研创新发展专业委员会主任委员
中国医师协会内科医师分会副会长
北京乳腺病防治学会理事长
HR+/HER2− eBC存在未被满足的临床需求,亟待探索新策略降低疾病复发风险
尽管HR+/HER2-早期乳腺癌患者经过标准内分泌治疗后普遍预后良好,但临床实践证实部分患者仍受疾病复发的威胁。据报道,HR+/HER2-早期乳腺癌患者中短期复发(<5年)率为20%~30%。对于淋巴结阳性,其复发风险较高,从短期来看,有1-3 个淋巴结转移(N1)的患者和有4-9个淋巴结转移(N2)的患者5年复发风险分别为10%和22%,从长期来看,N1和N2患者的20年复发风险分别为31%和52%。2024年ASCO公布的一项美国真实世界研究显示:具有高危因素的N0亚组患者的3年、5年、7年内侵袭性疾病复发的累积风险分别为8.5%、17.4%和25.7%。如何降低HR+/HER2-早期乳腺癌患者的早期复发风险和远期复发风险,实现更多患者临床治愈成为临床医生特别关注的问题。
NATALEE研究匠心设计,瑞波西利为更广泛HR+/HER2-早期乳腺癌患者带来治愈希望
NATALEE研究为一项全球多中心、随机对照、3期临床试验,共纳入5101例II-Ⅲ期HR+/HER2-早期乳腺癌患者,1:1分为瑞波西利+内分泌治疗组或单独内分泌治疗组(图1)。
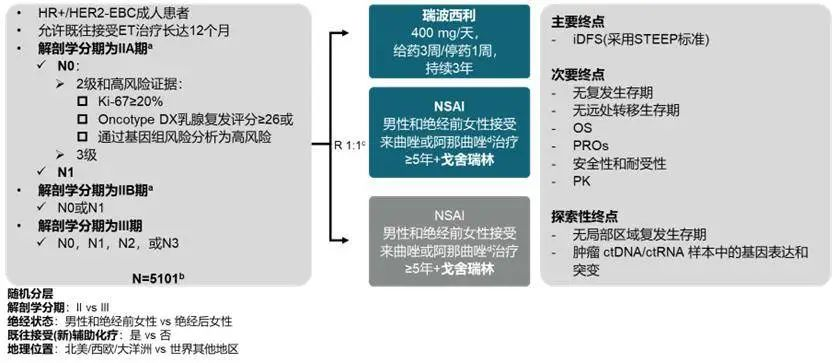
图1. NATALEE研究设计
广泛的入组人群,更加符合临床实践

NATALEE研究人群几乎包含了所有II到III期HR+乳腺癌患者,包括以下三类人群:1)所有淋巴结阳性 2)N0合并肿瘤≥5cm 3)N0且肿瘤大小2-5cm,但合并高危复发因素(G3或Ki-67≥20%或基因组高风险)。
从纳入人群特点上看,NATALEE研究包括了monarch E研究中的所有入组人群,并且II期患者占比相对较多,纳入了N0伴复发风险和所有II-III期HR+早期乳腺癌中的N1患者,更加贴合临床实际中具有复发风险人群的分布,旨在满足更多HR+/HER2-早期患者的未尽之需。
优化剂量为400mg,用药时间达3年,保证患者耐受性和依从性,且不影响疗效

NATALEE研究中,瑞波西利的用药方案为400mg/天,给药3周+停药1周,持续3年。相比瑞波西利用于晚期乳腺癌中的剂量600mg/天相对较低,这可能是考虑到不同于晚期乳腺癌以解救治疗为目的,相对足量的剂量起效迅速,可以更快降低肿瘤负荷,即便不良反应较为明显,也可以调整剂量继续治疗。而早期辅助治疗旨在预防复发,如果初始治疗不良反应较重,可能导致患者放弃治疗。因此,在辅助治疗背景下,通过减少用药剂量,从而降低剂量依赖性不良反应的发生率,能够改善患者的耐受性和依从性。
瑞波西利+ET稳健获益,为HR+/HER2- eBC患者带来辅助强化治疗新选择

2024 ESMO年会上,NATALEE研究4年随访结果再次证实瑞波西利强化辅助治疗方案能够为II-III期患者带来持续的iDFS获益,两组之间的iDFS绝对获益进一步扩大,为临床实践再次增添了用药信心。4年随访研究结果显示,中位随访44.2个月后,所有患者均已停止瑞波西利用药,意向治疗(ITT)人群中,瑞波西利组和对照组的4年iDFS绝对获益为4.9%(88.5% vs 83.6%,HR=0.715,P<0.0001)。而接受瑞波西利联合内分泌治疗后,II期亚组患者的4年iDFS绝对获益可提高4.3%,伴有高危因素的N0亚组患者可提高5.1%。
结合《「健康中国2030」规划纲要》提出的我国癌症防治目标,早期乳腺癌治愈尤为重要,NATALEE是目前CDK4/6抑制剂辅助治疗3期研究中纳入最广泛HR+/HER2-早期乳腺癌患者的临床研究,其获益人群拓展至几乎所有II-III期,包括N0伴有复发风险以及全部N1患者,更加符合临床实际中具有复发风险的早期乳腺癌患者分布。基于该研究的阳性成果,瑞波西利+内分泌治疗的辅助强化治疗适应症已经在FDA获批,我们也期待其在中国适应症尽快获批,惠及更多中国乳腺癌患者。
参考文献:
1. Slamon D, et al. N Engl J Med. 2024 Mar 21;390(12):1080-1091.
2. Zeng H, et al. Lancet Public Health. 2021;6(12):e877-e887.
3. Iqbal J, et al. JAMA 2015; 313: 165–173.
4. Howlader N, et al. J Natl Cancer Inst 2014; 106: dju055.
5. Pan H, et al. N Engl J Med 2017;377: 1836–1846.
6. Bria E, et al. Expert Rev Anticancer Ther 2010; 10:1239–1253.
7. Gelao L, et al. Ecancermedicalscience. 2013 May 21;7:320.
8. Gnant M, et al. J Clin Oncol 2022; 40: 282–293.
9. Loibl S, et al. J Clin Oncol 2021; 39: 1518–1530.
10. Rastogi P, et al. J Clin Oncol. 2024 Mar 20;42(9):987-993.
11. Slamon DJ,et al. Ther Adv Med Oncol. 2023 May 29;15:17588359231178125.
12. Schäffler H, et al. Int J Mol Sci. 2023 Nov 15;24(22):16366.
13. Bardia A.et al. 2023 ESMO LBA23.
14. Denise Yardley, et al. 2024 ASCO. 512.
15. Fasching P, ET AL. 2024 ESMO LBA13.
16. Rao P, et al. In: AACR Annual Meeting 10–15 April and 17–21 May 2021.
17. Peuker CA, et al. Eur J Cancer 2022;162: 45–55.
18. Hamilton E, et al. In: San Antonio Breast Cancer Symposium, San Antonio, TX, 6–10 December 2022.
(上滑查看更多)
查看更多