查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过






孙凤 教授
北大循证医学中心副主任
中国医师协会循证医学专业委员会副主任委员
国际考科蓝中国协作网之北京大学循证医学中心机构主任
世中联临床疗效评价专业委员会副会长
一、仿真/模拟目标RCT研究概述
1.研究背景 —— 效力效果差距
①效力(Efficacy) 是指某种干预措施在最理想条件下所产生的最大期望作用,即 回答干预措施是否起作用;随机对照试验(RCT)是干预措施效力估计的黄金标准。
②效果(Effectiveness) 是指在真实医疗环境下所能达到的作用大小,即回答该干预 措施在临床实践中是否有效;真实世界研究(RWS)是指使用真实世界环境下收集与患者有关的数据,通过分 析,获得医疗产品的实际使用效果或风险的临床证据。
③药物在上市后的临床实践中所表现出的效果通常与提交的RCT结果存在差异,这种RCT结果和RWE之间的潜在差异被称为效力 -效果差距(Efficacy -Effectiveness Gap)。
④产生原因:RWS人群异质性大,包括身高、体重、年龄、合并症、疾病基线严重程度等差异;患者和医疗提供者的行为差异 ,患者依从性差和可能会出现偏离临床指南的干预措施等, 如可能存在超适应症用药情况和不合理用药问题;研究设计和/或治疗效果测量差异,RWS往往采用观察性研究方法,无法严格遵循随机化 且数据来源广泛,测量方法不一等原因而导致RWS的标准化和随机化程度都不如RCT。
2.目标RCT仿真/模拟研究概述
RCT及其Meta分析提供流行病学研究的最高等级证据,是验证科学假设 的理想首选。但RCT往往花费巨大、耗时长,个别情况下甚至会违背伦 理或没有实际可行性。现实中RCT往往难以开展或难以满足当下的证据 需求。因而,观察性研究有时会成为循证决策的主要证据来源。
观察性研究的统计分析过程实质上可以看作是在模拟相对应的RCT(倾向性评分匹配、逆概率加权、工具变量等方法减轻混杂因素干扰)。但除了混杂偏倚,也有明显的选择偏、倚等,主要是因为研究者没有从头至尾贯彻模拟RCT的思路。
为此,哈佛大学公共卫生学院的Miguel Hernan教授完善了模拟目标试验(emulate a target trial)的方法框架,并应用于队列研究和巢式病例对照研究,以研究流行病学的实际问题。
(1)概念:模拟目标临床试验( emulate target trial),主张在设计观察性研究时,通过假想一个解决研究问题的目标临床试验 ,参照目标临床试验进行观察性研究的关键因素设计 ,在因果推断方法学的合理运用下也可以达到RCT试验的效果。
(2)模拟目标试验的方法主要分为三步:
①确定理想中的目标RCT的试验方案,至少应包含研究对象的纳入排除标准、干预措施等7部分
②根据目标试验的方案,基于观察性数据,制定对应的RCT的模拟方案
③评价一致性
(3)两个关键考虑
模拟目标试验方法的关键之一:便是实现研究对象的入组、干预分配和随 访开始时间的同步。
在RCT中,研究对象的入组、干预的分配和随访的开始是同步的,即随访开始时间( time zero)是研究对象达到纳入排除标准的入组时间,也是干预措施的分配时间。因此,RCT避免了恒定时间偏倚和和现使用者偏倚。
如果要使用观察性研究数据实现这一目标,则有以下问题需要解决:
①治疗分配时刻 :在真实世界研究中,无法实现入组和干预分配的同步(现使用者偏倚);
②随访时刻 :在观察性研究中,研究对象可能在多个时间点满足入组标准,都可以作为随访开始时间,但分析时需将随访开始时间确定下来(恒定时间偏倚)。
模拟目标试验方法的关键之二:模拟随机化
新用药者队列 :使用新用药者队列设计来减少现用药者偏倚和不朽时间偏倚,即在零时刻前设定一个洗脱期(180d),仅在洗脱期内有诊疗记录且无目标干预措施处方记录患者被纳入队列之中。
使用患者克隆的方法 :在基线时,每一个满足纳排标准的患者都形成一个相同的克隆分别被分配到干预组和对照组。从容保证干预组与对照组在基线上的完全可比。然后,当患者实际接受的治疗与其分到的组别不一致时,作删失处理。但这种删失是不随机的可能会导致发生信息偏倚,这种潜在偏倚可以在分析中使用删失逆概率权重来解决。
对时依性协变量进行调整:通常的RCT模拟研究使用倾向性评分相关方法来模拟随机化时,通常仅考虑了基线期的协变量,而未考虑基线变量的时变性,如用药和患病情况的改变,而已有研究探讨将时依性变量校正相关方法(边际结构模型与逆概率加权结合)应用到RCT模拟研究之中。
高维倾向性评分 :通常的RCT模拟研究会提前确定需要校正的基线协变量,由于PS仅能校正确定的基线协变量,因此需要纳入较多的基线协变量,但是多数协变量在PS前后组间差异并无意义,而且部分可能对结局有关的需要校正的基线协变量无法直接在数据库中进行获取,但可以通过其他协变量进行间接校正时,使用高维倾向性评分可能是一个不错的选择。因此已有研究探讨在RCT模拟研究中使用高维倾向性评分方法,自动挑选基线协变量进行匹配。
二、全球模拟/复制目标RCT研究现状
1.利用Bibliometrix探索研究进展
检索Pubmed及Web of Science数据库;检索出14078篇文献,进行剔重、筛选后,共纳入文献220篇;利用Bibliometrix对年发文量、发文期刊、高被引文献、发文 作者及机构、发文国家、关键词等进行可视化分析
2.结果展示
(1)年发文量
该领域发文时间在2007-2023年。其中,在2007-2018年间只有零星的发表;之后
开始急剧增加,在2022年达到高峰(105篇)。
(2)发文期刊
纳入文献共涉及130本杂志,发文量频次排名前3的杂志依次为《JAMA NETWORK OPEN》(10篇)、《ANNALS OF INTERNAL MEDICINE》(9篇)、CLINICAL PHARMACOLOGY & THERAPEUTICS(9篇)。
(3)发文作者
纳入文献共计1248名作者,发文2篇及以上的作者共48人,作者合作指数为7.88,处于较高水平。应用Bibliometrix软件分析作者的年发文量可知,HERNAN MA作者的年发文量最大、被引次数最多、H-index指数最高。
(4)发文国家
共涉及28个国家,美国发文量最多(109篇),其次为英 国(16篇)、荷兰(11篇)、 法国(9篇)、德国(9篇)、 瑞士(8篇)。中国发文量仅5篇。国际间合作方面,美国与英国合作16篇,美国与加拿大及西班牙各合作10篇。
三、RCT Duplicate国际经验
1.RCT Duplicate研究背景
在Hernan基础之上,2018年由FDA、哈佛大学布莱根妇女医院以及Aetion公司共同牵头发起的RCT Duplicate项目,旨在利用医疗索赔数据重复37个RCT(30个已完成、7个ongoing),并阐述了目标RCT的筛选过程、模拟目标RCT的关键特征的界定、以及RCT与RWE结果的对比策略等。
其主要目标包括以下三部分:
①确定在新药审批以及药品上市后适应证扩展环节,RWE是否可以补充甚至取代作 为金标准的RCT以及如何起到充分补充作用;
②探讨何种类型的临床问题可以利用RWD进行分析,以及如何利用RWD进行相关研究设计和统计分析;
③规范RWE研究流程步骤及相关统计分析策略的建立。
2.项目实施流程

3.RCT Duplicate: 真实世界证据的“真实性”判断标准
(1)监管一致性:RWE研究模拟RCT结果的方向和统计显著性的能力。如模拟优效性RCT的RWE研究结果也应该是优效的。对于非劣效性RCT ,RWE研究显示的非劣效性应使用与RCT相同的界值。
(2)估计值一致性:当RWE研究的治疗效果估计处于RCT治疗效力估计值的95% CI内,即满足估计值的一致性。
(3)标准化差异SD:项目组还通过计算RCT和RWE研究结果效应估计值之间的标准化差异(standardized difference, SD)来进行假设检验并评估结果是否存在差异。
如RCT报告的HR=0.85, 95%CI(0.71-1.02),RWE研究 的HR=0.85, 95%CI(0.73-0.99),此时RWE研究与RCT未达到监管一致性,但满足估计值一致性。
四、案例展示
1.基于宁波鄞州区医疗大数据开展NCT00881530真实世界模拟研究:西格列汀联用二甲双胍的90周有效性与安全性分析
2.实证研究——数据源
数据来源为基于宁波市鄞州区医疗健康大数据分析平台数据;
主要包括:患者表、就诊表、观察期表、疾病状况表、用药记录表、操作表、检查表、死亡表;涵盖2021年12月31日前鄞州区三级医疗系统中所有就诊记录信息,以及当地公卫系统建档立卡登记信息和人口统计学信息等。
3.实证研究 —— 模拟RCT关键特征
①模拟RCT纳入标准
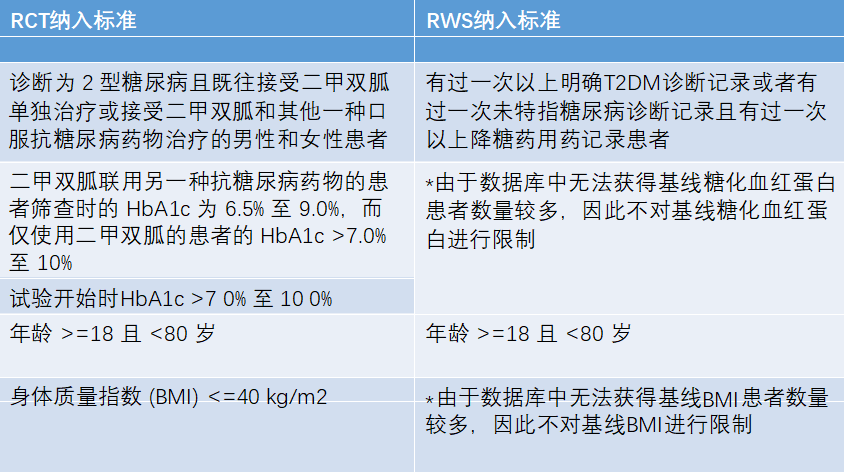
②模拟RCT排除标准
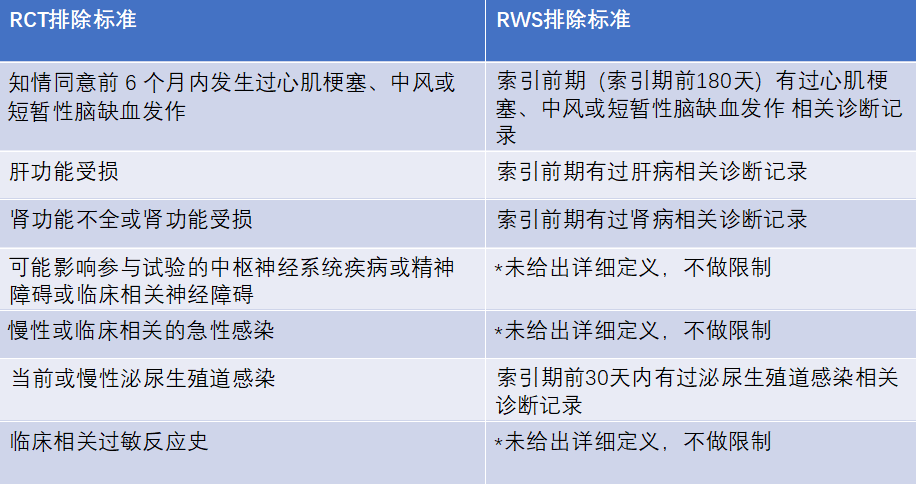
③模拟RCT关键特征——治疗定义与索引期定义
西格列汀+二甲双胍:规定时间窗内(2015年1月1日-2021年12月31日)有西格列汀处方记录且在索引前期有过二甲双胍处方记录,或者有西格列汀-二甲双胍复合制剂处方记录的T2DM患者。
二甲双胍:除干预组外,在规定时间窗内有过二甲双胍处方记录的其他T2DM患者。
基线协变量:(由于RCT随机化可以校正所有已知和未知协变量,而PS只能校正已知 协变量, 因此要尽可能收集对接结局产生影响的协变量)
包括:人口统计学特征,包括年龄、性别;行为和生活方式,包括吸烟、饮酒;T2DM的患病时间;糖尿病联合用药,包括胰岛素、磺脲类药物、SGLT -2等;可能对结局造成影响的合并用药,包括利尿剂、β-受体阻滞剂、钙通道阻滞剂、血管紧张素转换酶抑制剂、血脂调节剂等;基线合并症,高血压、高血脂、风湿等;糖尿病并发症和严重程度指数 (Diabetes complication and severity index,DCSI)
④模拟RCT关键特征——随访时间
干预组将西格列汀随访期内第一次使用除西格列汀和二甲双胍以外的降糖药的时间作为终止时间;或末次西格列汀处方记录+30天作为终止时间。
对照组将除二甲双胍随访期内第一次使用二甲双胍以外的降糖药的时间作为删失时间;或末次二甲双胍记录+30天作为终止时间。
五、小结
Target Trial的概念由Hernan等提出,强调开展RWS时要模拟RCT的关键特征,包括七个方面:采用与RCT相同的纳排标准、治疗策略、分配程序(倾向性评分、逆概率加权等)、随访时间、结局定义、因果分析策略(ITT,PP)和分析计划,从而增强RWS研究质量以及与RCT人群的可比性。
该方法框架可以作为既往观察性研究方法学质量的评价工具,大多数研究存在可以避免的方法学缺陷。
模拟目标试验并不是一种新的流行病学设计,仍然无法规避观察性研究的“先天缺点”(如残余混杂和测量偏倚等)。
模拟目标试验的分析过程也基于一系列的假设,容易受到研究者的影响。模拟目标试验也无法实现RCT的盲法和严谨的数据收集,其在证据等级上仍无法与RCT相比。
贯彻模拟目标试验的方法最好基于纵向随访的数据,已发表的文献往往是基于纵向随访调查的队列研究或者医保数据。即使没有类似的数据资料,模拟目标试验的思想对观察性研究也有普适性。
虽然使用倾向性评分相关技术来对基线协变量进行校正,但对于基线期的定义,和基线协变量的确认、倾向性评分相关技术,不同的工作组所采用的方法仍有一定区别。
查看更多