查看更多
密码过期或已经不安全,请修改密码
修改密码
壹生身份认证协议书
同意
拒绝

同意
拒绝

同意
不同意并跳过





三阴性乳腺癌的雌激素受体(ER)、孕激素受体(PR)、人类表皮生长因子受体(HER2)均为阴性,对内分泌治疗和HER2靶向治疗无效,而且对人体免疫细胞和免疫治疗药物可产生免疫排斥。既往研究发现,细胞外基质有助于免疫排斥。不过,减少细胞外基质的方法大多无效或造成不良结局,故有必要找出细胞外基质引起免疫排斥的关键靶点进行靶向治疗。
2021年11月3日,全球自然科学三大旗舰期刊之首、英国《自然》正刊在线发表美国乔治城大学、得克萨斯大学休斯敦健康科学中心、得克萨斯大学健康科学中心、西班牙加泰罗尼亚肿瘤研究所、贝尔维奇生物医学研究所、巴塞罗那大学希伯伦医院肿瘤研究所的研究报告,探讨了细胞外基质引起三阴性乳腺癌免疫排斥的具体机制及其关键靶点。
该研究发现,具有酪氨酸激酶活性的胶原蛋白受体DDR1通过促进三阴性乳腺癌细胞外基质胶原纤维紧密有序排列,如同金钟罩铁布衫,形成免疫排斥屏障。通过基因技术抑制肿瘤DDR1表达,可促进T淋巴细胞向肿瘤内渗透,并清除三阴性乳腺癌小鼠模型体内肿瘤生长。对于人类三阴性乳腺癌,DDR1表达与抗肿瘤T淋巴细胞在肿瘤内的丰度成反比,也证实了上述发现。免疫排斥必需的是DDR1细胞外结构,而非其细胞内结构。即使免疫活性宿主DDR1基因被剔除,从细胞膜脱落的DDR1细胞外结构也足以维持肿瘤生长。根据机制分析,DDR1细胞外结构域与胶原蛋白结合,可使胶原纤维紧密有序排列并阻碍免疫浸润。利用单克隆抗体对DDR1细胞外结构域进行中和,即可破坏胶原纤维排列,减轻免疫排斥并抑制免疫活性宿主体内肿瘤生长。
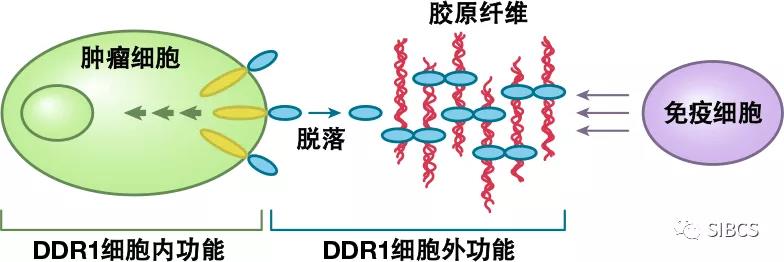
因此,该研究结果表明,三阴性乳腺癌细胞的胶原蛋白受体DDR1细胞外结构可促进细胞外基质胶原纤维紧密有序排列,从而形成免疫排斥屏障。利用靶向药物抑制该靶点,即可恢复肿瘤细胞外基质胶原纤维排列,破解三阴性乳腺癌排斥免疫的金钟罩铁布衫,显著增强人体免疫细胞和免疫治疗药物对三阴性乳腺癌的杀伤力,故有必要进一步开展人体临床研究进行验证。
SIBCS 平台发布
查看更多